Регуляция секреции АДГ. Факторы приводящие к секреции АДГ
Обновлено: 16.05.2024
Для цитирования: Центральный несахарный диабет - современные представления о диагностике и лечении. РМЖ. 2014;13:966.
Центральный несахарный диабет (ЦНД) - это тяжелое заболевание гипоталамо-гипофизарной системы, имеющее в своей основе дефект синтеза или секреции антидиуретического гормона (АДГ). Распространенность ЦНД варьирует от 0,004-0,01%. Заболевание чаще встречается у женщин, чем у мужчин, и начинается в 20-30-летнем возрасте [17].
Синтез и секреция антидиуретического гормона
Антидиуретический гормон вазопрессин синтезируется в супраоптических и паравентрикулярных ядрах гипоталамуса. Связываясь с нейрофизином, комплекс в виде гранул транспортируется к терминальным расширениям аксонов нейрогипофиза и срединного возвышения. В контактирующих с капиллярами окончаниях аксонов происходит накопление АДГ. Секреция АДГ зависит от осмоляльности плазмы, циркулирующего объема крови и уровня АД. На изменения электролитного состава крови реагируют осмотически чувствительные клетки, находящиеся в околожелудочковых отделах переднего гипоталамуса. Повышенная активность осморецепторов при повышении осмоляльности крови стимулирует вазопрессинергические нейроны, из окончаний которых в общий кровоток выделяется вазопрессин. В физиологических условиях осмоляльность плазмы находится в пределах 282-300 мОсм/кг [5]. В норме порогом для секреции АДГ является осмоляльность плазмы крови начиная с 280 мОсм/кг. Более низкие значения для секреции АДГ могут наблюдаться при беременности, острых психозах, онкологических заболеваниях. Снижение осмоляльности плазмы, вызванное приемом большого количества жидкости, подавляет секрецию АДГ. При уровне осмоляльности плазмы более 295 мОсм/кг отмечаются повышение секреции АДГ и активация центра жажды (рис. 1). Контролируемый осморецепторами сосудистого сплетения передней части гипоталамуса активированный центр жажды и АДГ препятствует дегидратации организма [18].
Регуляция секреции вазопрессина зависит и от изменений объема крови. При кровотечениях существенное влияние на секрецию вазопрессина оказывают волюморецепторы, расположенные в левом предсердии. В сосудах АД действует через , которые располагаются на гладкомышечных клетках сосудов. Вазоконстрикторное действие вазопрессина при кровопотере обусловлено сокращением гладкомышечного слоя сосуда, что препятствует падению АД. При снижении АД более чем на 40% отмечается повышение уровня АДГ, в 100 раз превышающее значение его базальной концентрации [1, 3]. На повышение АД реагируют барорецепторы, расположенные в каротидном синусе и дуге аорты, что в конечном итоге приводит к снижению секреции АДГ. Кроме этого, АДГ участвует в регуляции гемостаза, синтезе простагландинов, способствует высвобождению ренина [6].
Ионы натрия и маннитол являются мощными стимуляторами секреции вазопрессина. Мочевина не влияет на секрецию гормона, а глюкоза приводит к торможению его секреции [3].
Механизм действия антидиуретического гормона
АДГ является самым важным регулятором задержки воды и обеспечивает гомеостаз жидкости совместно с предсердным натрийуретическим гормоном, альдостероном и ангиотензином II.
Главный физиологический эффект вазопрессина заключается в стимуляции реабсорбции воды в собирательных канальцах коркового и мозгового слоя почек против осмотического градиента давления [6].
В клетках почечных канальцев АДГ действует через (вазопрессиновые рецепторы 2 типа), которые располагаются на базолатеральных мембранах клеток собирательных канальцев. Взаимодействие АДГ с приводит к активации вазопрессинчувствительной аденилатциклазы и повышению продукции циклического аденозинмонофосфата (АМФ). Циклический АМФ активизирует протеинкиназу, А, которая в свою очередь стимулирует встраивание белков водных каналов, в апикальную мембрану клеток. Это обеспечивает транспорт воды из просвета собирательных трубочек в клетку и далее: через находящиеся на базолатеральной мембране белки водных каналов и вода транспортируется в межклеточное пространство, а затем в кровеносные сосуды. В результате образуется концентрированная моча с высокой осмоляльностью (рис. 2).
Осмотическая концентрация — это суммарная концентрация всех растворенных частиц. Она может трактоваться как осмолярность и измеряться в осмоль/л или как осмоляльность — в осмоль/кг. Различие между осмолярностью и осмоляльностью заключается в способе получения данной величины. Для осмолярности — это расчетный способ по концентрации основных электролитов в измеряемой жидкости. Формула расчета осмолярности:
Осмолярность = 2 х + глюкоза (ммоль/л) + мочевина (ммоль/л) + 0,03 х общий белок () [5].
Осмоляльность плазмы, мочи и других биологических жидкостей — это осмотическое давление, зависящее от количества ионов, глюкозы и мочевины, которое определяется с помощью прибора осмометра. Осмоляльность меньше осмолярности на величину онкотического давления.
При нормальной секреции АДГ осмолярность мочи всегда выше 300 мОсм/л и может увеличиваться даже до 1200 мОсм/л и выше. При дефиците АДГ осмолярность мочи ниже 200 мосм/л [4, 5].
Этиологические факторы центрального несахарного диабета
Среди первичных причин развития ЦНД выделяют наследственную семейную форму заболевания, передаваемую по или типу наследования. Наличие заболевания прослеживается в нескольких поколениях и может затрагивать ряд членов семьи, оно обусловлено мутациями, приводящими к изменениям в строении АДГ (DIDMOAD- синдром). Врожденные анатомические дефекты развития среднего и промежуточного мозга также могут быть первичными причинами развития ЦНД. В 50-60% случаев первичную причину ЦНД установить не удается — это так называемый идиопатический несахарный диабет [17].
Среди вторичных причин, приводящих к развитию ЦНД, называют травму (сотрясение головного мозга, травма глазницы, перелом основания черепа).
Развитие вторичного НСД может быть связано с состояниями после транскраниальной или транссфеноидальной операций на гипофизе по поводу таких опухолей головного мозга, как краниофарингиома, пинеалома, герминома, приводящих к сдавлению и атрофии задней доли гипофиза [12].
Воспалительные изменения гипоталамуса, супраоптикогипофизарного тракта, воронки, ножки, задней доли гипофиза также являются вторичными причинами развития ЦНД.
Ведущим фактором в возникновении органической формы заболевания является инфекция. Среди острых инфекционных заболеваний выделяют грипп, энцефалит, менингит, ангину, скарлатину, коклюш; среди хронических инфекционных заболеваний — туберкулез, бруцеллез, сифилис, малярию, ревматизм [9, 10].
Среди сосудистых причин ЦНД можно назвать синдром Шиена, нарушения кровоснабжения нейрогипофиза, тромбозы, аневризмы.
В зависимости от анатомической локализации ЦНД может быть постоянным или транзиторным. При повреждении супраоптического и паравентрикулярных ядер функция АДГ не восстанавливается.
В основе развития нефрогенного НД лежат врожденные рецепторные или ферментативные нарушения дистальных канальцев почек, приводящие к резистентности рецепторов к действию АДГ. При этом содержание эндогенного АДГ может быть нормальным или повышенным, а прием АДГ не устраняет симптомы заболевания. Нефрогенный НД может встречаться при длительно текущих хронических инфекциях мочевыводящих путей, мочекаменной болезни (МКБ), аденоме предстательной железы.
Симптоматический нефрогенный НД может развиться при заболеваниях, сопровождающихся повреждением дистальных канальцев почек, таких как анемия, саркоидоз, амилоидоз. В условиях гиперкальциемии снижается чувствительность к АДГ и уменьшается реабсорбция воды.
Психогенная полидипсия развивается на нервной почве преимущественно у женщин менопаузального возраста (табл. 1). Первичное возникновение жажды обусловлено функциональными нарушениями в центре жажды [14]. Под влиянием большого количества жидкости и увеличения объема циркулирующей плазмы посредством барорецепторного механизма происходит снижение секреции АДГ. Исследование мочи по Зимницкому у этих пациентов выявляет снижение относительной плотности, тогда как концентрация натрия и осмолярность крови остается нормальной или пониженной. При ограничении употребления жидкости самочувствие больных остается удовлетворительным, при этом уменьшается количество мочи, а ее осмолярность повышается до физиологических пределов [11].
Клиническая картина центрального несахарного диабета
Для манифестации НД необходимо снижение секреторной способности нейрогипофиза на 85% [2, 8].
Основными симптомами НД являются обильное учащенное мочеиспускание и сильная жажда. Часто объем мочи превышает 5 л, может даже достигать 8-10 л в сутки.
Гиперосмолярность плазмы крови стимулирует центр жажды. Пациент не может обходиться без приема жидкости более 30 мин. Количество выпитой жидкости при легкой форме заболевания обычно достигает 3-5 л, при средней степени тяжести — 5-8 л, при тяжелой форме — 10 л и более. Моча обесцвечена, ее относительная плотность — 1000-1003 . В условиях избыточного употребления жидкости у больных снижается аппетит, происходит перерастяжение желудка, снижается секреция, замедляется моторика ЖКТ, развиваются запоры. При поражении гипоталамической области воспалительным или травматическим процессом наряду с НД могут наблюдаться и другие нарушения, такие как ожирение, патология роста, галакторея, гипотиреоз, сахарный диабет (СД) [3, 5]. При прогрессировании заболевания обезвоживание приводит к сухости кожи и слизистых, уменьшению слюно- и потоотделения, развитию стоматитов и назофарингитов. При резком обезвоживании начинают нарастать общая слабость, сердцебиение, отмечается снижение АД, быстро усиливается головная боль, появляется тошнота. Больные становятся раздражительными, могут быть галлюцинации, судороги, коллаптоидные состояния.
Диагностика центрального несахарного диабета
Для подтверждения диагноза на первом этапе обследования должны быть исключены наиболее частые причины нефрогенного НД (сахарный диабет, гиперкальциемия, гипокалиемия, воспалительные заболевания почек). При выявлении гиперосмолярности плазмы (более 3000 мОсм/кг), гипернатриемии и гипоосмолярности мочи (100-200 мОсм/кг) переходят ко второму этапу обследования [5].
На этом этапе обследования проводят пробу с дегидратацией (проба с сухоедением) для исключения первичной полидипсии и тест с десмопрессином для исключения нефрогенного НД.
Классическая проба с сухоедением заключается в запрещении употребления любой жидкости в течение 6-14 ч. До и в ходе теста (каждые 1-2 ч) измеряются масса тела, АД, пульс, определяется осмоляльность плазмы крови, содержание натрия в плазме крови, объем и осмоляльность мочи. Проба с сухоедением прекращается при потере пациентом массы тела более 5%, невыносимой жажде, нарастании содержания натрия и повышении осмоляльности крови выше границ нормы. Если в ходе пробы осмоляльность крови > 300 мОсм/кг, уровень натрия >145 ммоль/л, при этом осмоляльность мочи
Если после введения десмопрессина уровень осмоляльности мочи увеличивается более чем на 50%, диагностируется центральная форма НД. Если эффект от вводимого препарата менее 50% или отсутствует, это свидетельствует о нефрогенной форме НД.
Трудности в диагностике представляют частичные формы ЦНД, нефрогенного НД, первичной полидипсии, в этих случаях отсутствует яркая клиническая картина. После пробы с сухоедением осмоляльность мочи у этих пациентов определяется в диапазоне от 300 до 750 мОсм/кг, после приема десмопрессина осмоляльность мочи составляет
Пациентам с подтвержденным диагнозом ЦНД проводится томография головного мозга для установления причины заболевания и выявления патологических изменений области [5].
Лечение
Заместительная терапия ЦНД проводится синтетическим аналогом АДГ — десмопрессином. Особенности химической структуры десмопрессина заключаются в замещении в положении цепи , а также дополнительное дезаминирование цистеина в положении. Препарат действует только на почечных канальцев и не действует на гладкой мускулатуры кровеносных сосудов. В связи с этим на фоне приема препарата отмечаются минимальная сосудосуживающая активность и более выраженный и продолжительный антидиуретический эффект [16].
Среди лекарственных форм десмопрессина выделяют: таблетированную пероральную форму, таблетированную подъязычную форму и интраназальный спрей (табл. 2). При ЦНД средние терапевтические дозы таблетированного десмопрессина варьируют от 0,1 мг до 1,6 мг/сут, кратность приема составляет 2-3 р./сут. При употреблении таблетированной подъязычной формы начальная доза препарата — 60 мкг 2-3 р./сут, средняя суточная — от 60 до 360 мг/сут. При интраназальном введении препарата суточная доза — от 10 мкг до 40 мкг/сут, что обусловлено индивидуальной чувствительностью к препарату; кратность приема — 2 р./сут [7, 13].
При приеме таблетированной формы антидиуретический эффект наблюдается через 1-2 ч. Интраназальное введение обеспечивает более быстрое начало действия через 15-30 мин, введение препарата не связано с приемом пищи, что обеспечивает большую биодоступность [15]. Также быстрый терапевтический эффект отмечается при применении сублингвальной формы препарата, начало действия которой — 15-45 мин после приема. Интервал между приемом препарата и приемом пищи составляет 5-10 мин.
Необходимо учитывать, что прием пищи снижает абсорбцию препарата и его эффективность, поэтому рекомендовано принимать таблетированную форму препарата натощак за 30-40 мин до приема пищи или через 2 ч после него. Интраназальный спрей может применяться независимо от приема пищи у пациентов с различными заболеваниями ЖКТ, у больных в условиях реанимационных отделений. В то же время катаральные явления у пациентов существенно затрудняют лечение этой формой десмопрессина. Подъязычная форма введения препарата практически не связана с приемом пищи, легко титруется. Эта форма десмопрессина позволяет более точно подбирать необходимую дозу препарата.
При замене или при переходе с одной формы десмопрессина на другую производят перерасчет принимаемой дозы (табл. 3).
Заключение
В настоящее время для эффективного лечения пациентов с ЦНД используются различные формы десмопрессина. Только индивидуальный подбор препарата и титрация его дозы позволяют добиться клинической и лабораторной компенсации заболевания.
Параграф 113. 1. Антидиуретический гормон. АДГ
Содержание параграфа:
1. Антидиуретическое действие АДГ:
2. Механизм снижения диуреза под действием АДГ.
3. Другие эффекты АДГ.
4. Функции АДГ.
5. Места образования и секреции АДГ.
6. Регуляция секреции АДГ - п.6, 91.
7. Нарушения, связанные с АДГ (патологические аспекты).
8. Лекарства при несахарном диабете:
9. Сравнение несахарного диабета и сахарного диабета (п.103) (сходства и отличия).
1. Антидиуретическое действие АДГ:
Антидиуретический гормон (АДГ) снижает диурез
(снижает количество мочи),
как ясно из его названия.
Смысл снижения диуреза в том, чтобы
сохранить воду в организме при ее дефиците, избежать обезвоживания (дегидратации), которое могло бы привести к смерти.
Поэтому при дефиците АДГ диурез им снижается в меньшей степени,
что приводит к повышению диуреза до 10 литров в сутки.
и возникновению очень сильного обезвоживания, опасного для жизни.
Кроме этого, пополнение запасов воды в организме
приводит к тому, что поддерживается нормальная концентрация веществ,
то есть поддерживается нормальное осмотическое давление (ОД).
Иначе при потере воды концентрация стала бы сильно высокой.
Другое название АДГ - вазопрессин.
Поэтому рецепторы АДГ называются V-рецепторами.
2. Механизм снижения диуреза под действием АДГ.
Чтобы снизить диурез,
АДГ действует на почки через V2-рецепторы,
при этом вторым посредником является цАМФ - п.95.
Это приводит к увеличению синтеза белков,
которые называются АКВАПОРИНАМИ
и которые обеспечивают поступление (возвращение) воды
из первичной мочи в обратно в кровь
(то есть реабсорбцию воды).
3. Другие эффекты АДГ.
Снижение диуреза снижает, но не прекращает потерю жидкости организмом.
Для восполнение потери жидкости организмом нужно ещё выпить воду,
поэтому АДГ вызывает чувство ЖАЖДЫ
(действуя на рецепторы гипоталамуса).
Если возможности попить нет, то потеря жидкости приводит к обезвоживанию -
при этом снижается объем плазмы и артериальное давление,
что приводит к снижению кровоснабжения тканей,
в том числе мозга, почек.
Чтобы повысить артериальное давление
и улучшить кровоснабжение тканей
в условиях невозможно повысить объём плазмы (при отсутствии воды),
АДГ сужает сосуды (ВАЗОКОНСТРИКЦИЯ)
за счёт сокращения гладких мышц сосудов,
действуя через V1-рецепторы.
Вторым посредником при этом эффекте являются ионы кальция Cа++ - п.97.
Таким образом, функции АДГ - адаптировать организм к потере воды:
1) снизить потери воды с мочой (уменьшив образование мочи),
2) обеспечить организм водой за счёт вызывания жажды
3) и предотвратить падение артериального давления в условиях отсутствия воды
за счёт сужения сосудов.
5. Места образования и секреции АДГ.
Синтез АДГ происходит в гипоталамусе,
затем АДГ по отросткам нейронов (по аксонам)
поступает в нейрогипофиз, которым и секретируется в кровь.
Таким образом, нейрогипофиз не синтезирует АДГ,
он его только секретирует в кровь, а синтезирует гипоталамус.
6. Регуляция секреции АДГ - п.6, 91.
АДГ должен секретировать и действовать только тогда, когда это нужно организму, то есть при дефиците воды.
Другими словами, секреция АДГ должна соответствовать потребностям организма.
Секреция АДГ увеличивается,
когда он нужен, то есть при дефиците воды в организме (при обезвоживании).
Дефицит воды проявляется в:
1) в снижении артериального давления и ОЦК,
2) в высокой [Na+, Cl -] и соответственно высоком осмотическом давлении.
(Слишком высокой концентрации веществ).
Снижение секреции АДГ.
При повышении артериального давления и ОЦК
секреция АДГ, наоборот, снижается
(так как необходимость в его эффектах снижается).
Когда количество воды в сосудах становится нормальным
в результате работы АДГ, то
снижается концентрация веществ в крови
и снижается осмотическое давление -
это является сигналом для
снижения синтеза АДГ гипоталамусом (по принципу ООС).
При тошноте, рвоте, операциях на ЖКТ секреция АДГ увеличивается
(это проявляется в прекращении выделения мочи - в анурии) -
возможно, потому что в этих случаях есть вероятность значительной потери жидкости.
7. Нарушения, связанные с АДГ (патологические аспекты).
Дефицит АДГ приводит к:
к снижению эффектов АДГ и сильному повышению диуреза (полиурии) до 10 и более литров в сутки.
Это нарушение называется несахарным диабетом
(диабет означает «мочеизнурение»).
Потеря большого количества жидкости
приводит к сильному обезвоживанию,
которое вызывает сильную жажду:
настолько сильную, что человек способен пить из лужи и т.п..
8. Лекарства при несахарном диабете:
Для спасения человека при несахарном диабете
применяются агонисты рецепторов АДГ (десмопрессин).
Причиной дефицита АДГ
может быть повреждение гипоталамуса (места синтеза) и нейрогипофиза.
Бывает повреждение рецепторов АДГ -
в этом случае не помогут агонисты АДГ.
9. Сравнение несахарного диабета и сахарного диабета (п.103).
(сходства и отличия)
Сходство несахарного диабета и сахарного диабета только в том, что
при обеих патологиях очень много мочи, то есть в полиурии.
Причины полиурии.
Причины полиурии при несахарном диабете - дефицит АДГ,
а причина полиурии при сахарном диабете это избыток веществ,
растворённых в моче (то есть высокое осмотическое давление мочи).
Концентрация мочи.
При несахарном диабете концентрация веществ в моче очень низкая,
то есть моча разбавленная.
При сахарном диабете концентрация веществ в моче очень высокая,
то есть соча концентрированная.
Портал Проза.ру предоставляет авторам возможность свободной публикации своих литературных произведений в сети Интернет на основании пользовательского договора. Все авторские права на произведения принадлежат авторам и охраняются законом. Перепечатка произведений возможна только с согласия его автора, к которому вы можете обратиться на его авторской странице. Ответственность за тексты произведений авторы несут самостоятельно на основании правил публикации и законодательства Российской Федерации. Данные пользователей обрабатываются на основании Политики обработки персональных данных. Вы также можете посмотреть более подробную информацию о портале и связаться с администрацией.
© Все права принадлежат авторам, 2000-2022. Портал работает под эгидой Российского союза писателей. 18+
Регуляция секреции АДГ
Осмомолярность крови и внеклеточной жидкости является одним из жестких параметров внутренней среды. Изменение этого показателя регистрируют осморецепторы. Существование осморецепции было установлено Вернеем в 1947 году. Им показано, что интракаротидное введение гипертонических растворов сопровождается отчетливым торможением диуреза.
У людей, собак, крыс была установлена строгая линейная зависимость между осмомолярностью плазмы крови и концентрацией АДГ. Сдвиги осмотического давления воспринимаются осморецепторами. Эти рецепторы расположены в сосудах печени, почек, селезенки, поджелудочной железы, некоторых мышц (периферические осморецепторы). Они воспринимают изменение осмотического давления и передают эту информацию к супраоптическому ядру гипоталамуса (центральное звено осморецепции).
Помимо осморецепторов, в механизмах осмотического гомеостаза имеют значение волюморецепторы, реагирующие на изменение объема внутрисосудистой и внеклеточной жидкости. Волюморецепторы расположены во многих крупных сосудах , венах, артериях, а также в обоих предсердиях. От них информация передается к нейронам гипоталамуса и продолговатого мозга (к центру волюморегуляции). Ведущее значение в регуляции секреции АДГ имеют те волюморецепторы, которые реагируют на изменение напряжения сосудистой стенки в области низкого давления - барорецепторы, которые локализуются в афферентных артериолах почечных клубочков, в сонной артерии, дуге аорты, правом желудочке в каротидном синусе. Активация волюморецепторов, возникающая в ответ на увеличение объема жидкости, приводит к повышению экскреции солей натрия и воды.
Осморецепторы чутко реагируют на сдвиги концентраций осмотически активных веществ плазмы крови. При увеличении осмолярности плазмы крови на 1%, концентрация АДГ возрастает на 1 пг/мл (пикограмм равен миллионной доле микрограмма). Переход к состоянию максимального осмотического концентрирования мочи требует 10-кратного возрастания количества АДГ в крови.
Нейрогипофизарный механизм
В условиях дефицита воды увеличивается концентрация осмотически активных веществ, увеличивается осмотическое давление, возбуждаются осморецепторы, барорецепторы и волюморецепторы, от которых информация достигает центра регуляции ионного состава, который расположен в области супраоптического ядра, где усиливается секреция АДГ.
Механизм антидиуретического действия АДГ (вазопрессина) состоит в усилении обратного всасывания воды стенками собирательных трубочек нефрона.
Таким образом, происходит экономия воды организмом.
При избыточном содержании воды в организме, концентрация растворенных осмотически активных веществ снижается и ее осмотическое давление падает. Это уменьшает активность периферических и центральных осморецепторов, что снижает выделение АДГ из нейрогипофиза в кровь и приводит к усилению выделения воды почками (рис. 4.2.3.)
Кроме того, АДГ стимулирует центр жажды, т.е. вызывает повышение поступление воды в организм, что также способствует нормализации осмотического давления. Важную роль в обеспечении осмотического гомеостаза играет: ренин-ангиотензин-альдостероновая система.

Рис. 4.2.3. Механизмы, регулирующие секрецию АДГ задней долей гипофиза
- супраоптическое и паравентрикулярные ядра гипоталамуса;
- задняя доля гипофиза;
- внутренняя сонная артерия;
- каротидное тельце;
- каротидный синус;
- аорта;
- левое предсердие;
- правое предсердие;
- правый желудочек;
- почка.
Окситоцин
Синтез окситоцина в гипоталамических нейронах и его секреция нейрогипофизом в кровь стимулируется рефлекторным путем при раздражении рецепторов растяжения матки и механорецепторов сосков молочных желез. Усиливают секрецию гормона эстрогены.
Основные эффекты окситоцина заключаются в стимуляции сокращения матки при родах, сокращении гладких мышц протоков молочных желез, что вызывает выделение молока, а также в регуляции водно-солевого обмена и питьевого поведения. Окситоцин является одним из дополнительных факторов регуляции секреции гормонов аденогипофиза, наряду с либерилинами.
| ОСНОВНЫЕ ЭФФЕКТЫ ОКСИТОЦИНА · Стимуляция сокращений матки, особенно, беременной · Стимуляция выделения молока молочными железами. · Диуретический и натриуретический эффекты - угнетение эффектов вазопрессина, регуляция водно-солевого обмена. · Регуляция питьевого поведения. · Повышает и угнетает процессы запоминания, процессы забывания (амнестический гормон). · Гипотензивный эффект. |
Окситоцин - антагонист АДГ и АГ. Он угнетает процессы запоминания. Доказательство: при черепно-мозговых травмах - амнезия, при этом в ликворе имеет место увеличение содержания окситоцина и снижение АДГ.
Окситоцин усиливает доверие (склонность человека доверять незнакомцу, в случае если тот посылает сигналы, не содержащие угрозы). Окситоцин составляет положительную сторону межличностного взаимодействия. Человек буквально чувствует, что ему доверяют и это мотивирует его на ответные шаги.
Окситоцин усиливает сопереживание по отношению к другим людям и мотивирует наше желание помогать им.
У самок млекопитающих окситоцин стимулирует заботу о потомстве, вызывает выделение дофамина в областях, связанных с таким вознаграждающим поведением как секс и принятие пищи. Уровень оситоцина резко возрастает при оргазме, чем объясняют взаимные любовные чувства. Это «гормон объятий».
Как вы ведете себя при стрессе?: Вы можете самостоятельно управлять стрессом! Каждый из нас имеет право и возможность уменьшить его воздействие на нас.
Почему двоичная система счисления так распространена?: Каждая цифра должна быть как-то представлена на физическом носителе.
Регуляция секреции АДГ. Факторы приводящие к секреции АДГ
В статье изложены современные представления об эпидемиологии, этиологии, диагностике и лечении центрального несахарного диабета (ЦНД). Представлен опыт Эндокринологического диспансера Департамента здравоохранения города Москвы по лечению ЦНД с помощью препаратов десмопрессина. Хороший клинический эффект, обеспечивающий длительную компенсацию заболевания, был показан при назначении интраназальной формы препарата (Пресайнекс).
Центральный несахарный диабет (ЦНД) - нейроэндокринное заболевание, имеющее в своей основе дефект синтеза или секреции антидиуретического гормона (АДГ) вазопрессина, проявляющееся выраженной жаждой и выделением большого количества мочи низкой плотности.
Другими вариантами несахарного диабета являются нефрогенный (вазопрессинрезистентный) и психогенный (психогенная полидипсия).
Синтез и секреция АДГ
АДГ вазопрессин синтезируется в супраоптических и паравентрикулярных ядрах гипоталамуса. Далее он связывается с белком-носителем нейрофизином. Комплекс АДГ-нейрофизин в виде гранул транспортируется к терминальным расширениям аксонов нейрогипофиза и срединного возвышения, где и накапливается. Для манифестации ЦНД необходимо снижение секреторной способности нейрогипофиза на 85 % [1, 2, 4, 8].
Секреция АДГ зависит от осмоляльности плазмы, объема циркулирующей крови и уровня артериального давления (АД). На изменения электролитного состава крови реагируют осмотически чувствительные клетки, находящиеся в околожелудочковых отделах переднего гипоталамуса. Повышенная активность осморецепторов при повышении осмоляльности крови стимулирует вазопрессинергические нейроны, из окончаний которых в общий кровоток выделяется вазопрессин. Снижение осмоляльности плазмы, вызванное приемом большого количества жидкости, подавляет секрецию АДГ. В физиологических условиях осмоляльность плазмы находится в пределах 282-300 мосм/кг [5]. Ионы натрия и маннитол являются мощными стимуляторами секреции вазопрессина. Мочевина не влияет на секрецию гормона, а глюкоза приводит к торможению его высвобождения [3].
Регуляция секреции вазопрессина зависит и от изменений объема крови. При кровотечениях существенное влияние на его высвобождение оказывают волюморецепторы, расположенные в левом предсердии. В сосудах АДГ действует через V1-баро/осморецепторы, которые располагаются на гладкомышечных клетках сосудов. Вазоконстрикторное действие вазопрессина при кровопотере обусловлено сокращением гладкомышечного слоя сосуда, что препятствует падению АД. При снижении АД более чем на 40 % отмечается повышение уровня АДГ, в 100 раз превышающее значение его базальной концентрации [1, 3]. На повышение АД реагируют барорецепторы, расположенные в каротидном синусе и дуге аорты, что в конечном итоге приводит к снижению секреции АДГ.
Осмотическая концентрация - это суммарная концентрация всех растворенных частиц. Она может выражаться как осмолярность и измеряться в осмоль/л или как осмоляльность в осмоль/кг. Различие между осмолярностью и осмоляльностью заключается в способе получения данной величины. Для осмолярности это расчетный способ - по концентрации основных электролитов в измеряемой жидкости. Формула расчета для осмолярности: 2 × (Na ммоль/л + К ммоль/л) + глюкоза ммоль/л + мочевина ммоль/л + 0,03 × общий белок г/л [5].
Осмоляльность плазмы, мочи и других биологических жидкостей - это осмотическое давление, зависящее от количества ионов, глюкозы и мочевины, которое определяется с помощью прибора осмометра. Осмоляльность меньше осмолярности на величину онкотического давления.
Механизм действия АДГ
Главный физиологический эффект вазопрессина заключается в стимуляции реабсорбции воды в собирательных канальцах коркового и мозгового слоев почек против осмотического градиента давления [6]. В клетках почечных канальцев АДГ действует через V2-барорецепторы (вазопрессиновые рецепторы 2-го типа), которые располагаются на базолатеральных мембранах клеток собирательных канальцев. Взаимодействие АДГ с V2-рецепторами приводит к активации протеинкиназы А, которая стимулирует встраивание белков водных каналов, в частности аквапорина-2, в апикальную мембрану клеток, что обеспечивает транспорт воды из просвета собирательных трубочек в клетку, и далее через находящиеся на базолатеральной мембране белки водных каналов (аквапорин-3 и аквапорин-4) вода транспортируется в межклеточное пространство, а затем в кровеносные сосуды. В результате моча выделяется концентрированной. При нормальной секреции АДГ осмолярность мочи всегда выше 300 мосм/л, может увеличиваться даже до 1200 мосм/л и выше. При дефиците АДГ осмолярность мочи ниже 200 мосм/л [4, 5].
Эпидемиология ЦНД
Распространенность ЦНД варьируется от 0,004 до 0,010 %. Заболевание чаще встречается у женщин, чем у мужчин, и начинается в 20-30-летнем возрасте [17].
Этиологические факторы ЦНД
Среди первичных форм ЦНД выделяют наследственную семейную разновидность заболевания, передаваемую по аутосомно-доминантному или аутосомно-рецессивному типу наследования. Наличие заболевания прослеживается в нескольких поколениях и может затрагивать ряд членов семьи.
Болезнь обусловлена мутациями, приводящими к изменениям в строении АДГ. Врожденные анатомические дефекты развития среднего и промежуточного мозга также могут быть первичными причинами развития ЦНД. В 50-60 % случаев первичную причину ЦНД установить не удается: это т. н. идиопатический несахарный диабет [17].
Среди вторичных причин, приводящих к развитию ЦНД, отмечают черепно-мозговую травму (сотрясение головного мозга, перелом основания черепа), а также состояния после транскраниальной или транссфеноидальной операции на гипофизе [12]. Развитие вторичного ЦНД может быть связано с опухолями головного мозга - краниофарингиомой, пинеаломой, герминомой, приводящими к сдавлению и атрофии задней доли гипофиза. Воспалительные изменения гипоталамуса, супраоптикогипофизарного тракта, воронки, ножки, задней доли гипофиза также являются вторичными причинами развития ЦНД.
Причиной развития ЦНД могут также стать грипп, энцефалит, менингит, острые инфекционные заболевания (ангина, скарлатина, коклюш), хронические инфекционные заболевания (туберкулез, бруцеллез, сифилис, малярия, ревматизм) [9, 10]. Среди сосудистых причин ЦНД выделяют синдром Шиена, нарушения кровоснабжения нейрогипофиза.
В основе развития нефрогенного несахарного диабета лежат врожденные рецепторные или ферментативные нарушения дистальных канальцев почек, приводящие к резистентности рецепторов к действию АДГ. При этом содержание эндогенного АДГ может быть нормальным или повышенным,
а прием АДГ не устраняет симптомы заболевания. Нефрогенный несахарный диабет может встречаться при длительно текущих хронических инфекциях мочевыводящих путей, мочекаменной болезни, доброкачественной гиперплазии предстательной железы.
Симптоматический нефрогенный несахарный диабет может развиваться при заболеваниях, сопровождающихся повреждением дистальных канальцев почек, таких как серповидно-клеточная анемия, саркаидоз, амилоидоз. В условиях гиперкальциемии снижается чувствительность к АДГ и уменьшается реабсорбция воды.
Психогенная полидипсия развивается “на нервной почве” - преимущественно у женщин менопаузального возраста. Первичное возникновение жажды обусловлено функциональными нарушениями в центре жажды [14]. Под влиянием большого количества жидкости и увеличения объема циркулирующей плазмы посредством барорецепторного механизма происходит снижение секреции АДГ. Исследование мочи по Зимницкому выявляет у этих пациентов снижение относительной плотности, тогда как концентрация натрия и осмолярность крови остаются нормальными или пониженными. При ограничении употребления жидкости самочувствие больных остается удовлетворительным, при этом уменьшается количество мочи, а осмолярность мочи повышается до физиологических пределов [11].
Клиническая картина ЦНД
Основными симптомами несахарного диабета являются обильное учащенное мочеиспускание и жажда. Количество выпитой и выделенной жидкости при легкой форме заболевания обычно достигает 3-5 литров, при средней степени тяжести - 5-8, при тяжелой форме - 10 литров и более. Пациент может обходиться без приема жидкости не более 30 минут. Моча обесцвеченная, ее относительная плотность - 1000-1003 г/л. Обезвоживание приводит к сухости кожи и слизистых оболочек, уменьшению слюно- и потоотделения, развитию стоматитов и назофарингитов. При резком обезвоживании начинает нарастать общая слабость, быстро усиливается головная боль, появляется тошнота. Больные становятся раздражительными, у них могут быть галлюцинации, судороги, коллаптоидные состояния.
В условиях избыточного употребления жидкости у больных снижается аппетит, происходит перерастяже-ние желудка, снижается желудочно-кишечная секреция, замедляется моторика желудочно-кишечного тракта, развиваются запоры. При поражении гипоталамической области воспалительным или травматическим процессом наряду с несахарным диабетом могут наблюдаться и другие нарушения, такие как ожирение, патология роста, галакторея, гипотиреоз, сахарный диабет [3, 5].
Диагностика ЦНД
Диагностика ЦНД основана на жалобах пациентов на жажду и избыточное употребление воды, частое мочеиспускание в течение дня и ночью. При обследовании (анализ мочи по Зимницкому) подтверждение диагноза несахарного диабета основано на полиурии с выделением за сутки от 3 до 20 литров мочи с относительной плотностью 1003-1005 г/л во всех порциях. При биохимическом исследовании крови выявляется гиперосмолярность плазмы более 300 мосм/л (300-320 мосм/л), гипернатриемия более 155 мэкв/л. Моча у пациентов с несахарным диабетом гипоосмолярна
(100-200 мосм/л) [17].
На следующем этапе обследования проводят пробу с дегидратацией для исключения первичной полидипсии и тест с десмопрессином для исключения нефрогенного несахарного диабета. Пациентам с подтвержденным диагнозом ЦНД проводится магниторезонансная томография головного мозга для установления причины заболевания и выявления патологических изменений гипоталамо-гипофизарной области [5].
Лечение ЦНД
Всем пациентам с диагностированным ЦНД назначается десмопрессин - синтетический аналог вазопрессина [9]. Препарат лишен сосудосуживающей активности и обладает более выраженным и продолжительным антидиуретическим эффектом [16]. В настоящее время в России используется 2 формы десмопрессина: таблетированная форма (Минирин) и интраназальный спрей (Пресайнекс). При ЦНД средние терапевтические дозы таблетированного десмопрессина варьируются от 0,1 мг до 1,6 мг/сут, кратность приема - 2-3 раза в день. При интраназальном введении препарата доза составляет от 10 до 40 мкг в сутки, что обусловлено индивидуальной чувствительностью к препарату; кратность приема - 2 раза в день [7, 13].
При приеме таблетированной формы антидиуретический эффект наблюдается через 1-2 часа. Интраназальное введение обеспечивает более быстрое начало действия через 15-30 минут, т. к. введение препарата не связано с приемом пищи, что обеспечивает большую биодоступность. При простудных или аллергических заболеваниях возможно введение препарата сублингвально в дозах, в 1,5-2,0 раза превышающих дозы для интраназального введения [15].
Опыт ведения пациентов с ЦНД
В Эндокринологическом диспансере Департамента здравоохранения города Москвы под наблюдением находятся больные ЦНД. С таблетированной формы десмопрессина на интраназальный спрей были переведены 67 больных: 42 женщины и 26 мужчин в возрасте от 20 до 82 лет.
При переводе учитывалось, что прием 0,2 мг таблетированной формы десмопрессина эквивалентен 10 мкг десмопрессина, вводимого интраназально.

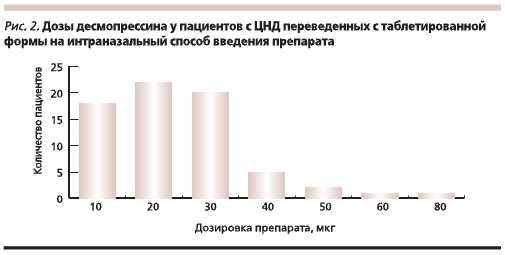
У подавляющего большинства пациентов доза перорального десмопрессина составляла от 0,2 до 0,6 мг/сут (рис. 1). При переводе на интраназальный спрей средние терапевтические дозы десмопрессина варьировались от 10 до 30 мкг/сут. У пациентов, получавших таблетированный десмопрессин в дозе от 1,0 до 1,8 г в сутки, кратность приема составила 8 раз, при переводе на интраназальную форму препарата компенсация заболевания была достигнута на дозе от 60 до 80 мкг/сут с кратностью приема 2 раза в день. Диапазон дозировок интраназального десмопрессина представлен на рис. 2. На фоне приема интраназальной формы препарата выраженных побочных эффектов не отмечено.
Клинические примеры
Больная М. 40 лет. В возрасте 17 лет стала испытывать жажду, выпивала по 8 литров воды в сутки. Впервые обратилась к врачам в 2009 г., когда объем потребляемой жидкости превысил 12 литров, стала нарастать общая слабость и утомляемость. Диагноз несахарного диабета был поставлен на основании жалоб, в анализе мочи по Зимницкому объем суточной мочи - 8550 мл, относительная плотность мочи - 1002-1005 г/л. Пациентке был назначен препарат Пресайнекс в дозе 10 мкг 2 раза в сутки. При повторном визите через месяц пациентка отметила улучшение самочувствия, объем
потребляемой жидкости снизился до 2500 мл. При контрольном анализе мочи по Зимницкому объем суточной мочи - 2350 мл, относительная плотность - 1006-1018 г/л. В дальнейшем титрация дозы не проводилась в связи с достигнутым терапевтическим эффектом препарата. За время наблюдения у пациентки отмечены острые респираторные вирусные инфекции, сопровождавшиеся отеком слизистой оболочки носа. Сублингвальное введение препарата в дозе 30 мкг в сутки было достаточным для устранения симптомов полиурии и полидипсии. Больной М. 19 лет. Диагноз несахарного диабета установлен в 14 лет после удаления герминомы пениальной области и курса химиолучевой терапии. Принимал Минирин 0,1 мг по 1 таблетке 3 раза в сутки. На фоне приема препарата отмечал боли в животе. По результатам проведенного обследования на фоне приема Минирина 0,3 мг/сут суточный диурез - 3 литра, относительная плотность мочи - 1003-1008 г/л. С мая 2010 г. переведен на интраназальное введение десмопрессина. Доза Пресайнекса составила 10 мкг 2 раза в сутки. На фоне приема препарата боли в животе не беспокоят. При контрольном анализе мочи по Зимницкому диурез - 2200 мл/сут, относительная плотность мочи в отдельных порциях составила 1012-1015 г/л. Дальнейшая титрация дозы не проводилась.
Больной Г. 56 лет. Первые признаки заболевания в виде жажды, полидипсии и полиурии до 5 литров в сутки наблюдались с 4-5-летнего возраста. При обследовании в 6-летнем возрасте выявлен несахарный диабет. У отца больного также наблюдались полиурия и полидипсия, но он никогда не обследовался и не лечился. В дальнейшем при обследовании у него также был выявлен несахарный диабет и назначено лечение хлорпропамидом 0,5 г в сутки. У дочери больного Г. с раннего возраста отмечены жажда и полиурия, после обследования у нее диагностировали несахарный диабет. Лечение десмопрессином (Адиуретин) привело к нормализации диуреза и относительной плотности мочи. В настоящее время пациент Г. переведен на препарат Пресайнекс 10 мкг 2 раза в сутки с ранее принимавшегося Минирина 0,2 мг 2 раза в сутки. Больной переведен на интраназальный десмопрессин в связи с неудобствами при приеме Минирина. Это было обусловлено 30-40-минутными интервалами между приемом препарата и приемом пищи, а также 2-часовыми интервалами между приемом пищи и приемом препарата, что затрудняло работу пациента, связанную с частыми командировками. На фоне приема препарата Пресайнекс 20 мкг/сут диурез - 2300 мл, относительная плотность мочи - 1006-1014 г/л.
Заключение
В настоящее время для эффективного лечения пациентов с ЦНД используются препараты десмопрессина. Хороший клинический эффект, обеспечивающий длительную компенсацию заболевания, показан при назначении интраназальной формы препарата (Пресайнекс).
Литература
Физиология АДГ
АДГ (антидиуретический гормон), или аргинин-вазопрессин (АВП), представляет собой нонапептид с молекулярной массой 1100, состоящий из шести аминокислот, замкнутых в кольцо, к которому в виде боковой цепи присоединены еще три аминокислоты.
Основное количество АДГ синтезируется в клеточных телах супраоптических и паравентрикулярных ядер гипоталамуса, аксоны которых представляют собой немиелинизи-рованные волокна, проходящие через ножку гипофиза и заканчивающиеся в задней его доле. Образование АДГ начинается с синтеза препрогормона, который превращается в прогормон. Последний в свою очередь превращается в АДГ, который связывается с белком-носителем, называемым нейрофизином. Вместе с нейрофизином АДГ в составе нейросекреторных гранул по аксонам мигрирует вниз к терминальным расширениям аксонов задней доли гипофиза (нейрогипофиза). В нервных окончаниях крупноклеточных нейронов нейрогипофиза, а также в мелкоклеточных нейронах в срединном возвышении он хранится в секреторных гранулах, откуда путем экзоцитоза в комплексе с нейрофизином выделяется в системный кровоток и гипо-таламо-гипофизарную портальную систему.
Важнейшая функция АДГ - антидиуретическре действие. Основной мишенью АДГ являются клетки дистальных канальцев и собирательных трубочек почек, на базолатераль-ной мембране клеток которых расположены рецепторы АДГ типа V2- Действуя на эти рецепторы, АДГ активизирует аденилатциклазу в результате чего образующийся цАМФ стимулирует встраивание водных каналов в апикальную мембрану и эпителий становится проницаемым для воды, что обеспечивает ее пассивную реабсорбцию в гипертоническое мозговое вещество почек. Именно благодаря этому поддерживается постоянство осмоляльности и объема жидких сред организма. В отсутствие АДГ число водных каналов невелико и эпителий практически непроницаем для воды, поэтому из организма выводится большое количество гипотонической мочи. В высоких концентрациях АДГ действует на Vj-рецепторы, вызывая сужение сосудов.
В физиологических условиях главным фактором, регулирующим секрецию АДГ и жажду, является ОП. Когда ОП становится ниже порогового уровня - около 285 мосм/кг (ги-поосмоляльность), секреция АДГ тормозится. Это приводит к выведению большого объема максимально разведенной мочи. Повышенное выведение воды предотвращает дальнейшее снижение ОП, даже при значительном потреблении воды. Осморецепторы гипоталамуса весьма чувствительны к колебаниям ОП - ее сдвиг всего на 1 % приводит к заметным изменениям секреции АДГ. При повышении ОП секреция АДГ усиливается: когда ОП достигает 295 мосм/кг, концентрация АДГ становится достаточной для обеспечения максимального антидиуретического эффекта (объем мочи 2 л/сут; ОМ более 800 мосм/кг). Одновременно активизируется и механизм утоления жажды, что приводит к увеличению потребления воды и препятствует дегидратации организма. Таким образом, наиболее важным физиологическим сигналом к изменению синтеза и секреции АДГ служит изменение ОП, возрастание которой приводит к усиленному выделению АДГ из нейрогипофиза.
Другой важный механизм регуляции секреции АДГ связан с изменениями объема циркулирующей крови (ОЦК) - регуляция объемом жидкости. Секреция АДГ зависит от ОЦК и регулируется барорецепторами легочных артерий (барорецепторами системы низкого давления). Рефлексы с барорецепторов легочной артерии тормозят секрецию АДГ. Гиперволемия стимулирует эти рецепторы и вызывает снижение секреции АДГ. Наоборот, гиповолемия усиливает секрецию АДГ. Барорецепторная система регуляции менее чувствительна, чем осморецепторная: для стимуляции секреции АДГ необходимо снижение объема крови в сосудах малого круга на 5-10%. Однако дальнейшее падение ОЦК приводит к активации барорецепторов аорты и сонных артерий (барорецепторов высокого давления), к увеличению секреции АДГ и значимому вазопрессорному эффекту.
В физиологических условиях между секрецией АДГ и жаждой существует тесная связь, причем и та, и другая регулируются небольшими подъемами и снижениями ОП. Чувство жажды возникает обычно при возрастании ОП выше 292 мосмоль/кг. Порог осмоляльности для утоления жажды обычно выше, чем для секреции АДГ. Гиповолемия запускает механизм утоления жажды даже при нормальной ОП. Кроме того, гиповолемия стимулирует ренин-ангиотензи-новую систему, которая в свою очередь стимулирует секрецию АДГ. Интеграция механизмов регуляции утоления жажды и секреции АДГ обеспечивает поддержание осмоляльности плазмы в узком диапазоне (285+5 мосм/кг). При нарушении секреции АДГ потеря воды обусловливает гипонат-риемию, которая усиливает жажду и потребление жидкости в степени, достаточной для восстановления и сохранения ОП. С другой стороны, утрата чувства жажды (адипсия) сопровождается некорригируемыми потерями жидкости и гипернатриемией, несмотря на возрастание секреции АДГ и экскрецию максимально концентрированной мочи.
В норме вазопрессин выделяется постоянно, поддерживая осмотическое давление плазмы на уровне 285-287 ммоль/кг. Падение осмотического давления плазмы ниже 280 ммоль/кг ингибирует секрецию вазопрессина, тогда как подъем выше 288 ммоль/кг стимулирует синтез и высвобождение гормона. Гипоталамические осморецепторы улавливают минимальные изменения осмотического давления плазмы и объема внутриклеточной жидкости и передают эту информацию в супраоптическое и паравентрику-лярное ядра гипоталамуса, секретирующие вазопрессин.
Таким образом, для поддерживания водного гомеостаза организма требуется наличие трех механизмов: осморегу-лируемая секреция АДГ, адекватная осморегуляция жажды и объема жидкости, нормальная чувствительность почек к АДГ. Нарушение одного из этих трех механизмов может приводить к развитию несахарного диабета.
Читайте также:
