Синдром Лера-Леона Киндберга (Lohr-Leon Kindberg) - синонимы, авторы, клиника
Обновлено: 17.05.2024
Лефгрена с. — массивные гилюсные лимфатические узлы с кожными проявлениями, двустороннее увеличение (симметричное) гилюсных лимфатических узлов, которое вначале протекает без каких-либо симптомов, туберкулиновые кожные пробы отрицательные или слабоположительные, узловатая эритема, нередко лихорадка и мигрирующая суставная боль. Костных изменений не наблюдается. Гинекотропизм. Обычно наблюдается при саркоидозе (Синдром Besnier-Boeck-Schaumann).
Синдром Lohr-(Leon) Kindberg
Lohr Hans, немецкий врач; Kindberg Michel Leon (1883—1945), французский врач.
Лера-(Леона) Киндберга с. — своеобразное течение легочного инфильтрата с эозинофилией; внезапное и острое начало болезни; септическая температура, которая держится неделями; нередко озноб с потливостью; обычно выраженные катаральные явления; в крови — эозинофилия и лейкоцитоз. Рентгенологически — легочные инфильтраты и плевральный выпот. Отличается от Синдрома Леффлера (Loffler) (I) более выраженными клиническими проявлениями и более длительным течением.
Синдром van Lohuizen, phlebectasia congenita generalisata, cutis marmorisata teleangiectatica congenita
van Lohuizen Cato H. J., голландский врач.
ван Лохейзена с. — наследственная сосудистая дисплазия с прогерией: клиническая симптоматика полностью выражена уже при рождении — тонкая («как бумага») кожа с резко выраженным сосудистым рисунком, образованным расширенными, извитыми и увеличенными численно венами. Одновременно признаки прогерии: отсутствие нормального подкожного жирового слоя, гидроцефалоидный череп, расширенные вены черепа, пучеглазие, микрогения, голубые склеры, старческие черты лица, диастаз прямых мышц живота, размягчение (нерахитическое) костей черепа, преимущественно теменных и височных, в крови — гиперкальциемия. Симптомы не прогрессируют, общее развитие протекает нормально.
Синдром Lorain, infantilismus hypophysarius, panhypopituitarismus praepubertaticus, Синдром Lorain-Levi, ateliosis
Lorain Paul Joseph (1827—1875), французский терапевт.
Лорена с. — деструктивные процессы в гипофизе с вторичными расстройствами физического и умственного развития у детей: пропорциональный, гипофизарный малый (или карликовый) рост, гипогенитализм, инфантилизм, гипотиреоз, надпочечниковая недостаточность (адинамия, гипотензия), акромикрия, акроцианоз, геродермия, старческое выражение лица. Расстройства трофики жировой ткани (дис- или атрофия).
Хроническая эозинофильная пневмония: причины, симптомы, диагностика, лечение
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Хроническая легочная эозинофилия (длительная легочная эозинофилия, синдром Лера-Киндберга) - вариант простой легочной эозинофилии с существованием и рецидивированием эозинофильных инфильтратов в легких более 4 недель. Хроническая эозинофильная пневмония характеризуется хроническим патологическим накоплением эозинофилов в легком.
Распространенность и частота встречаемости хронической эозинофильной пневмонии (ХЭП) неизвестны. Хроническая эозинофильная пневмония, как считается, является аллергическим диатезом. Большинство пациентов - некурящие.
Чем вызывается хроническая эозинофильная пневмония?
Причины этой формы легочных эозинофилий та же, что синдрома Леффлера, однако, кроме того, причиной заболевания могут быть опухоли (рак желудка, щитовидной железы, легких), гемобластозы, системные васкулиты и системные заболевания соединительной ткани.
Основные патогенетические факторы те же, что при простой легочной эозинофилий.
Симптомы хронической эозинофильной пневмонии
Хроническая эозинофильная пневмония часто развивается молниеносно: появляются кашель, повышение температуры тела, прогрессирующая одышка, снижение массы тела, хрипы и ночная потливость. Бронхиальная астма сопутствует или предшествует заболеванию более чем в 50 % случаев.
Где болит?
Что беспокоит?
Диагностика хронической эозинофильной пневмонии
Диагноз требует исключения инфекционных причин и основан на анализе клинических проявлений, результатах анализов крови и рентгенографии органов грудной клетки. Часто обнаруживаются эозинофилия периферической крови, очень высокая СОЭ, железодефицитная анемия и тромбоцитоз. На рентгенограмме органов грудной клетки выявляются двусторонние инфильтраты в боковых или субплевральных зонах (приблизительно в 60 % случаев), обычно в средних и верхних отделах легких, описываемые как «негатив» отека легких; данная картина является патогномоничной (хотя встречается у 40 %) является достоверным признаком хронической эозинофильной пневмонии; исследования бронхоальвеолярного лаважа в динамике могут помочь контролировать течение заболевания. При гистологическом исследовании биоптата легкого выявляются интерстициальные и альвеолярные эозинофилы и гистиоциты, включая многоядерные гигантские клетки и облитерирующий бронхиолит с организующейся пневмонией. Фиброз минимален.
Что нужно обследовать?
Как обследовать?
Какие анализы необходимы?
Лечение хронической эозинофильной пневмонии
При хронической эозинофильной пневмонии высока эффективность внутривенных или пероральных глюкокортикоидов; отсутствие ответа свидетельствует в пользу другого диагноза. Начальное лечение хронической эозинофильной пневмонии состоит в назначении преднизолона (в дозе от 40 до 60 мг, 1 раз в сутки). Клиническое выздоровление часто отмечается поразительно быстро, возможно в течение 48 ч. Полное разрешение клинических проявлений и рентгенологических изменений происходит в течение 14 дней у большинства пациентов и 1 мес почти у всех. Поэтому оценка динамики данных показателей является надежным и эффективным средством контроля эффективности терапии. Хотя КТ более чувствительна в выявлении рентгенологических изменений, преимущества ее в оценке динамики процесса не показаны. Количество эозинофилов в периферической крови, СОЭ и концентрации IgE могут также использоваться для контроля клинического течения заболевания на фоне проводимого лечения. Однако не у всех пациентов отмечаются патологические изменения результатов лабораторных исследований.
Клинический или рентгенологический рецидив отмечается в 50-80 % случаев после прекращения терапии или, реже, при снижении дозы глюкокортикоидов. Рецидив может развиваться через месяцы и годы после первичного эпизода заболевания. Таким образом, лечение хронической эозинофильной пневмонии глюкокортикоидами иногда продолжается неопределенно долго. Ингаляционные глюкокортикоиды (например, флутиказон или беклометазон в дозе от 500 до 750 мкг 2 раза в сутки), вероятно, эффективны, особенно при снижении поддерживающей дозы перорального глюкокортикоида.
Хроническая эозинофильная пневмония иногда приводит к физиологически значимому и необратимому фиброзу легких, хотя летальные исходы чрезвычайно редки. Рецидив, вероятно, не указывает на отсутствие эффекта терапии, худший прогноз или более тяжелое течение. Пациенты продолжают также отвечать на глюкокортикоиды, как и при предшествующих эпизодах. Фиксированное ограничение воздушного потока может отмечаться у некоторых выздоровевших пациентов, но эти нарушения имеют обычно ограниченное клиническое значение.
Синдром Лера-Леона Киндберга (Lohr-Leon Kindberg) - синонимы, авторы, клиника

Саркоидоз — особенности болезни

Пневмофиброз — осложнения и последствия

Пневмомикоз — что это такое и методы лечения

Кровь при кашле при бронхите

Вильпрафен при бронхите

Киста легкого — симптомы, причины и лечение
Выбрать оборудование













@ RESPIMED, г. Санкт-Петербург, Все права защищены Медицинская лицензия ФС-99-04-007463 от 20.10.20г. ООО "Медика Трейд"
Информация на сайте предоставляется с целью ознакомления, не занимайтесь самолечением, обращайтесь за консультацией к врачам.
Несанкционированное использование материалов, размещенных на сайте, запрещено Законом об авторском праве. Если вы нашли на сайте ошибку, обращайтесь с помощью обратной связи к редакции сайта для исправления неточностей.
Фиброма легких, что это такое?
ЛЕФФЛЕРА СИНДРОМ
ЛЕФФЛЕРА СИНДРОМ (W. Loffler, швейцарский врач, род. в 1887 г.; син.: летучие легочные инфильтраты, эозинофильная пневмония, эозинофильные инфильтраты легкого) — сочетание транзиторных инфильтратов легких, определяемых при рентгенологическом исследовании, с высокой эозинофилией крови. Подобные инфильтраты обнаруживаются и в других органах.
Описан впервые Леффлером в 1932 г. Встречается во всех странах относительно редко, в тропических странах чаще.
Содержание
Этиология
Вызывается различными патогенными факторами. Основной этиол, фактор — инвазии гельминтами (аскаридами, анкилостомами, трихинами, плоскими червями Taenia saginata, печеночной двуусткой, шистосомами, стронгилоидами, а также кошачьей двуусткой), личинки к-рых мигрируют через легкие. Известны случаи заражения людей, особенно детей, личинками Toxocara — аскаридоподобного паразита собак и кошек. Личинки Toxocara мигрируют через легкие, но, в отличие от личинок аскарид, образуют цисты в легких, печени и других органах, не достигая зрелости. Процесс миграции этих личинок может сопровождаться Л. с. Вторая группа этиол. факторов Л. с.— хим. агенты и лекарства. Известны случаи Л. с. при проф. контакте с никелем и цинком и от многих лекарств как при проф. контакте, так и при леч. применении (пенициллин, ацетилсалициловая к-та, сульфаниламиды, нитрофураны, ПАСК, рентгеноконтрастные вещества и др.). Описаны случаи Л. с. у женщин, получавших по поводу рака молочной железы гормональные препараты (тестостерон-пропионат и синэстрол) в сочетании с лучевой терапией. Третья группа этиол. факторов — различные экзогенные аллергены (пыльца растений, споры грибков, табак и др.), вызывающие атопические заболевания респираторного аппарата (см. Атопия). Транзиторные эозинофильные легочные инфильтраты описаны в числе других проявлений сывороточной болезни, а также узелкового периартериита, протекающего с высокой эозинофилией; имеются указания на их связь с туберкулиновой аллергией и амебиазом. Нередко этиология Л. с. остается неясной.
Патогенез
В основе патогенеза Л. с. лежит формирование аллергического эозинофильного альвеолита. Наиболее вероятен немедленный тип аллергической реакции (см. Аллергия), к-рый подтверждается положительными кожными тестами, а также нек-рыми особенностями клин, течения: «летучий» характер инфильтратов, их полное обратное развитие без формирования очагов склероза. В отдельных случаях можно обнаружить повышенное содержание IgE в сыворотке крови у детей, страдающих аскаридозом, что характерно для заболеваний, обусловленных аллергическими реакциями немедленного типа. Интенсивная инфильтрация ткани легких эозинофилами и выраженная эозинофилия крови дают основание предполагать, что при Л. с. особая роль в формировании очагов аллергического воспаления принадлежит эозинофильному хемотаксическому фактору анафилаксии (см. Медиаторы аллергических реакций). Образование высоких титров преципитирующих антител к антигенам в ряде случаев Л. с. объясняется, по-видимому, участием аллергических реакций, развивающихся по типу феномена Артюса (см. Артюса феномен). В эксперименте получена эозинофильная пневмония, похожая на Л. с. у кроликов, сенсибилизированных лошадиной сывороткой после разрешающей интратрахеальной инъекции этой сыворотки.
Клиническая картина
Наиболее характерными в клин, картине Л. с. являются инфильтраты в легких, к-рые выявляются при рентгенол, исследовании, и эозинофилия крови (от 7 до 70%) при умеренно выраженном лейкоцитозе. Жалобы и симптомы (небольшой сухой кашель, легкое недомогание, слабость, потливость, субфебрильная температура) могут отсутствовать или быть очень скудными. Перкуторно при обширных инфильтратах определяется укорочение легочного звука. Аускультативно изредка выслушиваются в небольшом количестве влажные мелко-пузырчатые хрипы. Чаще поражается верхняя доля правого легкого. Описано сочетание эозинофильных легочных инфильтратов с сухим плевритом (см.), при этом могут быть боли при дыхании в соответствующей половине грудной клетки и прослушиваться шум трения плевры. Симптомы продромального периода могут протекать в виде катарального ринофарингита. Иногда температура достигает 38—39 °. В мокроте, если она отделяется, определяются преимущественно эозинофилы.
Для заболевания характерно легкое течение. Спонтанное выздоровление наступает через несколько дней или 2—4 нед. Инфильтраты держатся более продолжительно, вероятно в тех случаях, когда в патогенезе, помимо анафилактических реакций, участвуют реакции по типу феномена Артюса. Осложнений, как правило, не бывает.
При локализации эозинофильных инфильтратов в других органах обычно наблюдаются легкие быстро-преходящие симптомы поражения соответствующих органов и систем— гастрит, панкреатит, аппендицит, менингоэнцефалит и др.— в сочетании с эозинофилией крови.
Диагноз
Диагноз устанавливают на основании рентгенол, данных с их характерной быстрой динамикой и наличия выраженной эозинофилии крови. Часто Л. с. выявляется случайно при профилактическом рентгенол. обследовании.
Этиол, диагноз более труден; применяют кожное тестирование аллергенами, приготовленными из гельминтов, пыльцы растений, спор грибков (см. Кожные пробы); серол, тесты — реакцию преципитации (см.) в различных модификациях и реакцию связывания комплемента (см.), а также клеточные тесты, такие как реакция дегрануляции базофилов по Шелли (см. Базофильный тест) и реакция дегрануляции тучных клеток (см.) с соответствующими аллергенами. Профессиональный «никелевый» Л. с. обычно сочетается с аллергическим контактным дерматитом, компрессный (аппликационный) тест с никелем при этом положительный. В случаях, вызванных кишечными паразитами, можно, но не всегда, обнаружить яйца паразитов в кале, т. е. при первичной инвазии миграция личинок через легкие происходит до достижения паразитами зрелости и выделения яиц. Однако этот метод можно применить в расчете на возможность инвазии, предшествующей той, к-рая привела к формированию Л. с. При инвазии личинками Toxocara паразиты не достигают зрелости в организме человека, поэтому яйца в кале не обнаруживаются.

Рис. 1. Рентгенограмма грудной клетки больного с синдромом Леффлера: одиночный инфильтрат в правом легком (указан стрелкой).
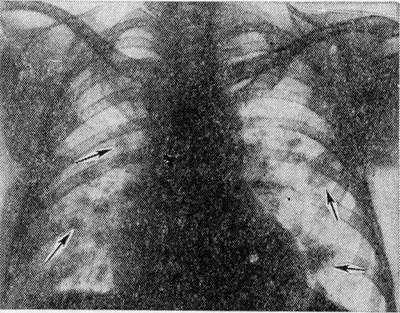
Рис. 2. Рентгенограмма грудной клетки больного с синдромом Леффлера: множественные двусторонние инфильтраты в легких (указаны стрелками).
Наиболее типичным рентгенол, проявлением Л. с. является тень одиночного инфильтрата, расположенного в любом отделе легкого, небольшой или средней интенсивности и, как правило, ее размеры 3—4 см в диаметре. Форма тени обычно неправильная, очертания нечеткие (рис. 1). Окружающий легочный рисунок усилен в связи с местной гиперемией. В большинстве случаев тень соответствующего корня легкого слегка расширена, структурна. При многопроекционном исследовании удается установить, что инфильтрат располагается чаще в плащевидном слое легкого. В связи с этим нередко можно выявить утолщение плевры, расположенной в непосредственной близости к инфильтрату. Характерным для динамики инфильтрата при Л. с. является его исчезновение через 1 — 3 дня после выявления; на месте бывшего инфильтрата в течение нескольких дней остается постепенно уменьшающееся усиление легочного рисунка. Такая быстрая динамика дала основание назвать эти инфильтраты летучими. Реже при Л. с. встречаются инфильтраты, принимающие форму анатомических структур — сегментов, долей, и множественные инфильтраты, к-рые иногда могут быть двусторонними (рис. 2). Быстрое исчезновение является типичным для всех видов инфильтратов при Л. с. В относительно редких случаях инфильтраты могут рецидивировать. В отдельных случаях при наличии крупных инфильтратов можно обнаружить небольшой транссудат в плевральной полости, к-рый рассасывается в течение нескольких дней.
Необходимо отличать эозинофильные инфильтраты в легких при Л. с. от эозинофильных инфильтратов как следствия эмболии легочных сосудов, обусловленной лимфографией. Наличие инфильтратов требует в ряде случаев дифференциальной диагностики с бактериальными и вирусными пневмониями (см.), туберкулезом, в т. ч. милиарным (см. Туберкулез органов дыхания).
Дифференцировать Л. с. необходимо с синдромом Вайнгартена (см. Вайнгартена синдром) и синдромом Лера—Киндберга, для к-рого характерно острое начало болезни, септическая температура (держится неделями), озноб, потливость, эозинофилия и лейкоцитоз, рентгенологически — легочные инфильтраты и плевральный выпот. Скудность и невыраженность клин, симптомов, наличие эозинофилии должны навести на мысль о Л. с. В дальнейшем транзиторный характер инфильтратов в легких решает диагноз в пользу Л. с.
Лечение
Если не наступает спонтанного выздоровления, проводят лечение кортикостероидными гормонами. Курс лечения начинают с дозы 15—20 мг в день (в пересчете на преднизолон), через день дозу снижают на 5 мг; курс продолжается от 6 до 8 дней. Этого курса бывает достаточно для полного выздоровления.
При синдроме Леффлера, вызванном глистной инвазией, проводится соответствующее лечение.
Прогноз благоприятный, выздоровление может наступить без всякого лечения.
Профилактика сводится к гиг. мерам предотвращения глистных инвазий. Больные атопическими заболеваниями респираторного аппарата должны избегать контакта с соответствующими аллергенами. При профессиональном характере сенсибилизации необходимо исключить контакт с «виновным» аллергеном.
К мерам профилактики Л. с. относится специфическая гипосенсибилизация (см.) больных атопическими заболеваниями.
Следует помнить также о различных мерах профилактики лекарственной аллергии (см.).
Библиогр.: Курашова М. В. и Белова Е. В. Синдром Леффлера, Клин, мед., т. 53, JSii 3, с. 13, 1975; Л и нденб р а т e н Л. Д. и H а у м о в Л. Б. Рентгенологические синдромы и диагностика болезней легких, М., 1972: Я с и н о в- с к и й М. А., Г а н д ж а И. М. и Лернер П.П. Поражения легких при ревматизме и некоторых аллергических заболеваниях, Киев, 1969, библиогр.; Loffler W. Zur Differential-Diagnose der Lungenin-filtrierungen, Uber fliichtige Succedanin-filtrate (mit Eosinophilie), Beitr. Klin. Tuberk., Bd 79, S. 368, 1932; Teschendorf W., A n a с k e r H. u. T h u r n P. Rontgenologische Differentia! diagnostik, Bd 1, T. 1, Stuttgart, 1975; U d w a d i a F. E. Pulmonary eosinophilia, Progr. Respirat. Res., y. 7, p. 275, 1975.
Синдром Жильбера - симптомы и лечение
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.

К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .

Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.

Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).

У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.

В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.
Читайте также:
