Регуляция сократительной деятельности желудка. Сокращение желудка.
Обновлено: 12.05.2024
Интенсивное превращение питательных веществ принятого корма осуществляется в желудке. Пищеварение в желудке связано с секреторной деятельностью желудочных желез, двигательной активностью мышц желудка и деятельностью его кардиального и пилорического сфинктеров.
Секреторная деятельность желудочных желез. В слизистой оболочке желудка имеется большое количество трубчатых желез, состоящих из трех видов клеток: главных, обкладочных и добавочных, которые образуют три секреторные зоны: кардиальную с железами из добавочных клеток; фундальную с железами из обкладочных, главных и добавочных клеток; пилорическую с железами из главных и добавочных клеток. Главные клетки продуцируют ферменты, об- кладочные — соляную кислоту, добавочные — слизь. Желудочные железы основной фундальной зоны вырабатывают кислый желудочный сок (НС1 — 0,3—0,6%, pH 1,0—4,0). Желудочный сок содержит воду, свободную и связанную соляную кислоту (связана с белками), неорганические и органические вещества — ферменты, белки, аминокислоты и др., слизь.
Основные ферменты желудочного сока — пепсины, реннин, желудочная липаза. Пепсины действуют на белки и расщепляют их до пептидов, альбумоз и пептонов, частично аминокислот (последних образуется мало). Действие пепсинов осуществляется только в кислой среде (они вырабатываются в форме пепсиногенов — неактивной форме и активируются соляной кислотой до пепсинов). Соляная кислота также вызывает набухание и денатурацию белка, поэтому он легче подвергается действию ферментов. Реннин превращает белок молока — казеиноген в казеин, обеспечивает створаживание молока (его много в желудочном соке новорожденных животных). Желудочная липаза превращает жиры молока (только эмульгированные жиры) до глицерина и жирных кислот.
Возбудителями желудочных желез являются белки, экстрактивные вещества, эмульгированные жиры (молока).
Корм, попадая в желудок, пропитывается желудочным соком постепенно. Поэтому расщепление белков начинается с поверхности пищевой массы, а в ее глубине временно под действием гликолити- ческих ферментов слюны также происходит расщепление крахмала, мальтозы. Когда вся пищевая масса пропитается кислым желудочным соком, действие ферментов слюны прекращается. Интенсивная ферментация питательных веществ корма осуществляется первые три часа (60%).
Сократительная деятельность желудка. Она обеспечивает депонирование в желудке принятого корма, его пропитывание желудочным соком, передвижение содержимого по желудку и изгнание порциями желудочного содержимого в двенадцатиперстную кишку. Эти процессы обеспечиваются благодаря особым свойствам гладких мышц желудка. Желудок благодаря своим мышцам осуществляет разнообразные сокращения: тонические, перистальтические и систолические. Поступление пищевых масс в желудок сопровождается его растяжением и слабыми перистальтическими сокращениями. Через некоторое время перистальтика желудка усиливается — начинается у кардиального сфинктера и заканчивается у пилорического, обеспечивая перемещение поверхностного слоя содержимого. Одновременно происходят тонические сокращения, обеспечивающие пропитывание содержимого желудочным соком. Систолические сокращения, напоминающие сокращения желудочков сердца, осуществляются в пилорической части желудка и обеспечивают изгнание содержимого из пилорической части желудка в кишечник порциями. Систолическое сокращение желудка сопровождается рефлекторным раскрытием пилорического сфинктера. Возбудителями этого рефлекса являются: жидкое содержимое, его кислая реакция и осмотическое давление, близкое по величине к осмотическому давлению крови. Кислое содержимое, поступая в двенадцатиперстную кишку, раздражает ее механорецепторы и хеморецепторы и рефлек- торно обеспечивает смыкание пилорического сфинктера. Содержимое из желудка в кишечник поступает порциями.
Желудочное пищеварение, возбуждение желудочных желез и выделение желудочного сока начинается через 10 мин после начала приема корма. Максимум возбуждения и выделения сока происходит к концу первого часа. Высокий уровень секреции удерживается 4—6 ч (у сельскохозяйственных животных — 9). Корм задерживается в желудке 6—9 ч, но уже с первых минут пищеварения пищевая масса (в первую очередь жидкости) из желудка начинает поступать в кишечник. В первые 3—4 ч в кишечник из желудка переходит 60% содержимого желудка.
Особенности желудочного пищеварения у лошади. Желудок у лошади относительно небольшой — 8—16 л, 2/5 его объема не имеет желез (так называемый слепой мешок). Принимаемый корм располагается послойно. Первые порции корма укладываются по периферии, последующие втискиваются в середину и увеличивают объем желудка. Слоистое расположение корма имеет место и в пилорической части желудка. Потребляемая животным вода по малой кривизне быстро проходит в пилорическую часть желудка и в кишечник. Кардиальный и пилорический сфинктеры располагаются на близком расстоянии друг от друга.
При обычном режиме кормления корм в желудке лошади находится постоянно, что вызывает непрерывную секрецию желудочного сока, причем после приема корма она усиливается.
Сократительная деятельность желудка слабая. Корм не перемешивается по несколько часов. Желудочный сок, следовательно, не может быстро пропитать содержимое желудка (пропитывает слои содержимого постепенно — в течение 1—2 ч), что способствует длительному развитию гликололитических процессов (за счет ферментов корма, микроорганизмов и слюны).
В области слепого мешка обитает микрофлора — лактобациллы, стрептококки и дрожжевые грибки. Они обеспечивают бактериальное молочнокислое брожение одновременно с ферментацией белка под влиянием ферментов желудочного сока в фундальной части желудка.
В фундальной и пилорической частях желудка постепенно нарастает ферментация белков под действием пепсина желудочного сока. Желудочный сок содержит пепсины и липазу. Конечными продуктами бактериального брожения являются молочная, уксусная, масляная кислоты и газы — Н2 и С02. В желудке лошади клетчатка не расщепляется — там нет целлюлозолитической микрофлоры.
С усилением сократительной деятельности желудка в первые часы после кормления желудочный сок постепенно проникает в содержимое слепого мешка, фундальной и пилорической частей желудка, реакция содержимого становится кислой. В этих условиях действие гликолитических ферментов бактерий прекращается. В кислой среде повышается активность пепсина. Содержание соляной кислоты в желудке лошади — 0,1—0,25%.
Механизм возбуждения и регуляции секреторной и сократительной деятельности у лошади такой же, как у других животных. Время интенсивного желудочного пищеварения — 6 ч.
Особенности желудочного пищеварения у свиньи. Желудок у свиней однокамерный, вмещает 6,5—9 л, в области малой кривизны имеется безжелезистая зона, вдоль большой кривизны располагается большая кардиальная зона. В начальной части кардиальной зоны имеется выступ — дивертикул. Только фундальная (30%) и пилорическая (20%) зоны имеют железы. Железы фундальной зоны состоят из обкладочных и главных клеток, продуцируют кислый секрет, содержащий соляную кислоту и ферменты пепсиноген, реннин и липазу. В пилорической зоне железы состоят из главных и добавочных клеток, продуцируют щелочной секрет.
Принимаемый корм располагается послойно и не перемешивается по несколько часов. Сократительная деятельность желудка после приема корма нарастает постепенно.
Желудочный сок в небольших количествах выделяется у свиней постоянно, даже при отсутствии корма в желудке. Кормление усиливает отделение сока. За 1 сут при трехразовом кормлении выделяется более 6—9 л желудочного сока.
Начальная фаза желудочного пищеварения — фаза смешанного пищеварения, переваривания белков, липидов и углеводов. По мере пропитывания содержимого желудочным соком эта фаза сменяется на фазу истинного желудочного пищеварения — переваривания белков до альбумоз и пептонов.
До 20% легкорастворимых углеводов расщепляется в желудке (в дивертикуле и верхней части кардиальной зоны) под действием амилазы и глюкозидазы слюны и бактериального брожения до мальтозы, глюкозы, молочной, масляной и уксусной кислот. В фун- дальной и пилорической зонах происходит расщепление белков и жиров. У свиней происходит периодический заброс кишечного содержимого в желудок — регургитация.
Эвакуация содержимого из желудка в кишечник наиболее интенсивно происходит в первые 3 ч. Время желудочного пищеварения — 9 ч.
Особенности желудочного пищеварения у жвачных. Желудок у жвачных сложный многокамерный, состоит из рубца, сетки, книжки и сычуга — истинного желудка (рис. 26.2). Рубец, сетка, книжка — преджелудки, они не имеют желез, их слизистая покрыта многослойным ороговевающим эпителием, образует выступы — сосочки в рубце, складки (ячейки) в сетке, листочки в книжке. Объем рубца у коровы в среднем — около и более 140 л, у овец — 16 л, сетки соответственно — 8 и 0,8 л, книжки — 12 и 1 л, сычуга — 15 и 1,5 л.
В преджелудках превращаются белки, жиры и углеводы, а также в больших количествах клетчатка. Превращения происходят под действием внутриклеточных и внеклеточных ферментов микроорганизмов — бактерий, простейших и грибов, обитающих в преджелудках. Микроорганизмы продуцируют три группы ферментов: преобладают целюлозолитические, продуцирующие целлюлазу, целлобиазу (расщепляют клетчатку): протеолитические, продуцирующие протеиназы (расщепляют белки); липолитические, продуцирующие липазы (расщепляют жиры). Также много и бактерий, расщепляющих небелковые азотистые продукты, крахмал, сбражива-
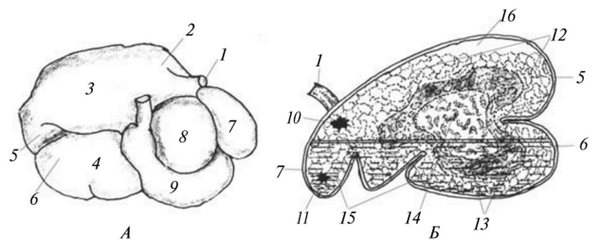
Рис. 26.2. Желудок жвачного животного (крупного рогатого скота):
А — отделы сложного желудка (вид справа): 7 — пищевод; 2 — преддверие рубца; 3 — дорсальный мешок рубца; 4 — вентральный мешок рубца; 5 — каудо-дорсальный и б — каудо-вентральный слепые выступы; 7 — сетка; 8 — книжка; 9 — сычуг; б — расположение плотных и жидких кормовых масс в рубце: 10 — кардиальное отверстие; 11 — сетко-книжное отверстие; 12 — легкий, недавно проглоченный влажный корм; 13 — тяжелые частицы корма, суспенизированные в воде;
14 — плотная масса; 75 — жидкая масса; 16 — газы
ющих глюкозу, дезаминирующих аминокислоты. Простейших содержится меньше, они также обладают высокой протеолитической, гликолитической и липолитической способностью.
Под влиянием протеиназ и пептидаз белки расщепляются сначала до пептидов, затем до аминокислот. Большая часть аминокислот дезаминируется с образованием аммиака. Аммиак используется микроорганизмами для синтеза собственных белков в связи с размножением. Аммиак частично связывается глутаминовой кислотой и транспортируется кровью в печень, где в орнитиновом цикле превращается в мочевину, последняя из крови снова поступает через стенку преджелудков и со слюной в рубец, где под действием фермента бактерий уреазы расщепляется, превращается в аммиак, который используется микроорганизмами.
Крахмал, дисахариды гликолитическими ферментами микроорганизмов расщепляются до моносахаридов.
Клетчатка (в основном целлюлоза) под действием фермента цел- люлазы целюлозолитических бактерий вначале расщепляется до целлобиозы, затем под действием фермента целлобиазы — до глюкозы. Глюкоза подвергается сбраживнию до низкомолекулярных жирных кислот — уксусной, пропионовой, масляной (летучие жирные кислоты). Летучие жирные кислоты (ЛЖК) всасываются в кровь и используются как источник энергии.
Липиды (сырой жир) подвергаются действию липолитических бактерий, расщепляются на моноглицериды, жирные кислоты, глицерин. Глицерин сбраживается с образованием ЛЖК. Жирные кислоты подвергаются гидрогенизации, превращаются в насыщенные кислоты, которые используются микроорганизмами для синтеза липидов. В бактериях определяется много фосфолипидов. Для синтеза фосфолипидов бактерии используют и ЛЖК. Поэтому в предже- лудках определяется больше жира, чем поступило с кормом.
Ферментация питательных веществ корма в преджелудках сопровождается образованием газов — С02, СН4, N2, Н2, которые создают оптимальную для микроорганизмов газовую среду. Образующиеся газы отрыгиваются.
Пищеварение в преджелудках сопровождается их сократительной деятельностью (рис. 26.3). Сократительная деятельность осуществляется циклами: сокращается сетка, за ней преддверие рубца, далее дорсальный мешок, вентральный мешок, каудодорсальный и каудовентральный выступы рубца. Через 2—3 цикла сокращается книжка. Количество циклов — 7—14 за 5 мин.
Пищеварение в преджелудках связано с жвачным процессом (жвачкой) — отрыгиванием из преджелудков порциями принятого корма, его повторным пережевыванием и проглатыванием. Жвачный процесс осуществляется периодами (жвачные периоды) — 8—16 раз в 1 сут, продолжительностью 30-50 мин. Отрыгивание порций корма осуществляется рефлекторно с рецепторов сетки и рубца через

Рис. 26.3. Последовательность сокращений преджелудков жвачных:
A, B,C,D — фазы сокращений (пунктирная линия на контурах преджелудков — состояние до сокращения); С — сетка; Пр — преддверие рубца; Дмр — дорсальный мешок рубца; Вмр — вентральный мешок рубца; Кк — канал книжки; Тк — тело книжки; Ог — отрыгивание газов систему блуждающих и чревных нервов, центр в продолговатом мозге. Рецепторы возбуждают грубые компоненты кормов. Животное делает холостой вдох, при закрытой голосовой щели в грудной полости понижается давление, расширяется пищевод, открывается его сфинктер, сокращается сетка, затем преддверие рубца и порция корма выбрасывается в пищевод, антиперистальтическими сокращениями пищевода она перемещается в ротовую полость.
Значительная часть конечных продуктов ферментации в предже- лудках всасывается.
Регуляция всех процессов осуществляется рефлекторно с рецепторов преджелудков через блуждающие и чревные нервы, нервный центр, расположенный в продолговатом мозге, и вышележащих отделов головного мозга. Через блуждающие нервы осуществляются влияния, учащающие сокращение преджелудков и увеличивающие всасывание конечных продуктов; через симпатические нервы — влияния, повышающие силу сокращения преджелудков и активность ферментов — переносчиков из преджелудков в кровь продуктов переваривания.
Рефлекторно с хеморецепторов слизистой оболочки преджелудков обусловливается непрерывная секреция слюны околоушными слюнными железами. Слюна нейтрализует кислые продукты, образующиеся при брожении. Так поддерживается близкая к нейтральной реакция содержимого преджелудков.
Регуляция сократительной деятельности желудка. Сокращение желудка.
Моторная функция желудочно-кишечного тракта. Гладкая мускулатура пищеварительного тракта. Cфинктеры жкт. Сократительная деятельность кишечника.
Процесс пищеварения во всех отделах пищеварительного тракта осуществляется при участии двигательной активности его мускулатуры. Сокращения мышц обеспечивают: прием и измельчение пищи в процессе жевания в ротовой полости, глотание и продвижение порции пищи по пищеводу, накопление ее в желудке и эвакуацию его содержимого в кишечник, сокращение и расслабление желчного пузыря, перемешивание и продвижение кишечного содержимого, движение ворсинок, переход химуса из тонкой кишки в толстую, его перемещение по толстой кишке, сокращение и расслабление сфинктеров, перистальтику выводных протоков пищеварительных желез и выведение экскрементов.
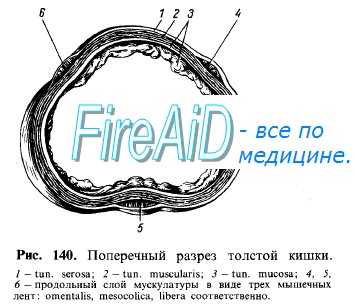
Гладкая мускулатура пищеварительного тракта состоит из гладкомы-шечных клеток (миоцитов). Они собраны в пучки и соединены друг с другом нексусами. Пучок получает нервные терминали, артериолу и выполняет роль функциональной единицы гладкой мышцы. Миоциты обладают способностью к спонтанному ритмическому возбуждению за счет периодической деполяризации их мембраны. Это возбуждение распространяется благодаря нексусам от клетки к клетке (как по синцитию). Пучки миоцитов образуют гладкомышечные слои пищеварительной трубки — циркулярный (внутренний), продольный (наружный) и подслизистый (косой).
Растяжение мышц содержимым желудочно-кишечного тракта является для них адекватным раздражителем, вызывающим деполяризацию мембран их клеток и сокращение мышечных волокон. Частота и сила сокращений миоцитов изменяются в широком диапазоне под влиянием нервных импульсов эфферентных терминалей вегетативных нервных волокон, гормонов и гастроинтестинальных регуляторных пептидов. Комплексная нервно-гуморальная регуляция миоцитов обеспечивает соответствие уровня активности мускулатуры объему и составу содержимого желудка и кишечника.
Характер сократительной деятельности мускулатуры пищеварительного тракта зависит от активности водителей ритма, расположенных в желудке и кишечнике. Они представляют собой гладкомышечные клетки, более чувствительные к биологически активным веществам и имеющие более обильную иннервацию, чем другие пучки миоцитов.
На протяжении пищеварительного тракта у человека имеется около 35 сфинктеров. Они состоят из мышечных пучков, расположенных циркулярно (в основном), спирально и продольно. Сокращение циркулярных пучков приводит к смыканию сфинктера, а сокращение спиральных и продольных пучков увеличивает его просвет, что способствует переходу содержимого пищеварительного тракта в нижележащий отдел. Сфинктеры обеспечивают движение содержимого пищеварительной трубки в каудальном направлении и временное разобщение функционально различных частей пищеварительного тракта. Основные из них — кардиальный (на входе в желудок), пилорический (на выходе из желудка), в основании баугиниевои заслонки (на входе в слепую кишку), внутренний и наружный анальный (на выходе из прямой кишки).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Влияние антагонистов допаминовых рецепторов на двигательную функцию желудочно-кишечного тракта
Изучение механизмов влияния допамина на двигательную функцию пищеварительного тракта позволили внедрить в практику один из самых эффективных классов гастроэнтерологических препаратов – селективные антагонисты D2-рецепторов, наиболее изученным и эффективны
Influence of the antagonists of dopamine receptors on the motor function of the gastrointestinal tract
The study of the mechanisms of the influence of dopamine on the motor function of the digestive tract made it possible to put into practice one of the most effective classes of gastro enterologic preparations - selective antagonists of D2-receptors, most studied and effective is domperidon.
Допамин является нейротрансмиттером из группы катехоламинов, регулирующим различные функции центральной и периферической нервных систем, включая поведение, синтез и высвобождение гормонов и нейротрансмиттеров, а также кровяное давление и внутриклеточный транспорт ионов [1]. Роль допаминергической иннервации в регуляции деятельности желудочно-кишечного тракта (ЖКТ) по сравнению с таковой в нервной системе изучена меньше. По-прежнему существуют противоречия во взглядах на источник допамина (нейрональный или ненейрональный) в ЖКТ [2–4]. Тем не менее, антидопаминергические препараты, в частности домперидон, многие годы чрезвычайно эффективно используются для коррекции таких нарушений двигательной функции верхних отделов пищеварительной системы, как функциональная диспепсия (ФД), нарушение опорожнения желудка различного генеза, тошнота и рвота. Изучение влияния допамина на различные функции мозга привели к появлению гипотезы о существовании нескольких подтипов рецепторов допамина. Ранние исследования позволили выявить два класса рецепторов: D1 и D2. Дальнейшая гетерогенность рецепторов была изучена с использованием метода клонирования, который показал существование по крайней мере пяти подтипов рецепторов допамина (D1–D5) [5, 6]. Данный обзор посвящен роли дофаминергической системы в регуляции деятельности ЖКТ и сосредоточен на D2-подтипе рецепторов допамина. В частности, обсуждаются клинические проявления блокады D2-рецепторов таким эффективным прокинетическим препаратом, как домперидон, в том числе в ЖКТ (прокинетический терапевтический эффект) и центральной нервной системе (противорвотный эффект).
Многочисленные гистохимические и иммуногистохимические исследования строения стенки кишечной трубки млекопитающих продемонстрировали наличие нескольких популяций нейронов, содержащих амины, которые могут участвовать в регуляции моторики ЖКТ. Эти группы нейронов включают в том числе и норадренергические нейроны, имеющие происхождение из экстраорганной симпатической нервной системы. Они содержат допамин, который выступает как промежуточный продукт метаболизма в процессе формирования норадреналина [3]. В то же время значительное количество допамина в организме не преобразуется в другие катехоламины, что предполагает существование периферической дофаминергической системы, независимой от симпатической норадренергической системы [7]. Ткань тела желудка морских свинок спонтанно продуцирует допамин в количестве, сопоставимом с таковым в центральных дофаминергических нейронах. Высвобождение допамина увеличивается при трансмуральной электрической стимуляции через механизм, чувствительный к тетродотоксину (блокатор нейрональных Na + -каналов), и зависит от концентрации внеклеточного Ca 2+ , что предполагает нейрональный механизм высвобождения [8]. И в организме человека, в тканях ЖКТ, селезенки и поджелудочной железы синтезируется значительное количество допамина [4]. Сопоставление количества допамина и его метаболитов, синтезирующегося во внутренних органах с объемом, удаляемым почками, указывает на то, что до 46% допамина, сформированного в организме, не метаболизируется в норадреналин. Источник этого значительного количества допамина частично представлен не-нейрональными клетками дофаминергической паракринной системы в слизистой оболочке ЖКТ [4].
Как сам допамин, так и агонисты допаминовых рецепторов могут оказывать и тормозящее, и стимулирующее действие на двигательную функцию пищеварительного тракта (рис.). Тормозящее действие состоит в расслаблении мышечного слоя стенки и угнетении перистальтики пищеварительной трубки, которые наблюдаются от пищевода до толстой кишки [2]. Известны убедительные работы, демонстрирующие способность допамина приводить к расслаблению стенки желудка в экспериментах на живых собаках [9]. Гораздо реже по сравнению с тормозящим может наблюдаться и стимулирующее действие допамина [2].
К настоящему времени изучены гены, кодирующие пять подтипов допаминергических рецепторов. Эти пять рецепторов допамина принадлежат к надсемейству G-белок-связанных рецепторов и структурно характеризуются наличием семи трансмембранных доменов, которые связывают допамин. Из этих пяти подтипов D1- и D5-рецепторы объединены в подсемейство D1-подобных рецепторов, потому что имеют до 80% гомологичных аминокислотных последовательностей в трансмембранных доменах. Аналогично рецепторы D2, D3 и D4, также демонстрирующие значительное подобие, классифицируются как члены подсемейства D2-подобных рецепторов. Эти два подсемейства отличаются тем, что активация D1-подобных рецепторов стимулирует выработку аденилатциклазы, тогда как активация D2-подобных рецепторов препятствует таковой [10]. D1-рецепторы расположены в основном на постсинаптической мембране эффекторных клеток, тогда как D2-рецепторы расположены и пост-, и пресинаптически. В последнем случае они оказывают негативное модулирующее влияние на высвобождение ацетилхолина из внутренних холинергических нервных терминалей [11].
Убедительным доказательством того, что допамин играет существенную роль в регуляции моторики ЖКТ, служит тот факт, что антагонисты рецепторов допамина активно стимулируют двигательную функцию ЖКТ начиная от пищевода и заканчивая толстой кишкой. Домперидон, селективный антагонист D2-рецепторов, в частности, существенно улучшает антродуоденальную координацию [12]. Также было установлено, что этот препарат блокирует тормозящий эффект допамина на моторику желудка [13] и усиливает сократительную активность толстой кишки у здоровых добровольцев [14].
На животных моделях стимуляция D2-допаминовых рецепторов (с помощью апоморфина или непосредственно допамина) на уровне триггерной зоны широко используется для изучения рвоты и связанных с ней изменений двигательной активности ЖКТ [15–17]. Рвота (то есть насильственное изгнание желудочно-кишечного содержимого через рот) является высокоорганизованным процессом, координируемым центром рвоты, который получает импульсы от нескольких периферических и центральных рецепторных полей. Этот процесс включает в себя следующие события. Расслабление желудка начинается за несколько минут до появления гигантского ретроградного сокращения (ГРС) тонкой кишки [17] и достигает максимума к моменту достижения ГРС антрума. ГРС появляется в средней части тонкой кишки и движется по направлению к антруму со скоростью 5–10 см/сек. Его появлению предшествует торможение перистальтики тонкой кишки и исчезновение медленных волн [16, 18]. После прохождения ГРС следуют фазы повышения и снижения тонуса кишки. Данные изменения моторики всегда сопровождают рвоту, но могут наблюдаться и независимо от нее [16, 18]. Блокада ретроградной двигательной активности, которая сопровождает тошноту и рвоту, может вносить вклад в общее прокинетическое действие антидопаминергических препаратов.
Предположение о том, что блокада допаминовых рецепторов может привести к прокинетическому действию, имеет обоснование в тех наблюдениях, которые свидетельствуют об очень широком распространении допамина в стенке пищеварительной трубки, где он оказывает отчетливое действие на моторику: уменьшает тонус нижнего пищеводного сфинктера, снижает тонус стенки желудка, уменьшает внутрижелудочное давление и угнетает гастродуоденальную координацию [19]. Поэтому блокада данных ингибирующих D2-допаминовых рецепторов селективными антагонистами оказывает прокинетический эффект. Кроме того, у домперидона можно предположить и наличие еще одного механизма, объясняющего его прокинетическое воздействие. Ряд работ продемонстрировал ингибирующий эффект допамина на стимулированное сокращение гладкомышечных клеток желудка морских свинок, обусловленный активацией альфа-2-адренорецепторов [20]. Впоследствии было установлено, что допамин угнетает высвобождение ацетилхолина в желудке морских свинок путем активации пресинаптических D2-рецепторов, и данный эффект снижается при применении домперидона, который, в свою очередь, отчетливо стимулирует сокращения стенки желудка [21]. Таким образом, по меньшей мере, на животных моделях, было показано наличие холинергического механизма прокинетического действия домперидона.
Домперидон как антидопаминергический препарат, обладающий прокинетическим действием, в клинической практике нашел применение в лечении диспепсических расстройств и тошноты и показан при лечении пациентов с ФД, гастропарезом различного генеза, включая диабетический, а также для предупреждения и купирования тошноты и рвоты.
Были проведены многочисленные клинические исследования, продемонстрировавшие эффективность домперидона при лечении этих состояний [22, 23]. Подробный анализ этих исследований лежит за рамками данной работы, но, тем не менее, среди них следует упомянуть работу Sturm, доказавшую большую эффективность домперидона по сравнению с метоклопрамидом в лечении гастропареза [24], а также метаанализ, который провели V. Van Zanten et al., продемонстрировавший эффективность домперидона в лечении ФД и установивший его семикратное превосходство над плацебо — отношение шансов (ОШ) 7,0 (95% ДИ, 3,6–16) [25]. Это несомненно делает Мотилиум® (оригинальный домперидон) препаратом выбора в лечении больных с ФД.
Мотилиум® (оригинальный домперидон) плохо проникает через гематоэнцефалический барьер, что, с одной стороны, подчеркивает его безопасность, с другой стороны, делает препаратом выбора для предупреждения и устранения тошноты, в том числе индуцированной применением L-DOPA у больных с болезнью Паркинсона [26], при проведении химиотерапии, после хирургических вмешательств, при мигрени. Экстрапирамидные расстройства при применении домперидона встречаются редко, в отличие от других препаратов данной группы, в частности метоклопрамида [27–29].
Таким образом, изучение механизмов влияния допамина на двигательную функцию пищеварительного тракта, особенностей функционирования рецепторов допамина позволили внедрить в практику один из самых эффективных классов гастроэнтерологических препаратов — селективные антагонисты D2-рецепторов. Наиболее изученным в многочисленных исследованиях, доказавшим свою эффективность в клинической практике представителем этого класса является Мотилиум® (оригинальный домперидон).
Литература
- Palermo-Neto J. Dopaminergic systems. Dopamine receptors // Psychiatr Clin North Am. 1997; 20: 705–721.
- Willems J. L., Buylaert W. A., Lefebvre R. A., Bogaert M. G. Neuronal dopamine receptors on autonomic ganglia and sympathetic nerves and dopamine receptors in the gastrointestinal system // Pharmacol Rev. 1985; 37: 165–216.
- Mann R., Bell C. Distribution and origin of aminergic neurones in dog small intestine // J Auton Nerv Syst. 1993; 43: 107–115.
- Eisenhofer G., Aneman A., Friberg P. et al. Substantial production of dopamine in the human gastrointestinal tract // J Clin Endocrinol Metab.1997; 82: 3864–3871.
- Hartman D. S., Civelli O. Dopamine receptor diversity: molecular and pharmacological perspectives // Prog Drug Res. 1997; 48: 173–194.
- Sidhu A. Coupling of D1 and D5 dopamine receptors to multiple G proteins: implications for understanding the diversity in receptor-G protein coupling // Mol Neurobiol. 1998; 16: 125–134.
- Kopin I. J. Catecholamine metabolism: basic aspects and clinical significance // Pharmacol Rev. 1985; 37: 333–364.
- Shichijo K., Sakurai-Yamashita Y., Sekine I., Taniyama K. Neuronal release of endogenous dopamine from corpus of guinea pig stomach // Am J Physiol.1997; 273: G1044–1050.
- Valenzuela J. E. Dopamine as a possible neurotransmitter in gastric relaxation // Gastroenterology. 1976; 71: 1019–1022.
- Crocker A. D. A new view of the role of dopamine receptors in the regulation of muscle tone // Clin Exp Pharmacol Physiol. 1995; 22: 846–850.
- Tonini M. Recent advances in the pharmacology of gastrointestinal prokinetics // Pharmacol Res. 1996; 33: 217–226.
- Schuurkes J. A., Van Nueten J. M. Domperidone improves myogenically transmitted antroduodenal coordination by blocking dopaminergic receptor sites // Scand J Gastroenterol Suppl. 1984; 96: 101–110.
- Nagahata Y., Urakawa T., Kuroda H. et al. The effect of dopamine on rat gastric motility // Gastroenterol Jpn. 1992; 27: 482–487.
- Wiley J., Owyang C. Dopaminergic modulation of rectosigmoid motility: action of domperidone // J Pharmacol Exp Ther. 1987; 242: 548–551.
- Wang S. C., Borison H. L. A new concept of organization of the central emetic mechanism: recent studies on the sites of action of apomorphine, copper sulfate and cardiac glycosides // Gastroenterology. 1952; 22: 1–12.
- Lang I. M., Sarna S. K., Condon R. E. Gastrointestinal motor correlates of vomiting in the dog: quantification and characterization as an independent phenomenon // Gastroenterology. 1986; 90: 40–47.
- De Ponti F., Malagelada J. R., Azpiroz F., Yaksh T. L., Thomforde G. Variations in gastric tone associated with duodenal motor events after activation of central emetic mechanisms in the dog // J Gastrointest Motil. 1990; 2: 1–11.
- De Ponti F. Pharmacology of emesis and gastrointestinal motility: implications for migraine // Funct Neurol. 2000; 15 (Suppl. 3): 43–49.
- Demol P., Ruoff H. J., Weihrauch T. R. Rational pharmacotherapy of gastrointestinal motility disorders // Eur J Pediatr. 1989; 148: 489–495.
- Costall B., Naylor R. J., Tan C. C. The mechanism of action of dopamine to inhibit field stimulation-induced contractions of guinea pig stomach strips // Naunyn Schmiedebergs Arch Pharmacol. 1984; 328: 174–179.
- Kusunoki M., Taniyama K., Tanaka C. Dopamine regulation of [3H]acetylcholine release from guinea-pig stomach // J Pharmacol Exp Ther. 1985; 234: 713–719.
- Soykan I., Sarosiek I., McCallum R. W. The effect of chronic oral domperidone therapy on gastrointestinal symptoms, gastric emptying, and quality of life in patients with gastroparesis // Am J Gastroenterol. 1997; 92: 976–980.
- Barone J. A. Domperidone: a peripherally acting dopamine2-receptor antagonist // Ann Pharmacother. 1999; 33: 429–440.
- Sturm A., Holtmann G., Goebell H., Gerken G. Prokinetics in patients with gastroparesis: a systematic analysis // Digestion. 1999; 60: 422–427.
- Veldhuyzen van Zanten S. J., Jones M. J., Verlinden M., Talley N. J. Efficacy of cisapride and domperidone in functional (nonulcer) dyspepsia: a meta-analysis // Am J Gastroenterol. 2001; 96: 689–696.
- Soykan I., Sarosiek I., Shifflett J., Wooten G. F., McCallum R. W. Effect of chronic oral domperidone therapy on gastrointestinal symptoms and gastric emptying in patients with Parkinson’s disease // Mov Disord. 1997; 12: 952–957.
- Pinder R. M., Brogden R. N., Sawyer P. R., Speight T. M., Avery G. S. Metoclopramide: a review of its pharmacological properties and clinical use // Drugs. 1976; 12: 81–131.
- Brogden R. N., Carmine A. A., Heel R. C., Speight T. M., Avery G. S. Domperidone. A review of its pharmacological activity, pharmacokinetics and therapeutic efficacy in the symptomatic treatment of chronic dyspepsia and as an antiemetic // Drugs. 1982; 24: 360–400.
- Sol P., Pelet B., Guignard J. P. Extrapyramidal reactions due to domperidone // Lancet. 1980; 2: 802.
А. С. Трухманов, доктор медицинских наук, профессор
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития России, Москва
РЕГУЛЯЦИЯ ДЕЯТЕЛЬНОСТИ ОРГАНОВ ПИЩЕВАРЕНИЯ
В регуляции деятельности органов пищеварения следует различать:
- 1) регуляцию приема корма;
- 2) регуляцию образования в нужных объеме и составе пищеварительных соков, секреторной деятельности;
- 3) регуляцию сократительной деятельности желудка и кишечника;
- 4) регуляцию всасывательной деятельности.
Регуляция приема корма
Она осуществляется центром питания (или голода), расположенным в гипоталамусе. Здесь же расположен центр насыщения. Рефлекторно со зрительных, обонятельных, вкусовых рецепторов, хеморецепторов сосудов, механо- и хеморецепторов желудка при недостатке питательных веществ в крови информация поступает в центр питания (гипоталамус) и обусловливает поиск и прием корма. При захвате корма информация с вкусовых рецепторов поступает в центр жевания (продолговатый мозг) и обусловливает жевание. Сформированная в нервном центре программа действия поступает к жевательным мышцам и вызывает захват корма и жевание. Формируется пищевой ком, который вызывает возбуждение рецепторов и центра глотания, периферического глотательного аппарата и глотание. Торможение центра голода происходит после насыщения (заполнения кормом желудка) рефлекторно с рецепторов желудка, возбуждается центр насыщения, прекращается прием корма.
Регуляция образования и выделения в нужных объемах и составах пищеварительных соков, сократительной и всасывательной деятельности желудка и кишечника
Регуляция образования и выделения пищеварительных соков, сократительной и всасывательной деятельности желудка и кишечника осуществляется рефлекторно-гормонально в три фазы.
I фаза — сложно-рефлекторная. В период этой фазы возбуждение пищеварительных желез, сократительного и всасывательного аппаратов желудка и кишечника осуществляется по типу условного рефлекса с рецепторов зрения, слуха, обоняния на вид, запах корма, сопровождающие прием корма, и безусловного рефлекса с рецепторов ротовой полости, раздражаемых пищевыми компонентами самого корма.
II фаза — желудочная нервно-гормональная. В эту фазу регуляции возбуждение пищеварительных желез, сократительного и всасывательного аппаратов желудка и кишечника продолжается за счет раздражения рецепторов желудка с момента поступления в него корма, причем с участием тканевых гормонов желудка и кишечника (гаст- рина, гистамина, мотилина, энтерогастрина, возбуждающих желудочные железы; гастрона, энтерогастрона, секретина, холецистоки- нина, желудочного тормозного полипептида, вазоактивного кишечного пептида, тормозящих желудочные железы).
III фаза — кишечная нервно-гормональная. В эту фазу возбуждение пищеварительных желез, сократительного и всасывательного аппаратов желудка и кишечника продолжается с момента поступления химуса в кишечник, причем с участием тканевых гормонов кишечника (секретина, холецистокинина, возбуждающих поджелудочную железу, глюкагона, простагландина, тормозящих ее дуокринина, эн- терокинина, гастрина, кишечного полипептида, холецистокинина, возбуждающих, секретина тормозящего кишечные железы).
Рефлекторная регуляция с рецепторов желудка и кишечника осуществляется через афферентные и эфферентные нервные волокна блуждающих и чревных нервов, а также центр, расположенный в продолговатом мозге. Через парасимпатические эфферентные волокна блуждающих нервов передаются влияния, стимулирующие секреторную деятельность желудочных, поджелудочной, кишечных желез и секреторных клеток печени, сократительную деятельность желудка и кишечника, всасывательную деятельность всасывательного аппарата. Через симпатические нервные волокна чревных нервов передаются влияния, повышающие активность ферментов, силу сокращений желудка и кишечника, активность ферментов переносчиков, всасывательного аппарата. К слюнным железам из центра стимулирующие влияния передаются по парасимпатическим волокнам языкоглоточного нерва (к околоушным железам), лицевого нерва, барабанной струны (к подчелюстным и подъязычным железам) и по симпатическим волокнам (от краниального шейного симпатического узла).
Дискинезия желудка
Дискинезия желудка – это функциональное нарушение сократительной активности органа, которое может протекать по гиперкинетическому и гипокинетическому типу (вплоть до полной атонии). Основные признаки патологии – боли в животе различной интенсивности без четкой локализации, не связанные с приемом пищи, а также диспепсические явления. Диагностика основана на характерной клинической картине, рентгенологическом определении нарушения моторики и отсутствии гистологических признаков органической патологии. Лечение комплексное, направлено на коррекцию нейропсихических нарушений и моторики желудка; эффективна физиотерапия.
Общие сведения
Дискинезия желудка – функциональное расстройство, характеризующееся нарушением моторики желудка; может протекать с диспепсическими явлениями и болевым синдромом, однако при этом гастроскопия не выявляет органических изменений. В современной гастроэнтерологии дискинезия является довольно распространенным заболеванием: примерно у трети пациентов, предъявляющих жалобы со стороны желудочно-кишечного тракта, не удается обнаружить морфологических изменений.
Данная патология распространена у лиц молодого возраста, а также у пациентов с функциональными или органическими заболеваниями центральной нервной системы. Многие специалисты считают, что такой диагноз нередко ошибочно выставляется на начальных стадиях заболеваний органов пищеварения, эндокринной, мочевыделительной, нервной систем, и с этим связана проблема гипердиагностики. Поэтому в настоящее время диагноз дискинезии правомочен только после исключения органических изменений желудка с помощью всех доступных диагностических методов.
Причины
Наиболее частыми причинами дискинезии желудка выступают алиментарные факторы: нерациональное питание (особенно отсутствие регулярного ритма), частая еда всухомятку, слишком быстрый прием пищи без достаточной механической и ферментативной обработки в ротовой полости; преобладание в рационе углеводных продуктов, дефицит витаминов и микроэлементов, белка; злоупотребление острым и жирным. Нарушение моторики желудка может быть проявлением аллергической реакции организма на пищевые продукты, чаще всего белки коровьего молока, яйца, рыбу.
Дискинезия также возникает в результате токсического влияния химических веществ, алкоголя, никотина. При воздействии таких экзогенных факторов происходит раздражение хемо- и барорецепторов желудка. Важная роль в этиологии дискинезии отводится заболеваниям нервной системы: как частым нервно-психическим стрессам, так и тяжелым органическим изменениям (инсультам, внутримозговым опухолям, энцефалиту).
Распространенными экзогенными этиологическими факторами дискинезии желудка служат высокая температура окружающей среды, действие ионизирующего излучения и вибрации, ожоги. Возможно нарушение двигательной функции желудка при приеме некоторых лекарственных препаратов, влияющих на вегетативную нервную систему, гипоталамус, эндокринные органы.
Из эндогенных факторов к нарушениям моторики желудка чаще всего приводят другие заболевания пищеварительной системы: холецистит, панкреатит, энтерит. Патологию могут провоцировать вирусные гепатиты. Иногда дискинезия желудка вплоть до атонии является одним из симптомов заболеваний сердца и сосудов, в частности – инфаркта миокарда. Возможно снижение моторики и при гипертонической болезни, ревматизме.
Функциональные изменения желудка могут развиться при любых заболеваниях, сопровождающихся интоксикацией. Довольно часто дискинезия сопровождает гнойно-воспалительные заболевания легких (в том числе туберкулез), патологию почек, а также эндокринной системы. В развитии функциональных нарушений при соматической патологии основная роль отводится висцеро-висцеральным рефлексам и воздействию нейрогуморальных механизмов (нарушению выработки гастроинтестинальных гормонов, пищеварительных ферментов и других веществ).
Классификация
В зависимости от типа нарушения моторики выделяют гипертоническую (с повышенной двигательной функцией), гипотоническую (с пониженной) и атоническую дискинезию желудка. По преобладающему клиническому синдрому заболевание классифицируют на болевой, диспепсический и смешанный тип. Дискинезия также подразделяется на экзогенную, при которой функциональные расстройства желудка вызваны внешними факторами (чаще алиментарными), и эндогенную, возникающую при патологии других органов и систем. Некоторые авторы выделяют следующие варианты течения патологии:
- Ахалазия кардии - спастическое сокращение кардии желудка, характеризуется затрудненным глотанием, выраженной болью за грудиной.
- Пилороспазм- спазм пилорического отдела, сопровождается нарушением эвакуации содержимого желудка и отрыжкой кислым, болью в эпигастрии.
- Тетания - судорожные спазмы желудка с интенсивной болью и гастрокардиальным синдромом.
- Острое расширение желудка - возникает при хроническом переедании и в послеоперационном периоде, когда существенно снижен тонус желудка.
- Аэрофагия - функциональные расстройства при быстром заглатывании еды с большим количеством воздуха.
Симптомы дискинезии желудка
Основное проявление патологии – болевой синдром в области живота без четкой локализации. Боль может возникать в эпигастрии, подреберьях, околопупочной области, при этом длительность приступа различная – от нескольких минут и часов до недель. Характер ощущений также может отличаться: некоторые пациенты описывают интенсивные схваткообразные боли, другие – ноющие, давящие (это зависит от характера и степени нарушения моторики). Возникновение таких признаков связано не с приемом пищи или его отсутствием, а чаще с нервно-психическим фактором.
При наличии антиперистальтических сокращений мышечного слоя желудка и забросе кислого содержимого в пищевод пациентов беспокоит изжога, отрыжка кислым. Выраженное снижение сократительной активности желудка приводит к застою его содержимого, появлению отрыжки тухлым. Дискинезия, развившаяся на фоне патологии ЦНС и раздражения рвотного центра, сопровождается обильной повторной рвотой, которая не приносит облегчения.
Все вышеописанные признаки нарушения моторики желудка могут иметь разную интенсивность и не являются специфичными - такие жалобы пациенты предъявляют при множестве других заболеваний. Но для дискинезии желудка характерна связь развития симптомов с психическими травмами и стрессами, наличие общих проявлений невроза, изменчивость жалоб и уменьшение их в ночное время, а также отсутствие признаков органической патологии при эндоскопическом и гистологическом исследовании.
Диагностика
Основой диагностики дискинезии желудка является исключение органической патологии при наличии характерной клинической картины. При проведении консультации гастроэнтеролога предположительно устанавливается тип изменения моторики и вероятный этиологический фактор (психоневрологические изменения, нерациональный режим питания, труда и отдыха, имеющиеся заболевания). При проведении пальпации живота возможно выявление болезненности, при атонии желудка перкуторно специалист может определить расширение границ органа.
Нарушения моторики желудка может выявить электрогастрография – метод регистрации электрических потенциалов при сокращении мышечного слоя органа. Для дискинезии желудка характерна высокая вариабельность результатов электрофизиологического исследования во временном промежутке. Высокой информативностью обладает рентгеноскопия желудка, которая дает возможность определить спазм или гипотонию органа, нарушения перистальтики, гастроэзофагеальный рефлюкс, опущение органа, пилороспазм или кардиоспазм.
К обязательным методам диагностики относится гастроскопия: характерной эндоскопической картиной является утолщение складок слизистой желудка без ее макроскопических изменений. При проведении исследования спастические сокращения желудка могут возникнуть при введении даже небольшого количества воздуха. В процессе эзофагогастродуоденоскопии обязательно осуществляется биопсия, поскольку именно отсутствие гистологических изменений является важнейшим дифференциально-диагностическим критерием дискинезии.
Лечение дискинезии желудка
Лечение данной патологии проводится обычно в амбулаторных условиях, госпитализация может потребоваться при выраженном болевом синдроме с целью выполнения диагностических процедур. Обязательным мероприятием является коррекция питания: соблюдение режима, объема порций пищи. С целью нормализации нервной регуляции моторики назначаются нейротропные и психотропные препараты, седативные средства. Коррекция сократительной активности желудка при гиперкинезии проводится М-холинолитиками, при гипокинезии назначаются кофеин, эуфиллин, в случае атонии – неостигмин.
Чаще всего дискинезия сочетается с патологией секреторной функции желудка, поэтому обязательной составляющей лечения является проведение заместительной терапии (натуральный желудочный сок, пепсин, препараты ферментов поджелудочной железы). Высокой эффективностью при дискинезии желудка обладает физиотерапия: электрофорез с новокаином, согревающие процедуры, грязевые аппликации, диатермия, парафинолечение и озокеритотерапия. Выбор методики определяется типом нарушения моторики и ведущим клиническим синдромом.
Прогноз и профилактика
Прогноз при дискинезии желудка благоприятный: заболевание хорошо поддается коррекции, трудоспособность сохранена. Пациенты подлежат диспансеризации, поскольку при неадекватном лечении заболевания и его длительном течении возможны выраженные деструктивные изменения слизистой оболочки желудка. Профилактика заключается в своевременном эффективном лечении патологии ЖКТ и других систем. С целью уменьшения частоты обострений рекомендуется санаторно-курортное лечение, коррекция режима труда и отдыха, питания.
Читайте также:
