Показания для дренирования псевдокисты поджелудочной железы в желудок
Обновлено: 14.05.2024
ГБУЗ Москвы «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия
ГБУЗ «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского» Департамента здравоохранения Москвы, Москва, Россия;
ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования», Москва, Россия
- SPIN РИНЦ: 4044-9661
- Scopus AuthorID: 55970485700
- ResearcherID: P-9151-2017
- ORCID: 0000-0003-1270-5414
Первый опыт эндоскопического лечения кистозных образований поджелудочной железы доброкачественного генеза
В статье представлен первый опыт применения эндоскопического метода лечения 23 пациентов с кистозными образованиями поджелудочной железы доброкачественного генеза. Цель исследования — оценить результаты эндоскопического цистогастро- и цистодуоденального стентирования при кистозных образованиях поджелудочной железы доброкачественного генеза. Материал и методы. Пролечены 23 пациента с острым панкреатитом и псевдокистой поджелудочной железы. Всем пациентам при поступлении выполнено ультразвуковое исследование (УЗИ), результаты которого позволили выявить кистозные образования поджелудочной железы, что явилось показанием к наложению цистогастроанастомоза. Пациентам в зависимости от расположения псевдокисты поджелудочной железы через желудок или двенадцатиперстную кишку в полость кисты вводили цистотом и выполняли аспирацию содержимого, после чего под рентгенологическим контролем производили контрастирование с целью определения ее точных размеров и герметичности, наличия связи с внутрипротоковой системой поджелудочной железы. Затем устанавливали пластиковый или металлический стент и проводили визуальный осмотр. Сразу после манипуляции выполняли рентгенографию органов брюшной полости с целью установления наличия или отсутствия свободного газа. После наложения цистогастроанастамоза на 2-е и 7-е сутки после операции проводили контроль с применением эндоскопической ультрасонографии для оценки адекватности дренирования псевдокисты. При неадекватном дренировании выполняли цистоназальное дренирование с использованием назобилиарного дренажа и последующей ежедневной санацией кисты. Результаты. Применение эндоскопического метода дренирования псевдокист под контролем эндоскопической ультрасонографии позволило достигнуть полного регресса полости кисты у 81,8% пациентов и уменьшения полости кисты более чем в 2 раза — у 18,2%. Выводы. Доказана высокая эффективность эндоскопического метода дренирования псевдокист под контролем эндоскопической ультрасонографии. Данный метод отличается малоинвазивностью, минимальным риском развития послеоперационных осложнений и летальности, коротким послеоперационным периодом по сравнению с оперативными вмешательствами, выполняемыми с применением лапаротомного или лапароскопического доступов.
В структуре острых хирургических заболеваний органов брюшной полости острый панкреатит (ОП) занимает 3-е место, составляя от 4,5 до 10% [1—7]. Отмечено, что заболеваемость ОП не имеет тенденции к снижению, а летальность с 1990 по 2015 г. возросла на 62% [8].
Деструктивные формы ОП в ранние сроки осложняются парапанкреатическим инфильтратом или абсцессом, перитонитом или флегмоной забрюшинной клетчатки. К поздним осложнениям относятся псевдокисты (ПК), частота выявления которых составляет от 0,1 до 1 случая на 100 000 взрослого населения в год [9, 10]. У мужчин в 57—84% случаев развитие ОП с исходом в ПК поджелудочной железы (ПЖ) связано со злоупотреблением алкоголем [11]. У женщин наиболее частым этиологическим фактором является желчнокаменная болезнь, которая встречается в 31—65% случаев [12]. На 2-м месте по частоте образования кист как у мужчин, так и у женщин находится травматический панкреатит, при котором псевдокисты формируются в 10—20% случаев [13].
Остается актуальной проблема выбора срока, объема и вида оперативного вмешательства. Приоритетные параметры для решения о хирургическом лечении следующие: 1) локализация и размеры ПК; 2) «зрелость» стенок ПК; 3) взаимосвязь с протоковой системой ПЖ [14—16]. На сегодняшний день широко используются различные варианты резекционных и дренирующих операций с лапаротомным или лапароскопическим доступом [15, 16]. При этом длительность стационарного лечения достигает 28 дней. В 15—29% наблюдений оперативное лечение сопровождается осложнениями, летальность достигает 17% [17—19].
Впервые эндоскопическое чрезжелудочное дренирование ПК с аспирацией содержимого выполнено в 1975 г. Эта операция заключалась в опорожнении кисты в просвет желудка. Попадание желудочного сока привело к инфицированию и нагноению ПК, а также к быстрой облитерации цистогастроанастомоза [16]. Это послужило поводом к разработке метода цистоназального дренирования ПК с аспирацией содержимого и ее санацией [20]. Наиболее перспективным методом является формирование эндоскопического цистогастроанастомоза с использованием синтетических стентов, предотвращающих быструю облитерацию соустья [21—23].
Цель исследования — оценить результаты эндоскопического цистогастро- и цистодуоденального стентирования при кистозных образованиях поджелудочной железы доброкачественного генеза.
Материал и методы
С ноября 2011 г. по декабрь 2018 г. в Научно-исследовательском институте скорой помощи им. Н.В. Склифосовского пролечены 23 пациента (20 (87%) мужчин и 3 (13%) женщины, средний возраст составил 52 года (39; 59 лет)) с ОП и развитием ПК П.Ж. Выполнено эндоскопическое дренирование ПК.
Диагноз ПК ПЖ установлен на основании анамнеза и трансабдоминального ультразвукового исследования (УЗИ), эндоскопической ультрасонографии (ЭУС) и компьютерной томографии (КТ). Для оценки сроков образования ПК использовали классификацию J. Howard и J. Jordar (1960), модифицированную J. Berk и W. Haubrich (1965), согласно которой все ПК делятся на острые — до 90 сут, подострые — от 91 до 180 сут и хронические — более 181 сут [7].
Размер и локализацию ПК устанавливали по данным УЗИ и К.Т. Все П.К. разделили в зависимости от размера на гигантские — более 15,1 см, большие — от 10,1 до 15 см, средние — от 5,1 до 10 см, малые — менее 5 см. Кроме этого, определяли их локализацию в П.Ж. При наличии нескольких кист учитывали локализацию наибольшей из них.
Для эндоскопического дренирования ПК под контролем ЭУС использовали ультразвуковую эндоскопическую систему Exera II и конвексный эхоэндоскоп Olympus GF-UCT140 («Olympus Corporation», Япония), рентгеновскую установку («Ziehm Imaging», Германия), цистотом («Соок Medical», США, Дания, Ирландия), струну диаметром 9 мм («Olympus Corporation», Япония), пластиковые стенты типа Pig Tail («Olympus Corporation», Япония), металлические саморасширяющиеся стенты Endostars и специальные саморасширяющиеся стенты для дренирования кист ПЖ HANAROSTENT («M.I. Tech Co. Ltd.», Республика Корея).
Вмешательство выполняли под общей анестезией в положении больного на спине. При осмотре желудка или двенадцатиперстной кишки выявляли выбухание их стенок за счет сдавления извне. При ЭУС определяли расстояние между стенками и выявляли бессосудистую область для безопасной установки стента. Применение ЭУС позволило выбрать точку дренирования ПК, которая у 20 (87%) пациентов локализовалась в желудке, у 3 (13%) — в двенадцатиперстной кишке. Через намеченную точку выполняли гастроцистостомию или дуоденоцистостомию. Аспирировали содержимое и контрастировали ПК для определения ее точных размеров, герметичности и связи с протоковой системой ПЖ. В просвет кисты по каналу цистостомы заводили струну, по которой устанавливали пластиковый или металлический стент. Инструменты извлекали и проводили визуальный осмотр стента. Выполняли рентгеноскопию для оценки размеров полости. При выявлении связи ПК с протоковой системой ПЖ проводили эндоскопическую ретроградную панкреатикографию, вирсунготомию и стентирование главного панкреатического протока пластиковым стентом длиной 6 см, диаметром 5 °F.
После операции выполняли рентгенографию брюшной полости с целью установления наличия или отсутствия свободного газа. На 2-е и 7-е сутки после операции проводили УЗИ.
В послеоперационном периоде всем пациентам внутривенно вводили цефтриаксон 1,0 г 2 раза в сут или метронидазол 500 мг 3 раза в сут в течение 7 дней; внутривенно вводили 0,9% раствор хлорида натрия по 500 мл 2 раза в сутки в течение 3 дней. В качестве антисекреторной терапии применяли омепразол 20 мг 2 раза в сут в течение 7 дней. Проводили спазмолитическую терапию — дротаверин 40 мг внутримышечно 2 раза в сут в течение 7 дней. Для купирования болевого синдрома использовали трамадол — 50 мг или тримеперидин — 10 мг.
Эффективность эндоскопической операции оценивали по изменению объема полости кисты по данным УЗИ или К.Т. При невозможности адекватного дренирования ПК пластиковым стентом под рентгенологическим контролем устанавливали саморасширяющийся стент и назобилиарный дренаж диаметром 7 °F с последующей ежедневной санацией полости ПК.
Для оценки хирургических осложнений применяли классификацию хирургических осложнений Clavien—Dindo (2004).
Результаты и обсуждение
Причиной ОП с развитием ПК у 15 (65,2%) пациентов явилась желчнокаменная болезнь, у 7 (30,5%) — злоупотребление алкоголем, у 1 (4,3%) — перенесенная операция резекция хвоста ПЖ по поводу цистаденомы. Средний срок повторного обращения после перенесенного панкреонекроза составил в среднем 315 (135; 720) дней. При этом острые формы ПК выявлены у 3 (13%) пациентов, подострые — у 4 (17,4%), хронические — у 16 (69,6%), что свидетельствует о рецидивирующем течении О.П. Гигантские П.К. при УЗИ были выявлены у 3 (13%) больных, большие — у 5 (21,7%), средние — у 14 (60,9%), малые — у 1 (4,4%). У всех пациентов с гигантскими ПК имело место сдавление антрального отдела желудка и двенадцатиперстной кишки, что приводило к сочетанию болевого синдрома с нарушением эвакуации из желудка.

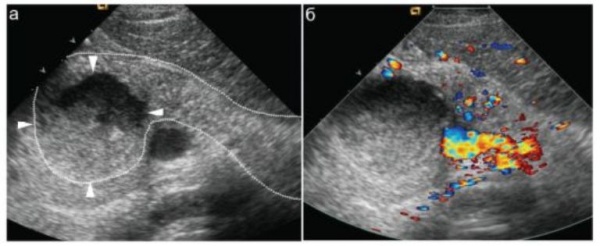
ПК локализовались в теле ПЖ у 7 (30,4%) пациентов, в хвосте ПЖ — у 7 (30,4%), в головке ПЖ — у 6 (26,2%) (рис. 1). Рис. 1. Псевдокиста головки поджелудочной железы (изображение при ультразвуковом исследовании). Стрелками указаны полость псевдокисты (1), бессосудистая зона (2). The arrows indicate pseudocyst cavity (1), avascular zone (2). У 3 (1%) больных имело место сочетанное расположение ПК в головке и теле ПЖ.

Пластиковые стенты применяли при наличии «зрелой» фиброзной капсулы толщиной от 3 до 9 мм и однородном содержимом кисты. Металлические саморасширяющиеся стенты устанавливали в отсутствие капсулы, при инфицированном содержимом и наличии секвестров (рис. 2). Рис. 2. Состояние после цистогастростомии. а — саморасширяющийся стент в просвете инфицированной кисты указан стрелкой (изображение получено при эндоскопической ультрасонографии); б — саморасширяющийся стент в просвете инфицированной кисты указан стрелкой 2 (по данным рентгенографии); в — пластиковый стент в просвете неинфицированной кисты указан стрелкой (изображение получено при эндоскопической ультрасонографии); г — пластиковый стент в просвете неинфицированной кисты указан стрелками (по данным рентгенографии). a — self-expanding stent inside infected cyst is indicated by the arrow 2 (us); b — self-expanding stent inside infected cyst is indicated by the arrow 2 (X-ray); c — plastic stent inside sterile cyst is indicated by the arrow (us); d — plastic stent inside sterile cyst is indicated by the arrows (X-ray).

После эндоскопической цистогастростомии у 8 (34,7%) больных отмечен умеренный болевой синдром в верхних отделах живота, у 6 (26,1%) — сочетание болевого и диспепсического синдромов, у 4 (17,4%) — выраженный болевой синдром, у 3 (13%) — подъемы температуры тела до субфебрильных цифр. Не предъявляли никаких жалоб 2 (8,7%) больных. Точка доступа для эндоскопического дренирования зависела от локализации ПК: при ее расположении в хвосте оптимальными областями для стентирования были тело желудка (56,5%) и задняя стенка антрального отдела желудка (21,7%), а при ее расположении в головке — двенадцатиперстная кишка (13,1%) (см. таблицу). Локализация цистостомы в желудке и двенадцатиперстной кишке (n=23) Примечание. Данные представлены в виде абсолютных и производных (%) величин.
Серозно-геморрагическое содержимое ПК было у 20 (85%) больных, в связи с этим им были установлены пластиковые стенты, а гнойное содержимое — у 3 (15%), что явилось показанием для применения саморасширяющихся стентов.
Связь ПК с протоковой системой ПЖ имелась у 2 (8,7%) пациентов, что явилось показанием к стентированию главного панкреатического протока. На момент выписки по данным УЗИ жидкостные образования в тканях ПЖ у пациентов отсутствовали, а полость кисты не определялась.
Выраженный болевой синдром после цистогастростомии отметили у 4 (17,4%) пациентов в 1-е сутки. При рентгеноскопии в брюшной полости выявлен свободный газ. На фоне консервативной терапии болевой синдром купирован. При УЗИ выявлено минимальное количество жидкости в брюшной полости у 2 больных. При УЗИ на 3-и и 4-е сутки жидкость в брюшной полости отсутствовала, полость ПК не определялась.
При попытке эндоскопической цистогастростомии у 1 (4,3%) пациента отмечено большое количество свободного газа в брюшной полости. При ЭУС выявлено разобщение стенок желудка и ПК, что явилось показанием к конверсии и хирургическому наложению цистогастроанастомоза.

Контрольное УЗИ, выполненное перед выпиской, выявило отсутствие жидкостного образования у 18 (81,9%) пациентов, у 4 (18,2%) — уменьшение полости ПК более чем в 2 раза (рис. 3). Рис. 3. Стент в области головки поджелудочной железы, полость отсутствует, стрелками указаны края стента (изображение при ультразвуковом исследовании).
Таким образом, осложнения возникли у 5 (21,7%) из 23 больных, у 4 из них отмечали хирургические осложнения I степени и в 1 наблюдении — IIIb степени.
Ведущую роль в диагностике ПК играет УЗИ, которое у всех пациентов позволило обнаружить кистозное образование, оценить его размеры, локализацию, толщину капсулы. Для выявления бессосудистой области, необходимой для безопасной установки стента, использовали ЭУС. Для уточнения связи с протоковой системой ПЖ применяли эндоскопическую ретрограднаю панкреатографию. КТ применили у 3 больных, если данные УЗИ не позволяли оценить связь ПК с окружающими органами.
При наличии сформированной фиброзной капсулы и однородном жидкостном содержимом кисты выполняли установку пластиковых стентов. Отсутствие капсулы свидетельствует о наличии острого жидкостного скопления, которое нельзя дренировать через желудок. При выявлении секвестров, признаков инфицирования содержимого и в отсутствие капсулы при минимальной длине анастомоза (менее 1 см) устанавливали металлический саморасширяющийся стент.
После аспирации содержимого из ПК выполняли бактериологическое исследование, а также биохимическое исследование для определения уровня амилазы. Это позволило подтвердить инфицирование ПК и при необходимости скорректировать антибактериальную терапию, а также оценить связь ПК с протоковой системой ПЖ.
Всем пациентам после эндоскопического оперативного вмешательства рекомендовано проведение рентгенологического исследования органов брюшной полости с целью установления наличия или отсутствия свободного газа. Как показал наш опыт, после вмешательства наличие свободного газа у 8,7% пациентов не явилось показанием к обязательной конверсии, достаточно было динамического наблюдения.
Выполнение повторных УЗИ в фиксированные сроки позволяет оценить динамику изменения размеров П.К. Таким образом, предложенная лечебная тактика показала эффективность данного метода лечения ПК, однако малое число наблюдений является поводом для дальнейшего продолжения исследования.
Полученные данные имеют ограниченную © степень статистической значимости и IV уровень доказательности публикации (по классификации степени достоверности публикаций Оксфордского центра доказательной медицины).
Заключение
Эндоскопическое дренирование псевдокист поджелудочной железы под контролем эндоскопической ультрасонографии является высокоэффективным методом лечения: у 81,8% пациентов достигнут полный регресс полости, у 18,2% отмечено ее уменьшение более чем в 2 раза. Эндоскопическая цистогастростомия (цистодуоденостомия) является эффективным методом лечения с минимальным риском послеоперационных осложнений: конверсия потребовалась лишь у 1 (4,3%) больного. При острой псевдокисте показана установка саморасширяющегося стента, что позволяет выполнять программную санацию полости псевдокисты и проводить цистоназальное дренирование. При хронической псевдокисте рекомендуется устанавливать пластиковый стент, этого достаточно для адекватного дренирования ПК.
Ложная киста поджелудочной железы
Ложная киста поджелудочной железы (псевдокиста) – полость в паренхиме поджелудочной железы, лишенная эпителиальной выстилки и содержащая панкреатический секрет и тканевой детрит. Причиной развития патологии наиболее часто являются панкреатиты (острые и хронические), реже – травмы брюшной полости. Основной признак заболевания - боль, интенсивность которой максимально выражена на первом этапе формирования полости. Также характерны диспепсические жалобы. Диагностическая программа включает рентгенографию органов брюшной полости, УЗИ и КТ поджелудочной железы, РХПГ. Лечение комплексное: фармакотерапия, эндоскопические и хирургические вмешательства (дренирующие или удаление кисты).
МКБ-10


Общие сведения
Ложная киста поджелудочной железы относится к опухолеподобным процессам. Данная патология представляет серьезную проблему в гастроэнтерологии, тесно связанную с увеличением заболеваемости населения острыми и хроническими панкреатитами, которые являются основной причиной формирования псевдокист. При алкогольном панкреатите ложные кисты поджелудочной железы образуются у 34-50% пациентов.
Псевдокисты склонны к нагноению, перфорации, малигнизации, образованию плохо поддающихся лечению внутренних и наружных свищей, чем обусловлена высокая летальность при данной патологии – до 53%. Клиническая картина псевдокисты часто маскируется под обострение основного заболевания, в ряде случаев ложные кисты являются интраоперационными находками. Несмотря на постоянное совершенствование методик лечения, в том числе микрохирургических, на сегодняшний день отсутствует единый лечебно-диагностический алгоритм и «золотой стандарт» лечения пациентов.

Причины ложной кисты поджелудочной железы
Наиболее часто формированию панкреатических псевдокист предшествует острый и хронический панкреатит, при этом острая форма сопровождается формированием полости в паренхиме железы в половине, а хроническая – в 80% случаев. В зоне повреждения паренхимы органа происходят деструктивные изменения, отграничение воспалительной массы с ее уплотнением и последующим разрастанием в строме соединительной ткани. Тканевой детрит постепенно уничтожается иммунными клетками, и на его месте остается полость без эпителиальной выстилки.
Реже причиной образования ложных кист поджелудочной железы выступает травма органа. Посттравматические псевдокисты - это гематомы с большим количеством панкреатических ферментов. Они обладают склонностью к быстрому нагноению, в связи с чем требуют неотложного хирургического вмешательства. Отдельным вариантом посттравматических псевдокист являются ятрогенные ложные кисты, которые формируются после оперативных вмешательств. Такие псевдокисты представляют собой затеки желчи (это осложнение характерно для лапароскопической холецистэктомии) или панкреатического сока (развиваются после резекции поджелудочной железы). После обширных хирургических вмешательств в поджелудочной железе может скапливаться осумкованная перитонеальная жидкость.
Иногда псевдокисты образуются при ограничении воспалительного процесса вследствие применения высоких дозировок ингибиторов панкреатических ферментов. Такие ложные кисты протекают на фоне хронического панкреатита. Редкой причиной формирования ложных кист поджелудочной железы является атеросклероз сосудов данного органа.
Классификация ложных кист поджелудочной железы
Панкреатические псевдокисты классифицируют по этиологии: возникающие после деструктивного панкреатита, посттравматические и другие. В зависимости от локализации различают псевдокисты головки, тела и хвоста панкреас.
Отдельно выделяют 4 стадии псевдокист, образующихся на месте очага деструкции паренхимы органа:
- Первая стадия характеризуется образованием начальной полости в зоне инфильтрации и аутолитических процессов, длится около шести недель.
- На второй стадии полость ограничивается рыхлой соединительнотканной капсулой, при этом продолжается разрушение инфильтрата иммунными клетками. Этот период может длиться 2-3 месяца.
- На третьей стадии псевдокиста «созревает» – образуется капсула из фиброзной ткани. Данный процесс происходит примерно через полгода от начала заболевания.
- Четвертая стадия характеризуется окончательным формированием плотной капсулы, которая легко отделяется от окружающих тканей.
В практической гастроэнтерологии чаще используется следующая классификация псевдокист:
- острые (до 2-3 месяцев)
- подострые (до полугода)
- хронические (более полугода).
Симптомы ложной кисты поджелудочной железы
Ведущим симптомом панкреатической псевдокисты является боль. Ее характеристики зависят от размера, локализации, а также стадии формирования полости. Наиболее интенсивную боль испытывают пациенты в первом периоде «созревания» псевдокисты, когда происходят деструктивные процессы в паренхиме органа. Через некоторое время боль стихает, становится тупой. У некоторых пациентов остается только ощущение дискомфорта. В дальнейшем возможны повторные болевые приступы, которые связаны с гипертензией в протоках поджелудочной железы. Значительное усиление боли может свидетельствовать о развитии таких осложнений, как разрыв, нагноение, кровоизлияние в полость псевдокисты.
Локализация болевых ощущений зависит от расположения псевдокисты: при образовании в области головки панкреас боли возникают в правом подреберье, тела и хвоста – в эпигастрии и левом подреберье. Некоторых пациентов беспокоят постоянные боли, что может быть связано с давлением псевдокисты на солнечное сплетение. В таких случаях ощущения усиливаются при смене положения тела, физических нагрузках, давлении поясом одежды. Характерны также диспепсические жалобы: тошнота, рвота, ухудшение аппетита.
Диагностика ложной кисты поджелудочной железы
Важную роль в диагностике панкреатических псевдокист играет оценка анамнеза и объективное обследование пациента. Консультация гастроэнтеролога позволяет выявить в анамнезе указания на недавно перенесенный острый панкреатит или обострение хронического, травму живота, а также наличие после них «светлого промежутка». При пальпации живота определяется боль, в некоторых случаях (при крупных псевдокистах) - асимметрия, прощупывание округлого образования.
Результаты лабораторных исследований обычно малоинформативны, поскольку выявляют изменения, причиной которых является первичное заболевание - панкреатит (лейкоцитоз, повышение СОЭ, возможно повышение билирубина и активности щелочной фосфатазы). Характерно изменение уровня панкреатических ферментов: на первой стадии формирования псевдокисты после купирования болевого синдрома определяется гиперферментемия, на более поздних стадиях – гипоферментемия.
При проведении рентгенографии органов брюшной полости возможно обнаружение тени псевдокисты, а также смещения двенадцатиперстной кишки или желудка. Более информативна ультразвуковая диагностика. УЗИ поджелудочной железы позволяет визуализировать ложную кисту, оценить ее локализацию и размеры, в некоторой степени – связь с протоковой системой, а также наличие или отсутствие осложнений (нагноения, кровоизлияния в полость). В случае сдавления холедоха выявляется расширение желчных протоков, при портальной гипертензии – селезеночной и воротной вен. При малигнизации псевдокисты визуализируются неровные контуры ее стенки.
Эзофагогастродуоденоскопия проводится с целью выявления косвенных признаков воспалительного процесса в поджелудочной железе, сдавления желудка и двенадцатиперстной кишки: над участками сдавления определяются эрозии слизистой оболочки, может быть обнаружено варикозное расширение вен пищевода.
Важным методом диагностики панкреатических псевдокист является эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Данный метод исследования позволяет оценить связь полости псевдокисты с протоковой системой, что играет определяющую роль в выборе лечебной тактики. Однако в связи с тем, что существует высокий риск инфицирования полости в ходе исследования, ЭРХПГ проводится исключительно перед хирургическим вмешательством для выбора метода лечения.
Для окончательной верификации диагноза, детальной оценки состояния ложной кисты поджелудочной железы и ее содержимого выполняются такие диагностические исследования, как МРТ поджелудочной железы, цитологическое исследование содержимого кисты. Дифференциальная диагностика проводится с ретенционными кистами, доброкачественными кистомами, злокачественными опухолями поджелудочной железы.

КТ органов брюшной полости. Псевдокиста поджелудочной железы у пациента после приступа острого панкреатита
Лечение ложной кисты поджелудочной железы
На данном этапе фармакотерапия комбинируется с ранним чрескожным пунктированием с установкой катетера. Катетер может находиться в полости псевдокисты до нескольких месяцев, что дает возможность выполнять промывание антисептическими растворами, аспирацию содержимого, а также пломбирование полости силиконовыми быстротвердеющими композициями. До формирования фиброзной капсулы псевдокисты применяется выжидательная тактика, которая обоснована и при бессимптомных ложных кистах поджелудочной железы. При этом активные методы применяются только при появлении клинических симптомов (сдавление соседних органов, боль).
Во втором и последующих периодах формирования псевдокисты ведущим методом лечения является дренирование. В настоящее время в клинической практике более часто применяются эндоскопические малоинвазивные методы, включающие цистогастростомию и цистодуоденостомию. В ходе данных вмешательств выполняется пункция стенки желудка или двенадцатиперстной кишки в области сдавления псевдокистой и установка стента, который может находиться в анастомозе несколько недель. Однако данные методы лечения имеют определенные недостатки: существует риск инфицирования псевдокисты с попаданием химуса в ее полость, раздражения слизистой пищеварительной трубки, кровотечения, а также рубцевания соустья, что приводит к рецидивам.
Хирургическое лечение показано при больших размерах ложных кист поджелудочной железы (более 6-7 сантиметров в диаметре), быстром их увеличении, длительно существующих полостях, большом количестве детрита в полости, а также при травматической этиологии. Также операция проводится при нагноении, перфорации, кровотечении, формировании свищей, неэффективности других методов лечения. Для лечения панкреатических псевдокист выполняется наружное дренирование (вскрытие псевдокисты с вшиванием в рану передней брюшной стенки), внутреннее дренирование (вскрытие кисты, ее ушивание и наложение анастомоза с желудком, двенадцатиперстной или тощей кишкой), удаление кисты (цистэктомия или резекция части панкреас с псевдокистой).
Прогноз и профилактика
Прогноз при ложных кистах поджелудочной железы зависит от причины их развития и выбора оптимального метода лечения в каждом конкретном случае. Послеоперационная летальность при данной патологии очень высокая – около 50%. В то же время рецидивы после различных видов лечения, в том числе эндоскопических, развиваются в 30% случаев. Существует высокий риск таких осложнений, как кровотечение, нагноение, перфорация псевдокисты, формирование свищей, малигнизация. Профилактика панкреатических псевдокист сводится к предупреждению панкреатитов (отказу от употребления алкоголя, рациональному питанию), травм брюшной полости.
Киста поджелудочной железы
Киста поджелудочной железы – ограниченное стенками образование в паренхиме органа, заполненное жидкостным содержимым, которое развивается вследствие травматического или воспалительного повреждения поджелудочной железы. Симптомы зависят от размеров, локализации и причины формирования кисты и варьируют от ощущения дискомфорта до выраженного болевого синдрома, сдавления соседних органов. Для оценки размеров, расположения кисты, ее связи с протоковым аппаратом и выбора тактики лечения проводится УЗИ, КТ, МРТ поджелудочной железы, ЭРХПГ. Лечение хирургическое: внутреннее или наружное дренирование, реже – резекция части железы с кистой.

Киста поджелудочной железы – патология, распространенность которой в последние годы увеличилась в несколько раз, причем страдают преимущественно лица молодого возраста. Гастроэнтерологи причину этого видят в росте заболеваемости острыми и хроническими панкреатитами различной этиологии (алкогольной, билиарной, травматической). Киста поджелудочной железы является наиболее распространенным осложнением хронического панкреатита (до 80% случаев). Сложность данной патологии заключается в отсутствии единого представления о том, какие именно образования следует относить к панкреатическим кистам, общей классификации, отражающей этиологию и патогенез, а также стандартов оказания медицинской помощи.
Некоторые авторы к кистам поджелудочной железы относят образования, имеющие ограниченные стенки и заполненные панкреатическим соком, другие специалисты считают, что содержимым кисты может быть также некротизированная паренхима органа, кровь, воспалительный экссудат или гной. В любом случае, мнения сходятся в том, что для формирования кисты поджелудочной железы непременно должны быть следующие условия: повреждение паренхимы органа, затруднение оттока панкреатического секрета, а также локальное нарушение микроциркуляции.
Причины
Наиболее частая причина развития кист поджелудочной железы – панкреатиты. Острое воспаление поджелудочной железы осложняется развитием кист в 5-20% случаев, при этом полость обычно формируется на третьей – четвертой неделе заболевания. При хроническом панкреатите постнекротические кисты поджелудочной железы образуются в 40-75% случаев. Чаще всего основным этиологическим фактором является алкогольная болезнь. Реже кисты образуются после травм поджелудочной железы, а также вследствие желчнокаменной болезни с нарушением оттока панкреатического сока, обструктивного хронического панкреатита с нарушением оттока по вирсунгову протоку, опухолей большого дуоденального соска, рубцового стеноза сфинктера Одди.
Формирование кисты поджелудочной железы при панкреатите происходит следующим образом. Повреждение ткани органа сопровождается локальным скоплением нейтрофилов и лимфоцитов, деструктивными процессами и воспалением. При этом область повреждения отграничена от окружающей паренхимы. В ней происходит разрастание соединительной ткани, формируются грануляции; тканевые элементы внутри очага постепенно разрушаются иммунными клетками, и на этом месте остается полость. Если киста поджелудочной железы сообщается с протоковой системой органа, в ней накапливается панкреатический сок, также возможно скопление тканевых некротических элементов, воспалительного экссудата, а при повреждении сосудов – крови.
При нарушении пассажа по общему панкреатическому протоку формируются кисты поджелудочной железы, имеющие эпителиальную выстилку, внутри которых накапливается панкреатический сок. Ключевым патогенетическим механизмом их образования является внутрипротоковая гипертензия. Доказано, что внутри полости кисты давление может в три раза превышать нормальные показатели внутри протоков.
Классификация
Условно все кисты поджелудочной железы по морфологическим признакам подразделяют на два типа: сформированные вследствие воспалительного процесса и не имеющие эпителиальной выстилки (некоторые авторы называют такие образования псевдокистами, другие не выделяют в отдельную группу) и образованные при обструкции протоков и имеющие эпителий (ретенционные).
Для характеристики кист поджелудочной железы, образовавшихся как осложнение острого панкреатита, наиболее часто используется Атлантская классификация, согласно которой выделяют острые, подострые жидкостные образования и абсцесс поджелудочной железы. Остро развившиеся образования не имеют окончательно сформированных собственных стенок, в их роли могут выступать как паренхима железы, так и протоки, парапанкреатическая клетчатка, даже стенки соседних органов. Хронические кисты поджелудочной железы характеризуются уже сформировавшимися из фиброзной и грануляционной ткани стенками. Абсцесс – это заполненная гноем полость, образовавшаяся при панкреонекрозе или нагноении кисты.
В зависимости от локализации различают кисты головки, тела и хвоста поджелудочной железы. Выделяют также неосложненные и осложненные (перфорацией, нагноением, свищами, кровотечением, перитонитом, малигнизацией) панкреатические кисты.
Симптомы кисты поджелудочной железы
Клиническая картина при наличии кисты поджелудочной железы может существенно отличаться в зависимости от размера, расположения образования, причины его формирования. Довольно часто панкреатические кисты не вызывают симптоматики: полости диаметром до 5 сантиметров не сдавливают соседние органы, нервные сплетения, поэтому пациенты не испытывают дискомфорта. При крупных кистах основным признаком является болевой синдром. Характерный симптом - «светлый промежуток» (временное улучшение клинической картины после острого панкреатита или травмы).
Наиболее интенсивная боль наблюдается в период формирования псевдокисты при остром панкреатите или обострении хронического, поскольку имеют место выраженные деструктивные явления. Со временем интенсивность болевого синдрома снижается, боль становится тупой, может остаться только ощущение дискомфорта, которое в сочетании с анамнестическими данными (перенесенная травма или панкреатит) позволяет заподозрить заболевание. Иногда на фоне такой скудной симптоматики развиваются болевые приступы, причиной которых является внутрипротоковая гипертензия. Резкая выраженная боль может свидетельствовать также о разрыве кисты, постепенное усиление боли на фоне повышения температуры тела и явлений интоксикации – о ее нагноении.
Существенно отличаются симптомы кисты поджелудочной железы, если она сдавливает солнечное сплетение. При этом пациенты испытывают постоянную выраженную жгучую боль, иррадиирующую в спину, которая может усиливаться даже от сдавления одеждой. Состояние облегчается в коленно-локтевом положении, боль купируется только наркотическими анальгетиками.
Симптомами кисты поджелудочной железы могут быть и диспепсические явления: тошнота, иногда – рвота (ею может заканчиваться приступ боли), неустойчивость стула. В результате снижения экзокринной функции органа нарушается всасывание в кишечнике питательных веществ, снижается вес.
Для данной патологии характерен синдром сдавления соседних органов: если киста находится в области головки железы - возможна механическая желтуха (иктеричность кожи и склер, кожный зуд); при сдавлении воротной вены развиваются отеки на нижних конечностях; если образование нарушает отток мочи по мочеточникам, характерна задержка мочеиспускания. Редко крупные панкреатические кисты сдавливают просвет кишечника, в таких случаях может развиться неполная кишечная непроходимость.
Диагностика кисты поджелудочной железы
Консультация гастроэнтеролога при подозрении на панкреатическую кисту позволяет выявить характерные жалобы пациента, анамнестические данные. При осмотре живота возможна его асимметрия – выпячивание в области расположения образования. При проведении лабораторных анализов обычно специфических изменений нет, возможен незначительный лейкоцитоз, увеличение СОЭ, в некоторых случаях – повышение уровня билирубина и активности щелочной фосфатазы. Концентрация ферментов поджелудочной железы зависит не столько от наличия кисты, сколько от стадии панкреатита и степени повреждения железы. Примерно в 5% случаев нарушается эндокринная функция панкреас и развивается вторичный сахарный диабет.
Высокоинформативны инструментальные методы визуализации кисты. УЗИ поджелудочной железы позволяет оценить размеры образования, а также косвенные признаки осложнений: в случае нагноения определяется неравномерность эхосигнала на фоне полости, при малигнизации – неоднородность контуров. Компьютерная томография и магнитно-резонансная томография (МРТ поджелудочной железы) дают более детальную информацию о размерах, расположении кисты, наличии ее связи с протоками. В качестве вспомогательного метода может применяться сцинтиграфия, при которой киста определяется как «холодная зона» на фоне общей паренхимы органа.
Особое место в диагностике кисты поджелудочной железы отводится эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ). Данная методика дает детальную информацию о связи кисты с протоками железы, что определяет тактику лечения, однако при проведении обследования существует высокий риск инфицирования. Поэтому в настоящее время ЭРХПГ проводится исключительно при решенном вопросе о хирургическом лечении с целью выбора способа операции.
Лечение кисты поджелудочной железы
Лечение кисты поджелудочной железы хирургическое. Не существует единой тактики ведения пациентов с этим заболеванием, и выбор операции зависит от причин формировании кисты, ее размеров, морфофункциональных изменений ткани органа, а также состояния протоковой системы.
Специалисты в области хирургической гастроэнтерологии выделяют три основных направления тактики при кисте поджелудочной железы: ее удаление, внутреннее и наружное дренирование. Удаление образования производится путем резекции части поджелудочной железы вместе с кистой, при этом объем определяется размерами кисты и состоянием паренхимы органа (может быть выполнена резекция головки железы, дистальная, панкреатодуоденальная резекция).
Внутренние дренирующие вмешательства могут проводиться путем наложения анастомоза между кистой и желудком (цистогастростомия), двенадцатиперстной (цистодуоденостомия) или тонкой кишкой (цистоэнтеростомия). Данные методы считаются наиболее физиологичными: они обеспечивают пассаж панкреатического секрета, устраняют болевой синдром, редко приводят к рецидивам.
Наружное дренирование кисты применяется реже. Такое вмешательство показано при нагноении полости, несформировавшихся кистах, обильной васкуляризации образования, а также тяжелом общем состоянии пациента. Подобные операции являются паллиативными, поскольку существует риск нагноения и рецидивирования кисты, формирования панкреатических свищей, которые очень плохо поддаются консервативному лечению и иногда требуют проведения технически намного более сложных вмешательств. Любой вид дренирующих операций проводится только после подтверждения неопухолевой этиологии образования.
В последнее время все большую распространенность приобретают малоинвазивные дренирующие оперативные вмешательства, которые используются как альтернативное лечение. Однако, несмотря на малую инвазивность и теоретическую перспективность таких методов лечения, очень часто развиваются осложнения в виде формирования наружных панкреатических свищей, сепсиса.
Консервативная терапия при кисте поджелудочной железы определяется основным заболеванием. В случае панкреатита обязательно назначается диета, направленная на максимальное снижение панкреатической секреции. Применяются замещающие препараты, анальгетики, проводится контроль уровня гликемии, при необходимости – ее коррекция.
Прогноз и профилактика кисты поджелудочной железы
Прогноз при кисте поджелудочной железы зависит от причины заболевания, своевременности диагностики и хирургического лечения. Данная патология характеризуется высокой частотой осложнений – от 10 до 52% всех случаев сопровождаются нагноением, перфорацией, образованием свищей, озлокачествлением или внутрибрюшным кровотечением. Даже после хирургического лечения существует риск рецидивирования. Профилактика кист поджелудочной железы заключается в отказе от алкоголя, своевременном адекватном лечении заболеваний желудочно-кишечного тракта (ЖКБ, панкреатитов), рациональном питании.
Абсцесс поджелудочной железы
Абсцесс поджелудочной железы – это полость, заполненная гноем и некротическими массами в ткани железы. В подавляющем большинстве случаев развивается после острого алкогольного панкреатита. Характеризуется появлением лихорадки, опоясывающих болей, лейкоцитоза, опухолевидного образования в брюшной полости примерно через две недели после приступа панкреатита. Диагноз устанавливается после проведения УЗИ, МРТ или КТ брюшной полости, анализа биохимических и общеклинических параметров крови. Единственный эффективный метод лечения – хирургическая санация абсцесса с последующей антибактериальной терапией.



Абсцесс поджелудочной железы – тяжелейшее заболевание, которое развивается у пациентов, перенесших панкреатит (остро или повторное обострение) или панкреонекроз с формированием в железе отграниченной гнойной полости. Заболевание опасно для жизни пациента, а коварство его кроется в стёртости клиники на фоне антибиотикотерапии. Именно поэтому в современной гастроэнтерологии принято назначать антибиотики при панкреатите только при сопутствующем поражении желчных путей или доказанных бактериальных осложнениях. Все случаи повышения температуры и появления болей в животе в течение двух недель после панкреатита должны рассматриваться как вероятный панкреатический абсцесс. Единственный метод лечения, приводящий к выздоровлению – хирургическая операция по дренированию гнойника. Без операции летальность при данной патологии достигает 100%.

Абсцесс поджелудочной железы развивается на фоне острого панкреатита, может образовываться при любой форме патологии, кроме отёчной; 3-4% случаев этого заболевания заканчиваются образованием абсцесса. Наиболее часто выявляется на фоне алкогольного панкреатита. Причины формирования гнойной полости в поджелудочной железе до конца не ясны. Предполагается, что инфекция может быть занесена током крови, при проколе псевдокист (если не соблюдается асептика), при формировании свища кисты с кишечником. Развитию абсцесса способствуют:
- тяжёлый панкреатит с более чем тремя факторами риска;
- послеоперационный панкреатит;
- ранняя лапаротомия;
- раннее начало энтерального питания;
- нерациональная антибиотикотерапия.
В подавляющем большинстве случаев при аспирации и посеве содержимого гнойника выделяется кишечная палочка либо энтеробактерии. Согласно исследованиям в области гастроэнтерологии, присоединение вторичной инфекции наблюдается практически в 60% случаев панкреонекроза, поэтому при лечении этого заболевания следует учитывать вероятность образования полости с гнойным содержимым.
Патогенез
При возникновении острого панкреатита ткань железы повреждается, из-за чего ферменты попадают и на саму железу, и на окружающие ткани, разрушая их. Из-за этого может начаться панкреонекроз, образуются псевдокисты – полости, заполненные жидким содержимым и некротизированными тканями. При попадании в область патологического процесса инфекции развивается либо флегмона поджелудочной железы – тотальное гнойное расплавление, либо формируется абсцесс. Следует отметить, что флегмона является более тяжёлым и прогностически неблагоприятным состоянием, по клинике практически не отличающимся от единичного абсцесса. Кроме того, при флегмоне в тканях могут формироваться множественные абсцессы.
Симптомы абсцесса
Абсцесс поджелудочной железы формируется длительно – обычно не менее 10-15 дней. Таким образом, в течение двух-четырёх недель от начала панкреатита повышается температура до фебрильных цифр, появляются озноб, тахикардия, усиливаются боли в верхней половине живота. Боли носят опоясывающий характер, достаточно сильные. Больной обращает внимание на слабость, утомляемость, отсутствие аппетита, повышенное потоотделение. Беспокоит тошнота, рвота, после которой во рту долго ощущается горечь. Налицо все признаки интоксикации. При пальпации живота обращает на себя внимание наличие опухолевидного образования, напряжение мышц передней брюшной стенки.
Осложнения
Абсцесс поджелудочной железы часто осложняется дальнейшим распространением инфекции, образованием множественных гнойников в самой железе и окружающих органах. Гной может затекать забрюшинно, прорываться в полые органы (кишечник, желудок), поддиафрагмально и в околокишечную клетчатку, плевральную и перикардиальную полости, в связи с чем могут сформироваться абсцесс кишечника, поддиафрагмальный абсцесс, гнойный плеврит и перикардит. Также гнойник изредка может прорываться наружу через кожу с образованием свища. При разрушении ферментами стенки сосуда может возникнуть сильное кровотечение, иногда с летальным исходом.
Диагностика
Диагноз абсцесс поджелудочной железы устанавливается специалистом в сфере общей хирургии после тщательного обследования больного. Дифференциальный диагноз проводится с псевдокистой поджелудочной железы, панкреонекрозом. Применяются следующие методы:
- Лабораторные исследования. В общем анализе крови отмечается высокий лейкоцитоз, сдвиг формулы лейкоцитов влево, повышение СОЭ, анемия. В биохимическом анализе крови обращает на себя внимание повышение уровня панкреатических ферментов, гипергликемия. Повышен уровень амилазы мочи, хотя при формировании абсцесса её количество может постепенно снижаться.
- Визуализирующие методики. УЗИ поджелудочной железы, КТ органов брюшной полости позволит определиться с локализацией и размерами очага, количеством абсцессов. При необходимости возможно одновременное проведение чрескожной пункции с аспирацией, исследованием и посевом содержимого.

УЗИ поджелудочной железы. На фоне резкого увеличения размеров железы (обведена пунктиром) в ее головке определяется крупный (до 3 см в диаметре) абсцесс (показан стрелками).
Рентгенологическое исследование панкреатического абсцесса имеет некоторые особенности. Так как железа расположена за желудком, то тень полости гнойника может накладываться на газовый пузырь желудка. Поэтому экспозиция должна быть дольше, а при подозрении на абсцесс в полость желудка вводят контрастное вещество и делают вертикальный снимок в боковой проекции – при этом округлая тень с границей жидкости (абсцесс) будет находиться за желудком. При попадании контраста в полость абсцесса можно говорить о наличии свища. Также на снимках можно увидеть признаки сдавления кишечника, смещения органов. Левый диафрагмальный купол высокий, подвижность его ограничена, может быть выпот в плевральную полость.

КТ органов брюшной полости. Диффузно увеличенная поджелудочная железа. Большая стрелка указывает на тело поджелудочной железы, маленькие стрелки - на абсцесс, расположенный в хвосте поджелудочной железы.
Лечение абсцесса поджелудочной железы
Лечение осуществляет абдоминальный хирург. Абсцесс является абсолютным показанием к санации и дренированию. Практика показывает, что чрескожное дренирование гнойников приводит к излечению только в 40% случаев, к тому же при такой тактике можно пропустить флегмону, множественные абсцессы, распространение инфекции на окружающие панкреас ткани. Именно поэтому эндоскопическое или классическое лапаротомное иссечение и дренирование абсцесса будет наилучшим выходом.
Во время операции производится внимательный осмотр окружающих органов, забрюшинной клетчатки на предмет вторичных абсцессов. Параллельно пациенту назначается антибиотикотерапия согласно полученным посевам, обезболивающие препараты, спазмолитики, ингибиторы ферментов. Проводится инфузионная терапия с целью дезинтоксикации.

Поскольку причины образования абсцессов поджелудочной железы до конца не выяснены, на сегодняшний день не существует и мер профилактики развития этой патологии после панкреатита и панкреонекроза. Таким образом, профилактикой абсцедирования является предупреждение панкреатита – ведь абсцесс может сформироваться только на его фоне.
Прогноз при формировании абсцессов серьёзный: без хирургического лечения смертность составляет 100%, после проведения операции выживаемость достигает 40-60%. Исход заболевания зависит от своевременности обращения, быстрой диагностики и оперативного лечения. Чем раньше поставлен диагноз и проведена операция, тем лучше отдалённые результаты.
Ложная киста поджелудочной железы (K86.3)
Псевдокиста - локализованное скопление жидкости, состоящее из некротизированных тканей, крови, ферментов поджелудочной железы.
Псевдокисты часто связаны с протоком поджелудочной железы; лежат вне сосудов; не содержат эпителиальной выстилки (в отличие от истинных кист) и окружены фиброзной и грануляционной тканью. Чаще всего псевдокисты расположены в теле или головке поджелудочной железы.
Период протекания
Образуется спустя 1-4 недель после начала острого панкреатита.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, "Атакент"
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Общепринятая классификация отсутствует.
При описании используются следующие параметры:
1. Локализация:
- в головке пожелудочной железы (15%);
- в теле и хвосте (85%).
2. Число:
- единичная;
- множественные.
3. Размер:
- малые;
- большие ;
- гигантские.
4. Осложнения (см. соответствующем разделе).
Этиология и патогенез
Клиническая картина
Cимптомы, течение
Следует предполагать наличие псевдокист при наличии следующих проявлений:
1. Факт наличия диагноза панкреатита.
3. Компьютерная топография более чувствительна по сравнению с УЗИ. КТ позволяет проводить дифференциальную диагностику псевдокист. Кроме этого возможна пункция и дренирование псевдокист под контролем КТ.
4. Магнитно-резонансная томография. Данных о применении МРТ в диагностике псевдокист мало, но они позволяют отнести метод к необходимым в ряде случаев острого панкреатита. Преимущество МРТ по сравнению с МДКТ (мультидетекторной компьютерной томографией) при оценке перипанкреатических жидкостных скоплений является то, что твердые включения могут быть более легко оценены именно с помощью МРТ. Это может помочь отличить вызванные панкреатитом накопления жидкости от других кистозных поражений, а также выбрать методы дренирования, которые будет использоваться. Еще одним преимуществом МРТ является то, что при этой методике не используется ионизирующее излучение.
При контрастировании использование Т2-взвешенных последовательностей может быть очень полезным в оценке поджелудочной железы, а также при наличии жидкости внутри паренхимы поджелудочной железы (данный факт позволяет предположить некроз).
Таким образом, МРТ предлагает диагностические возможности похожие на МдКТ, но с лучшим изображением камней и системы поджелудочных и желчных протоков.
К недостаткам МРТ можно отнести ее недоступность.
Лабораторная диагностика
1. Определение активности амилазы в динамике.
Обычно активность амилазы повышается через 2-12 часов после развития клинических проявлений и постепенно снижается спустя 3-5 суток. Стойкое повышение ее активности при разрешении острого панкреатита свидетельствует о наличии псевдокисты.
Повышение амилазы также может быть обусловлено другими поражениями. Например, заболеваниями слюнных желез, легких, фаллопиевых труб, желчного пузыря, тонкого кишечника, некоторых кист яичников; при опухолях легких, толстой кишки, яичников.
Повышение амилазы и липазы может развиваться в отсутствие клинических признаков острого панкреатита. К примеру, при всех заболеваниях, сопровождающихся повреждением стенки тонкой кишки (перфорация, инфаркт, непроходимость) или нарушением выведения ферментов с мочой (почечная недостаточность).
Макроамилаземия отмечается в случае соединения амилазы с IgA. Такие комплексы имеют крупный размер и не фильтруются почками, накапливаясь в крови. Таким образом, активность амилазы в крови остается высокой, а в моче - низкой. Также низким остается показатель клиренса амилазы относительно клиренса креатинина.
2. Лабораторной диагностике также подвергается жидкость, полученная при пункции псевдокисты. Определяются содержание белка, клеточных элементов (в т.ч. атипичных), проводится бакпосев.
Дифференциальный диагноз
1. Вторичные инфекции -10%. Визуализируются КТ по наличию пузырьков газа в полости псевдокисты в 30-40% случаев.
2. Разрыв -3 %. Имеет различные клинические проявления. Может протекать с клиникой острого живота. Встречаются также случаи безсимптомного вначале асцита или плеврального выпота.
3. Панкреатический асцит. Источник жидкости псевокиста в 70%, проток поджелудочной железы в 10-20%. Прилабораторном исследовании асцитической жидкости в ней обнаруживается большое количество амилазы и белка.
4. Свищи в основном являются следствием черезкожного дренирования псевдокисты. Как правило закрываются самостоятельно. При значительном отделяемом может понадобиться хирургическое вмешательство.
5. Обьструкция псевдокистой различных отделов ЖКТ, нижней полой вены, мочевых путей. Требуется экстренная операция.
6. Желтуха - 10%. Обусловлена обструкцией внепеченочных желчных путей, стенозом общего желчного протока, желчекаменной болезнью.
7. Псевдоаневризма -10%. Развивается вследствие кровоизлияния в псевдокисту, если она эррозирует сосуды собственной капсулы или прилежащие сосуды. Визуально псевдокиста резко увеличивается в размерах, появляются или усиливаются боли, появляются кровопотёдки на коже в области локализации псевдокисты, появляются клинические и лабораторные признаки кровотечения. Если псевдокиста соединяется с протоком поджелудочной железы, то кровотечение в него приводит к массивному желудочно-кишечному кровотечению с кровавой рвотой и/или меленой. При разрыве псевдоаневризмы развивается кровотечение в брюшную полость.
Лечение
Медикаментозное
1. Назначение окреотида при образовании свища (вопрос остается дискутабельным).
2. Восполнение объема циркулирующей крови и внутрисосудистой жидкости при кровотечениях.
Хирургическое
1. Чрескожное дренирование через катетер.
Показания:
- пациенты низкой группы риска (шкалы APACHE, GLSGO);
- незрелость псевдокисты;
- инфицирование псевдокисты;
- предшествующая четкая визуализация анатомических особенностей протоков с применением эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) или магнитно-резонансной холангиопанкреатографии (МРХПГ).
2. Эндоскопическое дренирование.
Показания:
- псевдокисты небольшого размера;
- локализация псевдокисты в головке поджелудочной железы.
3. Хирургичекое дренирование.
Показания:
- неэффективность чрескожного и эндоскопического дренирования;
- множественные псевдокисты;
- гигантские псевдокисты;
- другие осложнения острого панкреатита;
- подозрение на опухоль.
Показания: при панкреатическом асците .
Дренирование жидкостных образований, не оформившихся в кисту, обязательно не всегда. Подобные жидкостные скопления образуются более чем в половине случаев острого панкреатита с тяжестью выше средней. В большинстве случаев (65%) выпот рассасывается в течение 6 недель. Выпот, как правило, не связан с протоками поджелудочной железы, поэтому концентрация ферментов в нем относительно низкая.
Если образование (неоформленная псевдокиста) сохраняется более 6 недель и вызывает клинические проявления (боль, желтуху, температуру и прочие) следует подумать об осложнениях (обструкция, инфицирование) и выбирать тактику как при сформировавшейся псевдокисте.
Читайте также:
