Методы лучевого обследования надпочечников
Обновлено: 17.05.2024
Методы лучевого обследования надпочечников
а) Анатомия, эмбриология и физиология. Надпочечники расположены в околопочечном пространстве, обычно краниально по отношению к почкам. Правый надпочечник расположен над почкой, латерально по отношению к ножкам диафрагмы, медиальнее печени и прилежит к задней поверхности нижней полой вены (НПВ). Левый надпочечник, как правило, находится спереди от верхнего полюса левой почки и позади селезеночной вены и поджелудочной железы.
Селезеночная вена - важный ориентир при определении происхождения опухоли в левом верхнем квадранте, место происхождения которой может быть неизвестно. Опухоли надпочечника обычно смещают селезеночную вену кпереди, в то время как опухоли желудка и поджелудочной железы смещают ее кзади.
Кора и мозговое вещество надпочечников-по существу разные органы, расположенные в одном структурном образовании. Кора надпочечников представляет собой эндокринную железу, секретирующую преимущественно кортизол, альдостерон и андрогенные стероиды; все они образуются из эфиров холестерина. Это способствует высокому содержанию липидов, что служит характерным признаком большинства аденом коры надпочечников. Мозговое вещество надпочечника-производное нервного гребня, секретирует адреналин и норадреналин.
Физиологию надпочечников контролируют сложные взаимодействия между гипоталамусом, гипофизом и надпочечниками. Стресс приводит к высвобождению адреналина и цитокинов, что вызывает выделение адренокортикотропного гормона (АКТГ) гипофизом, который, в свою очередь, стимулирует секрецию кортизола надпочечниками. Кортизол и адреналин часто рассматривают в качестве «гормонов стресса». Повышение уровня кортизола в сыворотке крови оказывает подавляющее действие на гипоталамус и гипофиз, вызывая снижение высвобождения АКТГ
Синдром Кушинга, возникающий вследствие избытка кортизола, характеризуется ожирением в верхней части туловища, гирсутизмом, аменореей, артериальной гипертензией, слабостью и стриями на брюшной стенке. Это состояние обусловлено гиперплазией надпочечников (75-80% случаев), но также может возникать вследствие аденомы надпочечника (20-25% случаев), рака надпочечников (менее 5% случаев) или экзогенной терапии глюкокортикоидами.
Синдром Конна - эпоним, который иногда используют для обозначения повышения уровня альдостерона, характеризуется артериальной гипертензией, гипокалиемией, алкалозом, мышечной слабостью и сердечной недостаточностью. В отличие от синдрома Кушинга, синдром Конна обычно возникает вследствие аденомы надпочечника (65-70% случаев). На гиперплазию надпочечников приходится большая часть оставшихся (25-30%) случаев, в то время как рак надпочечников является редкой причиной.
Поскольку у пациентов с синдромом Кушинга имеются клинические проявления, уровень поражения (гипофиз или надпочечники), как правило, устанавливают по биохимическим данным до визуализации. С помощью визуализации (МРТ или КТ), проведенной после постановки диагноза, обычно без труда выявляют аденому гипофиза или надпочечника, вызвавшую развитие синдрома Кушинга, что, как правило, позволяет избежать выполнение катетерной ангиографии или других инвазивных исследований. Однако аденома при синдроме Конна может быть весьма небольшой, и определение источника повышенного синтеза альдостерона, при использовании традиционных методов визуализации, может стать проблематичным
Болезнь (синдром) Аддисона представляется собой надпочечниковую недостаточность и характеризуется артериальной гипотензией, потерей веса, гиперпигментацией. Среди причин «медленного возникновения» надпочечниковой недостаточности аутоиммунные заболевания составляют самую частую причину в развитых странах. Туберкулез и другие инфекции - частые причины развития синдрома Аддисона в развивающихся странах, в то время как метастатическую болезнь и СПИД встречают во всех популяциях.
Наиболее частая причина внезапного развития надпочечниковой недостаточности - кровоизлияние в надпочечники, которое может возникнуть вследствие сепсиса, шока, повышенной антикоагуляционной активности или васкулитов. Резкая отмена глюкокортикоидов и послеродовой некроз гипофиза, также известный как синдром Шихана, также могут привести к острой надпочечниковой недостаточности. В этих случаях необходимы незамедлительная диагностика и лечение данных состояний.
(Слева) На рисунке показана типичная анатомия надпочечников. Обратите внимание на множественные источники кровоснабжения. Венозный отток от правого надпочечника осуществляется через надпочечниковую вену непосредственно в НПВ, в то время как левая надпочечниковая вена впадает в почечную вену.
(Справа) Правый надпочечник прилежит к НПВ, расположен латеральнее правой диафрагмальной ножки и медиальнее печени. Левый надпочечник обычно расположен вентрально по отношению к верхнему полюсу левой почки и позади селезеночной вены. Левый надпочечник выглядит в виде перевернутой «Y», а правый больше напоминает перевернутую «V». (Слева) На рисунке показана стимуляция передней доли гипофиза адреналином и цитокинами, гормонами гипоталамуса — кортиколиберин-рилизинг-гормоном (КРГ) или антидиуретическим гормоном (АДГ). Это приводит к высвобождению АКТГ, что вызывает секрецию кортизола надпочечниками. Избыточный уровень циркулирующего кортизола в крови ингибирует дальнейшую гипофизарную секрецию.
(Справа) Бесконтрастная КТ, аксиальная проекция: визуализировано случайно выявленное гиподенсное образование правого надпочечника с плотностью менее 10 HU. Этот признак имеет специфичность более 90% для диагностики аденом с высоким содержанием жира.
б) Методы и протоколы визуализации:
1. КТ-протокол для визуализации надпочечников. Проведение бесконтрастной КТ часто бывает достаточным для диагностики аденомы коры надпочечников, которая выглядит в виде узелка гомогенной низкой плотности (менее 10 HU). Если патологический очаг не определяют или выявляют только при контрастном исследовании, определяют контрастирование образования, а затем повторно выполняют серию тонких срезов через надпочечники и измеряют относительную или абсолютную задержку вымывания контраста.
2. MPT-протокол для визуализации надпочечников. Аденома надпочечника с высоким содержанием жира может быть выявлена с помощью Т1 -ВИ в последовательности градиентного эха, которая включает как синфазное, так и противофазное построение изображения. Потеря сигнала от образования надпочечника на противофазном изображении по существу служит диагностическим критерием аденомы. Аденомы с низким содержанием жира можно не определить на МРТ, они лучше всего могут быть оценены с помощью КТ-протокола для визуализации надпочечников.
в) Тактика при опухоли надпочечника:
1. Это аденома? Аденомы надпочечника встречают крайне часто, несмотря на то, что большинство из них-«нефункционирующие» (точнее-«без гиперфункции»). По оценкам, около 2% общей популяции имеет аденому надпочечника, что делает ее самой распространенной причиной образования надпочечника, даже у пациентов с выявленной вненадпочечниковой злокачественной опухолью.
Высокая распространенность аденом надпочечников в общей популяции, а также крупномасштабные исследования, показавшие, что подавляющее большинство «инциденталом» надпочечника служит доброкачественными находками и не имеет клинического значения, побудили некоторых авторов предложить гораздо более консервативный подход к случайно выявленным образованиям надпочечников малых размеров. Однако большинство профессиональных обществ продолжает выступать за визуализацию и агрессивную клиническую тактику при случайно выявленных на КТ-образованиях надпочечника.
Большинство аденом содержит большое количество внутриклеточного и внеклеточного жира, который обусловливает характерное проявление в виде гомогенной плотности, близкой к водной (от -5 до +10 HU) на бесконтрастной КТ. Аденомы, содержащие большое количество жира, имеют такие же характерные признаки и на МРТ. Лучший метод визуализации для меньшей части аденом надпочечника, содержащих низкое количество жира, - «надпочечниковый протокол» КТ. Аденомы отличаются от метастазов и большинства других опухолей надпочечника характерным симптомом «вымывания» контраста - быстрое возвращение к исходному уровню контрастирования после внутривенного введения контрастного вещества.
2. Это не аденома, тогда что это? Несмотря на то, что остальные опухоли надпочечника могут иметь схожие признаки, поставить точный диагноз нетрудно, принимая во внимание визуальные признаки образования, клинические и лабораторные данные конкретного пациента.
Причинами гетерогенного образования надпочечника больших размеров могут быть как феохромоцитома, так и метастазы. Однако корреляция с анамнезом заболевания, данные лабораторного эндокринологического исследования и физикального обследования, как правило, позволяют избежать расширенной или дорогостоящей дополнительной визуальной оценки.
(Слева) При образованиях надпочечника, не идентифицированных (более 70 HU) на бесконтрасной КТ, может быть выполнена оценка процента вымывания контраста на КТ надпочечников для выявления скрытых аденом с низким содержанием жира. На рисунке изображена формула определения процента вымывания контраста на КТ. Для расчета доступны веб-калькуляторы.
(Справа) Показан КТ-протокол для визуализации надпочечников. На бесконтрастной КТ (А) выявлено образование надпочечника с плотностью 30 HU. На КТ с контрастированием (Б) образование имеет плотность 60 HU, на отсроченной КТ (В) — 40 HU. Абсолютный процент вымывания контраста, составляющий 67%, служит характерным признаком аденомы с низким содержанием жира. (Слева) Схема алгоритма визуализации случайно выявленных образований надпочечника. Большое значение имеют история заболевания и предшествующие исследования. Большинство образований надпочечника-доброкачественные, однако диагностика может иметь решающее значение у пациентов с онкологическими заболеваниями. К/Н -контрольное наблюдение.
(Справа) Оценка повышения уровня кортизола или адреналина также служит определяющим фактором в диагностике образований надпочечники. (Слева) На синфазном Т1-ВИ в последовательности градиентного эха у пациента с двусторонними узелками или опухолями небольших размеров в надпочечниках достоверно выявлен узел только в левом надпочечнике.
(Справа) На Т1-ВИ в последовательности градиентного эха у этого же пациента выявлено выпадение сигнала от узелков в надпочечнике, что указывает на сочетание липидов и протонов воды. Это служит характерным признаком аденомы с высоким содержанием липидов.
3. Все ли опухоли надпочечника, содержащие жир, — аденомы? Аденомы редко содержат макроскопический жир. Липиды в аденомах надпочечников представлены микроскопическим жиром, а наличие макроскопических отложений жира характерно для менее распространенного новообразования надпочечника-миелолипомы (не путать с почечной ангиомиолипомой, отличающейся во всех отношениях). Миелолипома - редкая доброкачественная опухоль надпочечника, которая, как правило, может быть точно диагностирована на КТ или МРТ при наличии отложений зрелой жировой ткани с наличием или без кальцификатов или мягкотканных элементов.
4. Какой метод визуализации следует использовать при подозрении на феохромоцитому? Перед применением дорогостоящих методов визуализации рекомендовано уточнить анамнез заболевания, провести физикальное обследование, а также соответствующее биохимическое исследование. Это позволяет определить отсутствие или наличие данной опухоли у большинства пациентов.
С помощью КТ или М РТ легко выявить большинство симптоматических феохромоцитом, так как их диаметр, как правило, составляет 3-5 см. Часто в связи с большими размерами опухоли нет необходимости в исследовании с контрастным усилением. Однако при необходимости его следует проводить, поскольку данные о неблагоприятных эффектах внутривенного введения неионного контраста у пациентов с феохромоцитомой отсутствуют.
5. Какой метод визуализации следует использовать при подозрении на метастазы в надпочечниках? Надпочечники - частая локализация метастазов (и лимфомы), однако редко это единственная локализация. Следует помнить, что изолированное поражение надпочечников небольших размеров, скорее всего, представляет собой аденому надпочечника, особенно, если оно имеет гомогенную низкую плотность.
ПЭТ/КТ чаще используют для установления стадии заболевания у пациентов с раком и лимфомой, а большинство метастазов в над-почечниках-ФДГ-положительные. Стоимость ПЭТ/КТ обусловливает целесообразность применения данного метода для оценки стадии подтвержденного рака, а не для последующей оценки поражения надпочечников, выявленного другими методами визуализации.
(Слева) КТ с контрастированием, аксиальная проекция: у пациента с лимфомой надпочечников (диссеминированной) выявлено образование левого надпочечника, которое имеет такую же мягкотканную плотность, как и инфильтраты в поджелудочной железе, селезенке и лимфатических узлах.
(Справа) На КТ с контрастированием у пациента с раком пищевода и метастазами в надпочечниках обнаружены гетерогенные дольчатые образования надпочечников с обеих сторон. Перед плановой эзофагэктомией была выполнена ПЭТ/КТ. Это образование оказалось ФДГ-положительным, что привело к отмене запланированной эзофагэктомии. (Слева) МРТ, Т2-ВИ, аксиальная проекция: у пациента с феохромоцитомой выявлена крупная гетерогенная опухоль левого надпочечника, гиперинтенсивная на Т2-ВИ и гипоинтенсивная на Т2-ВИ. Такая картина характерна, но не патогномонична для феохромоцитомы. Диагноз был подтвержден посредством резекции.
(Справа) МРТ, Т2-ВИ, коронарная проекция: у этого же пациента выявлена гетерогенная гиперинтенсивная опухоль, что характерно для феохромоцитомы. (Слева) На рисунке показаны локализации феохромоцитомы (синим) и параганглиомы (зеленым). Обратите внимание на орган Цуккеркандля в области бифуркации аорты.
(Справа) КТ с контрастированием, аксиальная проекция: гиперваскуляризированное образование в области малого таза. Это образование оказалось параганглиомой с клиническим течением, характерным для феохромацитомы.
в) Список использованной литературы:
1. Berland LL et al: Managing incidental findings on abdominal CT: white paper of the ACR incidental findings committee. J Am Coll Radiol. 7(10):754-73, 2010
МЕТОДЫ ЛУЧЕВОЙ ВИЗУАЛИЗАЦИИ В ДИАГНОСТИКЕ ОБЪЕМНЫХ ОБРАЗОВАНИЙ НАДПОЧЕЧНИКОВ (ОБЗОР ЛИТЕРАТУРЫ)
Введение. На данный момент отмечается «эпидемия» инциденталомы надпочечников, частота выявления которой составляет около 7% населения. Под инциденталомой понимают случайно выявленное образования в надпочечниках, не связанное с гормональной активностью. Важную роль в определении природы объемных образований надпочечников и тактику ведения таких больных играют лучевые методы исследования. В последние десятилетия произошел прорыв в диагностике образований надпочечников. Именно комплексная лучевая визуализация в сочетании с УЗИ, КТ, МРТ позволила проводить дооперационную диагностику опухолей надпочечников, определять вид опухоли, устанавливать стадию и распространенность процесса. Несмотря на такое всестороннее изучение методов диагностики, это еще раз показывает актуальность проблемы надпочечников. Не стоит забывать, что при высокой диагностической эффективности современных лучевых методов диагностики опухолей надпочечников для постановки точного диагноза необходимо проведение гормональных исследований. Материалы и методы. В обзоре рассмотрены возможности и ограничения данных методов, представлена их техническая характеристика, рассматривается актуальность применения в научных исследованиях и клинической практике при забрюшинной патологии. Заключение. Проблема дифференциальной диагностики образований надпочечников остается открытой и нуждается в дальнейшем изучении.
Ключевые слова
Об авторах
Федеральное государственное бюджетное образовательное учреждение высшего образования «Башкирский государственный медицинский университет» Министерства здравоохранения Российской Федерации.
Россия
Шингареева Лилия Айратовна – врач-рентгенолог Клиники БГМУ, аспирант кафедры общей хирургии с курсом лучевойдиагностики ФГБОУ ВО БГМУ Минздрава Российской Федерации.
Байков Денис Энверович – доктор медицинских наук, заведующий отделением общей лучевой диагностики Клиники БГМУ, профессор кафедры общей хирургии с курсом лучевой диагностики ФГБОУ ВО БГМУ Минздрава Российской Федерации.
Список литературы
1. Ефимцев АЮ, Мищенко АВ. Практическая ультразвуковая диагностика. Москва; 2016. т. 2. [Efimtsev AYu, Mischenko AV. Practical ultrasound diagnosis. Moscow; 2016. vol. 2. (in Russ.)].
3. Котельникова ЛП, Каменева ОС, Дмитриева АМ. Компьютерная томография в дифференциальной диагностике инциденталом надпочечников. Современные проблемы науки и образования. 2008;(6):129-132. [Kotelnikova LP, Kameneva OS, Dmitrieva AM. Computer tomography in differential diagnosis of incidental adrenal tumors. Modern problems of science and education. 2008;(6):129-132 (in Russ.)].
4. Филимонюк АВ, Смирнова ЕА, Тедорадзе РВ, Смелкова НИ. Особенности диагностики опухолей надпочечника. Вестник Российского университета дружбы народов. Медицина. 2013;(1):77-83. [Filimonyuk AV, Smirnova EA, Tedoradze RV, Smelkova NI. Peculiarities of diagnosis of adrenal tumors. Vestnik Rossiiskogo universiteta druzhby narodov. Seriya: Meditsina=Bulletin of Russian Peoples’ Friendship University. Series Medical. 2013;(1):77-83 (in Russ.)].
5. Дворников МВ. Роль ультразвукового исследования в диагностике инциденталом надпочечников. Пермский медицинский журнал. 2013;30(5):99-103. [Dvornikov MV. Role of ultrasonic investigation in diagnosis of adrenal incidentalomas. Perm medical journal. 2013;30(5):99-103 (in Russ.)].
7. Никитин АД. Алгоритм лучевых методов при диагностике новообразований надпочечников. Бюллетень медицинских интернет конференций. 2014;4(5):582. [Nikitin AD. Algorithm of radial methods in the diagnosis of adrenal neoplasms. Bulletin of Medical Internet Conferences. 2014;4(5):582 (in Russ.)].
8. Руммени ЭЙ, Кармазановский ГК. Магнитно-резонансная томография тела. М.: Медицинская литература; 2014. [Rummeni HE, Karmazanovsky GK. Magnetic resonance imaging of the body. Moscow: Medical literature; 2014. (in Russ.)].
10. Садриев ОН, Гаибов АД, Анварова ШС. Диагностика и хирургическое лечение синдрома Конна. Вестник Авиценны. 2014;(1):47-52. [Sadriev ON, Gaibov AD, Anvarova SS. Diagnosis and surgical treatment of Conn’s syndrome. Bulletin of Avicenna. 2014;(1):47-52 (in Russ.)].
11. Зогот СР, Акберов РФ. Оптимизация лучевых методов исследования в диагностике рака гепатобилиопанкреатодуоденальной зоны. Вестник Чувашского университета. 2013;(3):426-430. [Zogot SR, Akberov RF. Optimization of radiation techniques in the diagnosis of cancer hepatobiliopancreatoduodenal zone. Vestnik Chuvashskogo Universiteta=Bulletin of the Chuvash University. 2013;(3):426-430 (in Russ.)].
12. Бельцевич ДГ. Адренокортиальный рак. Вопросы урологии и андрологии. 2013;2(3):55-61. [Beltsevich DG. Adrenocortial cancer. Voprosy urologii i andrologii=Urology and Andrology. 2013;2(3):55-61 (in Russ.)].
13. Газымов ММ, Шамитов ЮП, Филиппов ДС. Диагностика и лечение больных артериальной гипертонией надпочечникового и почечного генеза. Урология. 2014;(3):5-7. [Gazymov MM, Shamitov UP, Filippov DS. Diagnosis and treatment of patients with secondary arterial hypertension of adrenal and renal genesis. Urologiia=Urology. 2014;(3):5-7. (in Russ.)].
14. Мельниченко ГА, Стилиди ИС, Алексеев БЯ, Горбунова ВА, Бельцевич ДГ, Райхман АО и др. Федеральные клинические рекомендации по диагностике и лечению адренокортикального рака. Проблемы эндокринологии. 2014;60(2):51-67. [Melnichenko GA, Stilidi IS, Alekseev BYa, Gorbunova VA, Beltsevich DG, Raikhman AO, et al. Federal clinical practice guidelines on the diagnostics and treatment of adrenocortical cancer. Problems of endocrinology. 2014;60(2):51-67 (in Russ.)].
15. Ватутин НТ, Калинкина НВ, Столика ОИ, Высоцкая ВО, Ещенко ЕВ. Первичный альдостеронизм (синдром Конна): основные сведения и собственное наблюдение. Украинский кардиологический журнал. 2013;(4):61-65. [Vatutin NT, Kalinkina NV, Stolika OI, Vysotskaya VO, Yeshchenko EV. Primary aldosteronism (Conn syndrome): basic information and original observation. Ukrainian Journal of Cardiology. 2013;(4):61-65 (in Russ.)].
16. Glockner JF, Lee CU. Magnetic resonance imaging of perirenal pathology. Can Assoc Radiol J. 2016;67(2):149-57. DOI:10.1016/j.carj.2015.08.003.
17. Adam SZ, Nikolaidis PS, Horowitz JM, Gabriel HT, Hammond NA, Patel TA. Chemical shift MR imaging of the adrenal gland: principles, pitfalls, and applications. Radiographics. 2016;36(2):414-32. DOI:10.1148/rg.2016150139.
19. Song JH, Mayo-Smith WW. Current status of imaging for adrenal gland tumors. Surg Oncol Clin N Am. 2014;23(4):847-61. DOI:10.1016/j.soc.2014.06.002.
20. Tauchmanova L, Rossi R, Biondi B, Pulcrano M, Nuzzo V, Palmieri EA, et al. Patients with subclinicalCushing’s syndrome due to adrenal adenoma have increased cardiovascular risk. J Clin Endocrinol Metab. 2002;87(11):4872-8. DOI:10.1210/jc.2001-011766.
Возможности лучевых методов исследования в диагностике опухолей надпочечников

Цель исследования: оценка возможности ультразвукового исследования и компьютерной томографии в диагностике и дифференциальной диагностике опухолей надпочечников. В работе анализированы возможности ультразвукового исследования (УЗИ) и компьютерной томографии (КТ) в диагностике различных нозологических форм опухолей надпочечников у 54 пациентов. Как по данным УЗИ, так и по данным КТ большие размеры были характерны феохромоцитоме (ФХЦ) (78,5±5,3 - 75,6±6,3 мм), малые и средние кортикостероме (КС) (45,2±2,6 - 45,6±4,3 мм) и альдостероме (АС) (46,2±7,1 - 45,9±5,4 мм). Адренокортикальным опухолям было характерно в основном округлая или овальная форма, феохромоцитоме в большинстве случаев неправильная округлая форма. Такие морфометрические показатели как неровность контуров, неоднородность структуры и наличие включений в структуре опухоли было характерно в основном феохромоцитоме, тогда как у опухолей коры надпочечников эти признаки практически отсутствовали. Выявлены статистически значимые различия плотности ФХЦ (+24,2±2,3 UH), КС (+13,4±0,3 UH) и АС (+5,1±0,2 UH) в нативном режиме и при контрастировании (ФХЦ - +41,5±6,1 UH; КС - 18,6±0,9 UH; АС - +12,1±0,4 UH), а также разница времени вымывания контраста (при феохромоцитоме 14,7±0,5 мин., при кортикостероме 8,7±0,4 мин. и альдостероме 6,2±0,4 мин.). В связи с малым размером опухоли, при ожирении и метеоризме УЗИ был неинформативен в 3 случаях. Во всех случаях КТ позволила точно определить локализацию опухоли и достоверно дифференцировать различные их нозологические формы. УЗИ и КТ в выявлении и дифференциации опухолей надпочечников показали высокую чувствительность и специфичность, а сопоставление клинических признаков различных опухолей надпочечников с выявленными характерными КТ-признаками позволяют более точно предполагать морфологию опухоли надпочечника и быть клинически значимым в выборе дальнейшей лечебной тактики.
Ключевые слова
Полный текст
Проблема своевременной диагностики опухолей надпочечников (ОН) продолжает оставаться одним из ключевых вопросов современной эндокринной хирургии. Активное внедрение в ежедневную практическую деятельность врачей таких визуализирующих методов исследования как компьютерной (КТ) и магнитно-резонансной (МРТ) томографии, количество выявляемых опухолей надпо чечников значительно возросло [1], в том числе и в Республике Таджикистан [2]. КТ и МРТ с внутривенным контрастированием, несомненно, имеют более высокую чувствительность и специфичность (по сравнению с УЗИ и КТ в нативном режиме) для выявления опухолей надпочечников (97,7%), а при воссоздании трехмерного изображения позволяют более детально уточнить взаимоотноше 108 Российский медико-биологический вестник имени академика И.П. Павлова, № 2, 2016 г. ния опухоли надпочечника с окружающими тканями и крупными сосудами за-брюшинного пространства [2, 3]. Неинвазивность, высокая степень информативности, прямое изображение зон интереса, возможность трёхмерной реконструкции, отсутствие противопоказаний к проведению нативного (без контрастирования) исследования, сделала КТ «золотым стандартом» в диагностике различных патологий надпочечников [4, 5, 6]. Неоспоримым преимуществом её является также возможность оценки плотности любой зоны интереса, то есть распознавания содержимого того или иного образования (КТ-морфометрия) [6]. Однако до настоящего времени публикации, посвящённые вопросам диагностики опухолей надпочечников, где бы отражалась роль и место лучевых методов исследования в их дифференциальной диагностике, являются редкими. Следовательно, вышеизложенный вопрос актуален и требует дальнейшего изучения. Цель исследования. Оценка возможности ультразвукового исследования и компьютерной томографии в диагностике и дифференциальной диагностике опухолей надпочечников. Материалы и методы В основу настоящего исследования положен анализ результатов УЗИ и КТ и их корреляция с результатами гистологических исследований у 54 пациентов с различными нозологическими формами опухолей надпочечников. Феохромоцито-ма (ФХЦ) диагностирована у 23 (42,6%) пациентов, альдостерома (АС) у 18 (33,3%) и кортикостерома (КС) у 13 (24,1%). Среди пациентов лиц женского пола было 35 (64,8%), мужского - 19 (35,2%). Средний возраст больных, составляя 31,6 ± 2,4 лет. Одностороннее опухолевое поражение надпочечников отмечалось в 50 (92,6%) случаях, правосторонняя локализация - у 26 (48,1%) пациентов, левосторонняя - у 24 (44,4%). Двустороннее поражение отмечено у 4 (7,4%) человек (в 3 случаях у пациентов с феохромоцитомой и в одном случае -кортикостеромой). Ультразвуковое исследование проводилось с использованием УЗ аппарата «Alo-ka-SSD-4000» (Япония, 2008) и диагностической ультразвуковой системы DC-3 «Min-dray» (Китай, 2012), снабженной конвекс-ными датчиками частотой 3,5-7,0 Мгц. При помощи УЗИ определяли форму, размеры, капсулу, эхоструктуру выявленного новообразования надпочечника. КТ выполнялась на томографе Somatom Emotion фирмы «Siemens» (Германия, 2011). Ширина шага сканирования составляла 3 -5 мм. Внутривенное контрастное усиление проводилось препаратами Ультравист 270 («Shering», Германия) или Омнипак 350 («Nycomed», Норвегия) со скоростью 3,5-5,0 мл/с после предварительного определения индивидуальной чувствительности и переносимости препаратов, со сканированием в артериальную, портальную и паренхиматозную фазы. При трёхфазном КТ, оценивались такие показатели, как размеры опухоли, структура, нативная плотность и плотность в разных фазах контрастирования, а также время вымывания контраста более чем на 60%. Полученные результаты КТ сравнивались с данными морфологического исследования удалённых опухолей, при этом оценивались её чувствительность и специфичность. Морфологические исследования опухолей надпочечников выполняли в лаборатории морфологии опухолей Республиканского онкологического научного центра Республики Таджикистан (n = 54) и в сомнительных случаях (n = 2) в Российском онкологическом научном центре им. Н.Н. Блохина РАМН Российской Федерации. Микроскопическое и морфометрическое исследования препаратов проводились с помощью микроскопа «Primo Star» фирмы Zells (Германия) снабженной цифровым фотоаппаратом Canon в *10 и *40 кратном увеличении. Данные, полученные в результате исследования, были обработаны с использо 109 Российский медико-биологический вестник имени академика И.П. Павлова, № 2, 2016 г. ванием программы «Statistica 6.0». Применялась параметрическая [среднее (М), стандартное отклонение (g), среднеквадратическая ошибка (m)] и непараметрическая [медиана (Ме), верхний (Q25) и нижний (Q75) квартили] описательная статистика. Достоверность различий между группами определяли с использованием критериев Манна-Уитни и Краскела-Уоллиса. Различия между показателями считали статистически значимыми при p
Рентген надпочечников
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Лучевые методы оказывают существенную помощь клиницисту в распознавании поражений надпочечников. На обзорных рентгенограммах эти железы не видны. Только в тех случаях, когда болезнь Аддисона связана с туберкулезным поражением надпочечников, в последних иногда заметны мелкие отложения извести. В связи с этим наиболее простым методом лучевого исследования является сонография. Отметим лишь, что нормальные или слегка увеличенные надпочечники на сонограммах вырисовываются далеко не всегда.
На компьютерных томограммах надпочечник можно обнаружить как образование, находящееся над верхним полюсом почки и несколько кпереди от него. Нормальная железа обусловливает небольшое образование овальной или треугольной формы с прямыми или выпуклыми контурами. Опухоль приводит к его увеличению и деформации. Компьютерные томограммы позволяют выявлять опухоли диаметром всего 0,5-1,0 см. Еще более чувствительным методом считается МРТ, особенно при констатации гиперплазии коры надпочечников (при сонографии и КТ гиперплазия регистрируется лишь у половины больных). Разработана также сцинтиграфия надпочечников. Ее осуществляют посредством внутривенного введения 99mTc-MIBG. Нормальный надпочечник образует очаг накопления РФП над верхним полюсом почки. Эту методику применяют редко ввиду значительно больших диагностических возможностей КТ и МРТ. Однако она полезна при дифференциации гиперплазии и опухоли надпочечника. При аденоме увеличен один надпочечник, в котором накапливается большое количество РФП, тогда как функция второго подавлена. При нодулярной гиперплазии также увеличен и хорошо концентрирует РФП один надпочечник, а второй имеет небольшие размеры и слабо накапливает РФП.
Нарушение функции надпочечников проявляется различными клиническими синдромами и характеризуется специфическими лабораторными данными (синдром Иценко-Кушинга, синдром Конна - первичный альдостеронизм, симптоматическая гипертензия на почве развития феохромоцитомы). Органической основой синдрома Иценко-Кушинга чаще всего бывает двусторонняя гиперплазия коры надпочечников (преимущественно вследствие возникновения аденомы гипофиза), а синдрома Конна - гиперплазия или опухоль (обычно доброкачественная аденома надпочечника). Соответственно строится тактика лучевого обследования, в которой ведущее место занимает КТ.
Из изложенного ясно, что при синдроме Иценко-Кушинга исследование нужно дополнить рентгенографией, КТ или МРТ области турецкого седла в поисках аденомы гипофиза. Кроме того, при этом синдроме выполняют рентгенографию скелета. В молодом возрасте отмечается замедление роста костей Вследствие нарушения минерального обмена возникает системный остеопороз. Нередки переломы ребер и тел позвонков, а также асептические некрозы костей.
Исследование венозной крови на содержание надпочечниковых гормонов выполняют методом катетеризации надпочечниковых вен трансфеморальным доступом с последующей контрастной венографией и забором образцов крови из этих вен и нижней полой вены. Процедура имеет инвазивный характер и технически сложна, производят ее в ангиографическом кабинете. Тестирование венозной крови - достаточно надежный тест для разграничения одно- и двусторонней гиперплазии и аденомы, а также интра- и экстраадренальной локации феохромоцитомы.
В надпочечниках часто выявляют метастазы рака. Печальное первенство здесь принадлежит раку молочной железы и легких, что надо учитывать при клинико-лучевом обследовании больных.
Лучевая диагностика заболеваний надпочечников

Эхограмма правого надпочечника. Гиперэхогенное образование в области верхнего полюса почки (стрелки)
УЗИ. НП лоцируется со стороны передней, задней и боковой поверхностей. Надпочечники не всегда удается лоцировать (у 1/3, в 70-80%). Для качественной визуализации необходима тщательная подготовка. Корковое вещество имеет эхогенность как у печени, мозговое – гипоэхогенно. Структура мелкозернистая.

Магнитно-резонансная томограмма Т1-режим – срез на уровне надочечников. Левый надпочечник указан стрелкой.
МРТ. Характеристика размеров НП идентична РКТ исследованию. Характеристики МР-сигнала нормального надпочечника: T1 – слабо гипоинтенсивный по отношению к печени, T1 с подавлением жира – изоинтенсивный; T2 – гипоинтенсивный, T2 с подавлением жира – гиперинтенсивный.
Синтез гормонов. Клетки коркового вещества клубочковой зоны синтезируют кортикостерон и дезоксикортикостерон, участвующие в водно-солевом обмене. Суточная экскреция свободного кортизола менее 100 мкг.
В пучковой зоне образуются глюкокортикоиды, регулирующие проницаемость сосудов и процессы коллагенообразования.
В сетчатой зоне – половые гормоны: андрогены (мужчины), эстрогены и прогестерон (женщины).
В мозговом веществе синтезируется адреналин и норадреналин, стимулирующие функцию симпатической нервной системы.
Альдостерон. Концентрация в плазме у женщин – 0,14-0,83 нмоль/л (при беременности в 2-3 раза выше), у мужчин – 0,17-0,61 нмоль/л.
Катехоламины. Адреналин – 0-6.28 нмоль/л, норадреналин – 0-11.76 нмоль/л.
17-КС (17-кетостероиды) в моче: 27.7-79,7 мкмоль/сут (муж.), 17,4-55,4 мкмоль/сут (жен.).
Кортизол в плазме – 230-750 нмоль/л.
11-ОКС (11-оксикортикостероиды). В плазме – 130-230 мкг/л, связанные с белками 129-203 мкг/л, свободные 11-32 мкг/л.
17-ОКС (17-оксикортикостероиды). В плазме –0.14-0.55 мкмоль/л, в моче: 0,11-0,77 мкмоль/сут (свободные).
Тестостерон – 19,85+4,68 нмоль/л (муж.).
Классификация заболеваний надпочечников.
По функциональному состоянию (характеристика):
Недостаток гормонов: Острая недостаточность (надпочечниковый криз – синдром Waterhouse-Friderichsen). Первичная хроническая недостаточность (болезнь Аддисона). Вторичная хроническая недостаточность при пангипопитуитаризме. Гипоальдостеронизм.
Избыточная продукция гормонов:
Коркового слоя Синдром Кушинга. Альдостеронизм. Адреногенитальный синдром. Вирилизирующие опухоли. Феминизация. Пирогенный рак.
Мозгового слоя Феохромоцитома Симпатобластома Нейробластома Ганглионеврома
Болезнь Аддисона. Эндокринная болезнь, обусловленная двусторонним поражением коры надпочечников с выключением или уменьшением продукции ее гормонов. Клинически проявляется гиперпигментацией кожи и слизистых оболочек, исхуданием, артериальной гипотензией, нарушениями водно-солевого обмена. Рентгенологически со стороны надпочечников в отдельных случаях обнаруживают участки обызвествлений, а в легких - признаки перенесенного туберкулеза.
Синдром Кушинга. Диагностика. Суточная экскреция свободного кортизола > 100 мкг. Ночная дексаметазоновая проба с уровнем кортизола в плазме > 70 мкг/л. Определяют исходный уровень АКТГ в плазме, затем проводят пролонгированную дексаметазоновую пробу с определением уровня кортизола в плазме и свободного кортизола в моче. При опухолях надпочечников никакие дозы дексаметазона не вызывают угнетения секреции кортизола, АКТГ в крови не обнаруживается.
При синдроме эктопической секреции АКТГ дексаметазон не вызывает угнетения секреции кортизола, уровень АКТГ в крови повышен.
Болезнь Кушинга (гиперсекреция АКТГ гипофизом, двухсторонняя гиперплазия надпочечников): секреция кортизола не подавляется низкими, но подавляется высокими дозами дексаметазона менее чем на 50% по сравнению с исходным уровнем, уровень АКТГ нормальный или повышенный.
Первичный альдостеронизм. Диагностика. Активность ренина плазмы < 1 нг/мл/ч и суточная экскреция калия >30 мэкВ. Суточная экскреция альдостерона, натрия и кортизола; активность ренина плазмы в вертикальном положении, уровень калия плазмы. Для дифференциальной диагностики аденомы и двухсторонней гиперплазии надпочечников используют КТ. При неоднозначных результатах прибегают к МРТ или сцинтиграфии надпочечников с иодсодержащими холестерина. Если же и в этом случае диагноз не ясен, проводят двухстороннюю катетеризацию надпочечниковых вен (если уровень альдостерона различается менее чем в два раза, вероятен диагноз гиперплазии). Множественные кисты почек.
Адреногенитальный синдром. АГС (врожденная вирилизирующая гиперплазия коры надпочечников) – врожденное нарушение синтеза гормонов в коре надпочечников, в результате которых развивается избыточная продукция андрогенов. Наиболее часто наблюдаемый ферментный дефект – недостаточность 21-гидроксилазы, вследствие чего снижается синтез кортизола. Компенсация функции коры надпочечников на нижней границе нормы обеспечивается повышенной секрецией АКТГ, которая приводит к гиперпродукции андрогенов, прогестерона и 17-гидроксипрогестерона, угнетающих активность альдостерона (сользадерживающее действие на уровне почечных канальцев). Первичное обследование выявляет снижение кортизола, повышение кортикотропина и тестостерона в плазме, повышение суточной экскреции 17-КС. Дексаметазоновая проба приводит к снижению уровня кортикотропина и 17-КС > 50%. Ультразвуковое исследование и сцинтиграфия выявляют гиперплазию обоих надпочечников. В случае неэффективности этих методов используют РКТ или МРТ.
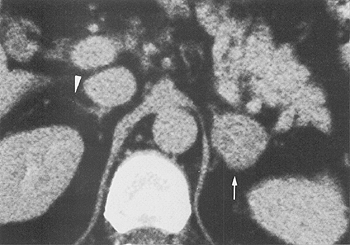
Рентгеновская компьютерная томограмма – срез на уровне надпочечников. Аденома правого надпочечника (стрелка).
Опухоль надпочечника. Бывает доброкачественной и злокачественной, встречается весьма редко. Для диагностики применяют пневморетроперитонеум и ангиографию, при помощи которой определяют форму и размеры органа, наличие опухоли. При больших опухолях надпочечника наблюдается смещение почки внизу, деформация верхних чашек, а нередко и лоханки. В диагностике большое значение имеет ретроградная пиелография в сочетании с томографией и особенно с пневморетроперитонеумом. На снимке хорошо определяется неизменный верхний полюс почки, а над ним - тень увеличенного надпочечника, контуры которого или неровные, или ровные, но четкие. На ангиограммах выявляют скопления различной формы и величины пятен контрастного вещества в области опухоли (аденома коры надпочечников, феохромоцитома).
МРТ исследование позволяет выявлять очаги гипо-, изо- или гиперинтенсивного МР-сигнала утолщенной ножки надпочечника (например, на T2-взвешенных изображениях МР-сигнал понижен при феохромоцитомах) или очага гипо- или гиперинтенсивного МР-сигнала (участок обызвествления, перераспределение жира, липома). Для дифференциальной диагностики доброкачественных и злокачественных опухолей надпочечников используется МРТ с усилением (контрастированием):
аденомы показывают медленное увеличение сигнала, которое обычно возвращается к первоначальному уровню к 10 минуте после введения контрастного вещества;
большинство злокачественных опухолей все еще показывает интенсивное накопление после 15 минуты.
Кроме того, могут использоваться изображения с использованием химического сдвига – in-phase и out-phase T1-взвешенные изображения показывают сигнал жировой ткани (спад сигнала) в доброкачественных образованиях.
Аденома коры надпочечников. Гормонально-активная аденома, происходящая из клеток коры надпочечников. Клинически проявляется адреногенитальным синдромом, включающим чаще всего признаки вирилизации. Рентгенологически - увеличением надпочечника; возможны обызвествления аденомы.
Феохромоцитома. Гормонально-активная опухоль, происходящая из зрелых клеток хромаффинной ткани, чаще из мозгового вещества надпочечников. Клинически проявляется внезапно наступающими приступами пароксизмальной гипертонии, тахикардии и сильной головной боли. Патогномоничным признаком является обнаружение высокого содержания катехоламинов (адреналина и норадреналина) в крови и в моче, суточной или собранной в течение нескольких часов после криза. Рентгенологическая картина феохромоцитомы мозгового слоя надпочечника не отличается от таковой при опухолях коры надпочечника (см. Опухоли надпочечника). Большую помощь в диагностике оказывает ангиография надпочечника. Характерные признаки: надпочечниковая артерия расширена и становится видимой на ангиограмме (в норме из-за малого калибра сосуда, который равен менее 1 мм, он не виден); скопления контрастной жидкости в виде бесформенных, разнопетлистых сеток, напоминающих обрывки сосудов, располагающихся вне тени почки, над ней. Наибольшая диагностическая эффективность отмечается при комбинированном исследовании больных - при помощи пневморетроперитонеума и аортографии.
Диагностика. Суточная экскреция метанефринов > 1,3 мкг. Уровень катехоламинов в плазме > 2000 пг/мл, при 500-2000 пг/мл проводится клонидиновая проба. Если уровень катехоламинов в плазме снижается более чем на 50%, то это свидетельствует о феохромоцитоме.
Определение локализации опухоли. В 90% случаев опухоль удается обнаружить при КТ. К другим методам относится с 131I-метаиодбензилгуанидином и селективная ангиография с определением регионального содержания катехоламинов.
ЛИТЕРАТУРА
Клиническая эндокринология: руководство. Под ред. Н.Т. Старковой. – Спб: Питер, 2002. – 576 с.
Эндокринология. Под ред. Н. Лавин. – Москва: Практика, 1999.
Никонова Л.В., Волков В.Н., Тишковский С.В. Гиперпаратиреоз. Часть I // Вестник ГрГМУ. – 2005. – № 3. – С. 13-16.
Никонова Л.В., Волков В.Н., Тишковский С.В. Гиперпаратиреоз. Часть II // Вестник ГрГМУ. – 2005. – № 3. – С. 17-18.
Читайте также:
- Варианты желудочно-кишечных кровотечений. Признаки желудочно-кишечного кровотечения.
- Орган Корти. Физиология и функция органа Корти
- Осложнения болезни Вильсона-Коновалова. Клиника гемолитического осложнения Вильсона-Коновалова
- Показания и методика операции эзофагомиотомии по Геллеру при ахалазии пищевода
- Примеры грибовидной беспигментной меланомы хориоидеи
