Гистиоцитоз из клеток Лангерганса под маской пеленочного дерматита у новорожденного
Обновлено: 02.05.2024
В статье описано клиническое наблюдение редко встречающегося заболевания — гистиоцитоза из клеток Лангерганса, ранее называемого гистиоцитозом Х. Этиология заболевания неизвестна. Основными механизмами развития заболевания считаются клональная пролиферация патологических клеток Лангерганса и аномальная регуляция взаимодействия клеток иммунной системы в очагах поражения. Клеточный инфильтрат носит полиморфный характер и содержит, помимо патологических клеток Лангерганса, лимфоциты, эозинофилы, моноциты, макрофаги. Гистиоцитоз из клеток Лангерганса — болезнь, патогенез которой сочетает черты новообразования и реактивного процесса. Пик заболеваемости приходится на ранний детский возраст. Клиническая картина заболевания варьирует от локализованных форм с доброкачественным течением и спонтанным выздоровлением до диссеминированных форм с быстро прогрессирующим течением и летальным исходом. В патологический процесс могут вовлекаться любые органы и системы в различном сочетании: скелет, кожа, лимфатические узлы, наружное ухо, печень, селезенка, костный мозг, легкие, эндокринные железы, центральная нервная система, желудочно-кишечный тракт, тимус.
Особенностью данного клинического случая является манифестация заболевания во взрослом возрасте с эндокринопатий: развитием несахарного диабета, гиперпролактинемии, аменореи.
Ключевые слова: гистиоцитоз из клеток Лангерганса, несахарный диабет, гиперпролактинемия, аутоиммунный тиреоидит, аменорея.
Для цитирования: Демидова Т.Ю., Грицкевич Е.Ю., Волкова Е.В. Гистиоцитоз из клеток Лангерганса в эндокринологической практике. Клиническое наблюдение. РМЖ. 2019;12:25-28.
Clinical case of Langerhans cell histiocytosis in endocrinological practice
T.Yu. Demidova, Ye.Yu. Gritskevich, Ye.V. Volkova
Pirogov Russian National Research Medical University, Moscow
The article describes a clinical case of a rare disease — Langerhans cells histiocytosis, formerly histiocytosis X, which etiology is unknown. The main mechanisms of disease progression are a clonal proliferation of pathological Langerhans cells and abnormal regulation of immune system cells interaction in lesions. Cell infiltration has polymorphic nature and contains lymphocytes, eosinophils, monocytes, macrophages alongside pathological Langerhans cells. Langerhans cells histiocytosis pathogenesis combines patterns of neoplasm and reactive process. The peak incidence is in early childhood. The disease clinical picture varies from localized forms with the benign course and spontaneous recovery to disseminated forms with a rapidly progressive course and fatal outcome. Pathological process can involve any organs and systems in different combinations: skeleton, skin, lymph nodes, outer ear, liver, spleen, bone marrow, lungs, endocrine glands, central nervous system, gastrointes tinal tract, thymus. The peculiarity of this clinical case is the disease manifestation in adulthood with endocrinopathy: development of diabetes insipidus, hyperprolactinemia, amenorrhea.
Keywords: Langerhans cells histiocytosis, diabetes insipidus, hyperprolactinemia, autoimmune thyroiditis, amenorrhea.
For citation: Demidova T.Yu., Gritskevich Ye.Yu., Volkova Ye.V. Clinical case of Langerhans cell histiocytosis in endocrinological practice.
RMJ. 2019;12:25–28.
Введение
Гистиоцитоз из клеток Лангерганса — заболевание, в основе которого лежат аномальная пролиферация и аккумуляция в органах и тканях патологических клеток Лангерганса, которые сливаются вместе с эозинофильными гранулоцитами в гигантские многоядерные клетки, образуя гистиоцитарные гранулемы, что ведет к локальному повреждению и нарушению функции пораженных органов [1]. Термин «гистиоцитоз из клеток Лангерганса» объединяет заболевания, ранее известные как эозинофильная гранулема, болезнь Хэнда — Шуллера — Крисчена и болезнь Абта — Леттерера — Зиве [2]. Этиология заболевания неизвестна. Основными механизмами развития заболевания считаются клональная пролиферация патологических клеток Лангерганса и аномальная регуляция взаимодействия клеток иммунной системы в очагах поражения. Клеточный инфильтрат носит полиморфный характер и содержит, помимо патологических клеток Лангерганса, лимфоциты, эозинофилы, моноциты, макрофаги. Гистиоцитоз из клеток Лангерганса сочетает черты новообразования и реактивного процесса. В исследованиях продемонстрированы участие в патогенезе провоспалительных цитокинов («цитокиновый шторм»), экспрессия факторов роста эндотелия (VEGF), белков сигнального пути Fas (Fas-лиганд и рецептор относятся к семейству фактора некроза опухолей, участвуют в механизмах апоптоза) [3]. Пик заболеваемости приходится на ранний детский возраст [4]. Клиническая картина заболевания варьирует от локализованных форм с доброкачественным течением и спонтанным выздоровлением до диссеминированных форм с быстро прогрессирующим течением и летальным исходом. В патологический процесс могут вовлекаться любые органы и системы в различном сочетании: скелет, кожа, лимфатические узлы, наружное ухо, печень, селезенка, костный мозг, легкие, эндокринные железы, центральная нервная система (ЦНС), желудочно-кишечный тракт, тимус.
Поражение кожи проявляется пятнисто-папулезной сыпью с бурым оттенком, корочками, геморрагическим компонентом. Патология ЦНС может носить очаговый дегенеративный характер либо характер объемного образования. Клиническая симптоматика включает общемозговые симптомы и очаговый неврологический дефицит, характер которого определяется локализацией поражения. Среди нарушений эндокринной системы часто инфильтративный процесс захватывает заднюю долю гипофиза с формированием несахарного диабета, возможно развитие пангипопитуитаризма. Среди других нарушений у пациентов могут быть гепатоспленомегалия, цитопенический синдром в результате нарушения функции костного мозга, желтуха, генерализованная лимфаденопатия, рецидивирующие наружные отиты (как компонент кожного синдрома), энтероколит [5].
В соответствии с числом пораженных органов принято выделять моно- и мультисистемное поражение. Учитывая, что наиболее часто органом-мишенью при гистиоцитозе является кожа, для верификации диагноза наиболее часто проводят биопсию кожи с последующим гистологическим исследованием, однако при отсутствии кожных проявлений возможно провести биопсию другого пораженного органа [6].
Стратегия лечения зависит от количества пораженных систем и органов и вовлеченности в процесс органов риска, к которым относят костный мозг, селезенку, печень. В случае моносистемного поражения кожи при нетяжелом течении заболевания терапия может ограничиваться местным лечением топическими глюкокортикостероидами. Системная комбинированная химиотерапия показана при мультисистемном поражении и случаях односистемных заболеваний, не поддающихся лечению другими методами. Применяется комбинация цитостатических препаратов и системных глюкокортикостероидов [7].
Клиническое наблюдение
Женщина, 25 лет, госпитализирована бригадой скорой медицинской помощи в отделение реанимации и интенсивной терапии ГКБ им. В.П. Демихова в связи с выраженной гипотонией, гиповолемией. После стабилизации состояния переведена в отделение эндокринологии с жалобами на сухость во рту, жажду, учащенное мочеиспускание, выраженную слабость (пациентка не могла встать с постели), болезненные зудящие кожные высыпания с серозным отделяемым в подмышечных областях, паховых складках. Объективные данные: рост 158 см, вес 93 кг, ИМТ 37,2 кг/м 2 . В сознании, однако без критического отношения к своему состоянию. Анамнез заболевания собирали со слов матери и по данным выписных эпикризов. Положение больной в постели активное. Температура тела 36,8 °C. Дыхание: самостоятельное, адекватное, аускультативно жесткое, проводится во все отделы грудной клетки. ЧДД 17 в минуту. SaО2 97%. Тоны сердца ясные. АД 100/57 мм рт. ст. Пульс по кардиомонитору: 74 в минуту, ритмичный. Язык: подсушен, обложен желтоватым налетом, на слизистой полости рта множественные изъязвления, трещины на губах, рот постоянно приоткрыт. Живот: округлой формы, увеличен в размерах за счет подкожной жировой клетчатки. В реанимационном отделении пациентке установлен уретральный катетер. В домашних условиях в связи с малоподвижностью используют подгузник.
Больная — единственный ребенок в семье, проживает с матерью, анамнез со стороны отца неизвестен. Мать страдает морбидным ожирением с детского возраста. У пациентки при рождении диагностированы фетопатия, врожденное расходящееся косоглазие. Ожирение развилось на первом году жизни. Росла и развивалась соответственно возрасту, однако, со слов матери, с детского возраста наблюдалась у психиатра (выписки не представлены). Впервые зудящие кожные высыпания появились в возрасте 19 лет, что связывает с укусом собаки и последующим лечением. В течение года зона поражения распространилась на волосистую часть головы, подмышечные впадины, затем на паховые складки. Местное лечение амбулаторно — без эффекта. Со слов матери, пациентка часто не соблюдала правила личной гигиены. Впоследствии, в том же году, появились жалобы на выделения из молочных желез, аменорею, затем присоединились жалобы на жажду, сухость во рту, учащенное мочеиспускание. При обращении в Эндокринологический научный центр (ЭНЦ) была выявлена гиперпролактинемия (пролактин составил 1374 мЕД/дл), несахарный диабет (осмоляльность плазмы 0,315 мосм/кг), по данным МРТ было обнаружено супраселлярное объемное образование, кистозное образование задней черепной ямки 23×58 мм, был предположен диагноз гистиоцитоза из клеток Лангерганса. Консультирована нейрохирургом, по заключению которого оперативное лечение не было показано. При выписке были рекомендованы каберголин 0,5 мг/нед. и десмопрессин 240 мкг 3 р./сут. На фоне терапии месячные у больной были регулярными, мочеиспускание нормализовалось.
По поводу кожных высыпаний рекомендована консультация в ГКБ им. Короленко, куда обратилась в возрасте 21 года, находилась на стационарном лечении и где была проведена биопсия кожи с последующим иммуногистохимическим исследованием. Диагноз при выписке: «Гистиоцитоз Х. Вторичная пиодермия». Больной проводилось лечение преднизолоном 50 мг/сут внутрь, цефазолином, метронидазолом, флуконазолом, наружно применялась 2% цинковая паста, мази. При выписке было рекомендовано продолжить глюкокортикоидную, антибактериальную, местную терапию под наблюдением дерматолога, эндокринолога по месту жительства.
Пациентка отметила улучшение самочувствия и регресс кожных высыпаний, однако терапия сопровождалась увеличением массы тела на 20 кг в течение месяца, что послужило причиной самостоятельной отмены препаратов.
Позднее, в 23 года, повторно госпитализирована в отделение терапии с группой ожирения ФГБУ ЭНЦ с прежними жалобами, где выявлена манифестация первичного гипотиреоза в исходе аутоиммунного тиреоидита. Антропометрические данные пациентки в этот период: вес 108 кг, рост 159 см, ИМТ 42,9 кг/м 2 . При осмотре кожного покрова отмечалась пиодермия паховых и подмышечных областей, гипотония — АД 100/60 мм рт. ст. При обследовании: пролактин 30,8 мЕд/л, антитела к тиреопероксидазе 731 МЕ/мл, тромбоцитоз 418 10×9 кл/л, гиперурикемия 401,17 мкмоль/л, осмоляльность мочи 0,405 мосм/кг (референсные значения 0,6–1,2 мосм/кг), при КТ органов грудной клетки инфильтративных поражений не выявлено. При повторном МРТ головного мозга: «МР-картина супраселлярного объемного образования. Арахноидальная киста задней черепной ямки, кистозное образование пинеальной области. Зоны умеренно выраженной перивентрикулярной лейкомаляции в области задних рогов боковых желудочков соответствуют перинатальной энцефалопатии». При УЗИ органов малого таза выявлена гипоплазия матки. Из Эндокринологического научного центра больная выписана с диагнозом: «Основное заболевание: Гистиоцитоз Х. Супраселлярное объемное образование, образование задней черепной ямки. Центральный несахарный диабет, компенсация. Синдром гиперпролактинемии. Вторичная аменорея. Гистиоцитарное поражение кожи. Микробная инфицированная экзема промежности, паховых областей, подмышечных впадин. Аутоиммунный тиреоидит. Первичный гипотиреоз, субкомпенсация. Ожирение III степени (ИМТ 42,9 кг/м 2 ). Сопутствующие заболевания: ЖКБ. OU — ангиопатия сетчатки. Миопия средней степени. Расходящееся косоглазие. OD — врожденная гипертрофия ретинального пигментного эпителия». При выписке из стационара рекомендованы: десмопрессин 0,5 мг/сут, каберголин 0,25 мг 2 р./сут, левотироксин натрия 150 мкг утром натощак за 30 мин до еды, наблюдение дерматолога по месту жительства, консультация онколога. К онкологу в дальнейшем больная не обращалась.
В 24 года пациентке была проведена денситометрия поясничного отдела позвоночника, где, согласно Z-критерию, отмечалось снижение минеральной костной плотности.
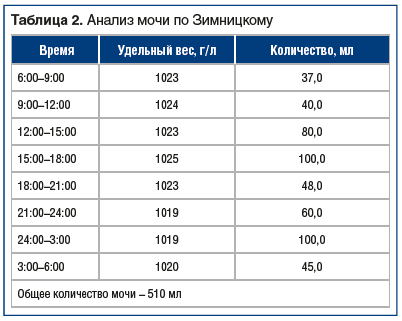
При обследовании в ГКБ им. Демихова в 2019 г. была выявлена железодефицитная анемия средней степени тяжести (гемоглобин 74 г/л, железо 4,7 мкмоль/л), гипертриглицеридемия 2,6 ммоль/л. Нарушений углеводного обмена не выявлено. Данные иммунохимических исследований и результаты пробы Зимницкого представлены в таблицах 1 и 2. Кожные покровы с выраженными изменениями: элементы папулезной сыпи, поражение всех кожных складок по типу интертриго инфильтративно-воспалительного характера с мацерацией и отделяемым с неприятным запахом, формирование корок, атрофические рубцы (рис. 1).


На фоне проведенной терапии состояние больной улучшилось, стала самостоятельно садиться в кровати, гемоглобин 115 г/л, АД 110/70 мм рт. ст., мацерации в паховых складках перестали кровоточить, гиперемия и отек уменьшились.
Описанное клиническое наблюдение интересно развитием полиорганной эндокринологической патологии на фоне течения редкого заболевания — гистиоцитоза из клеток Лангерганса. Первыми специалистами, заподозрившими гистиоцитарное поражение гипоталамо-гипофизарной области, были именно специалисты эндокринологического стационара. При изучении анамнеза больной можно проследить прогрессирование заболевания: вначале появилось поражение кожи, далее к нему последовательно присоединились гиперпролактинемия, несахарный диабет, гипогонадизм, что свидетельствует о мультисистемном поражении и прогрессирующем тяжелом течении заболевания. Так как больная не наблюдалась у гематолога, онколога, инфильтративный процесс поражал все большие участки кожи и ЦНС.
По данным «Федеральных клинических рекомендаций по диагностике и лечению гистиоцитоза из клеток Лангерганса» 2015 г. основными препаратами для лечения гистиоцитоза являются винбластин, преднизолон, 6-меркаптопурин. К терапии второй линии относится комбинированная химиотерапия препаратами 2-хлордезоксиаденозина и цитарабина и аллогенная трансплантация гемопоэтических стволовых клеток. Для определения тактики лечения выделяют 3 группы пациентов, в зависимости от количества пораженных систем органов и вовлеченности в патологический процесс печени, селезенки, костного мозга. К группе низкого риска относятся пациенты с локальным поражением одного органа/системы. К группе промежуточного риска относятся пациенты с поражением нескольких органов/систем без вовлечения органов риска, а также пациенты с интракраниальным объемным образованием, сдавлением спинного мозга, с литическими очагами основания черепа, височной кости, основной кости, сосцевидного отростка, орбиты. К группе высокого риска относятся пациенты с поражением нескольких органов/систем с вовлечением органов риска [1]. Следовательно, можно предположить, что данная пациентка относилась к группе промежуточного риска, т. к. имела интракраниальное объемное образование. Согласно клиническим рекомендациям таким пациентам необходима системная химиотерапия препаратами винбластин и преднизолон. Как мы видим, несмотря на поставленный 6 лет назад диагноз, пациентка не получала лечения по поводу гистиоцитоза из клеток Лангерганса, кроме краткосрочного лечения преднизолоном в возрасте 21 года, не была консультирована онкогематологом, получала только терапию, направленную на коррекцию функций пораженных органов.
Врачам-эндокринологам стоит иметь в виду возможность развития вторичной патологии органов эндокринной системы на фоне системного гранулематозного заболевания и направлять таких пациентов к специалистам для лечения основного заболевания.
1. Федеральные клинические рекомендации по диагностике и лечению гистиоцитоза из клеток Лангерганса. Под ред. М.А. Масчан, Г.А. Новичковой, Г.А. Румянцева. М.; 2014. [Federal clinical guidelines for the diagnosis and treatment of histiocytosis from Langerhans cells. Eds. M.A. Maschan, G.A. Novichkova, G.A. Rumyantsev. M.; 2014 (in Russ.)].
2. Новичкова Г.А., Минков М.Л., Масчан М.А. Гистиоцитозы. Клиническая онкогематология: руководство для врачей. Под ред. М.А. Волковой. М.: Медицина; 2007. [Novichkova G.A., Minkov M.L., Maschan M.A. Histiocytosis. Clinical oncohematology: a guide for doctors. Ed. M.A. Volkova. M.: Medicine; 2007 (in Russ.)].
3. Badalian-Very G., Vergilio J.A., Degar B.A. et al. Recent advances in the understanding of Langerhans cell histiocytosis. Br J Haematol. 2012;156:163–172.
4. Egeler R.M., van Halteren A.G., Hogendoorn P.C. et al. Langerhans cell histiocytosis: fascinating dynamics of the dendritic cell-macrophage lineage. Immunol Rev. 2010;234(1):213–132.
5. Windebank K.P., Nanduri V. Langerhans Cell Histiocytosis. Arch Dis Child. 2009;94(11):904–908. DOI: 10.1136/adc.2007.125872.
6. Chandekar S.A., Shah V.B., Kavishwar V. Cytological diagnosis of Langerhans cell histiocytosis with cutaneous involvement. J Cytol. 2013;30(1):81–83.
7. Gadner H. Treatment of adult-onset Langerhans cell histiocytosis — is it different from the pediatric approach? Ann Oncol. 2010;21(6):1141–1142. DOI: 10.1093/annonc/mdp540.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Пеленочный (памперсный) дерматит у детей - подходы к профилактике и лечению:
Т.А. Бокова, д. м. н., профессор; Г.В. Масликова, к. м. н., доцент, кафедра педиатрии факультета усовершенствования врачей ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, г. Москва
Пеленочный или памперсный дерматит (ПД) является актуальной проблемой детей грудного возраста. Частота его возникновения колеблется от 35 до 50%, причем у девочек он возникает чаще, чем у мальчиков. Преобладает среди младенцев второго полугодия жизни (6-12 месяцев) [1]. Предпосылкой для его развития являются особенности строения кожных покровов.
Ключевые слова: пеленочный дерматит, кожа, профилактика, лечение
Keywords: diaper dermatitis, skin, prevention, treatment.
Кожа новорожденного ребенка тонкая (3-4 слоя), слой между эпидермисом и дермой более рыхлый, тонкий слой эпидермиса склонен к повреждению, слабо развит соединительнотканный компонент дермы, базальная мембрана хрупкая, иммунная и терморегуляторная функции развиты недостаточно. У младенцев отмечаются более высокие значения рН и уровня поверхностных липидов кожи по сравнению со взрослыми, тогда как защитная кислая среда формируется в более старшем возрасте. Содержание воды в роговом слое кожи у детей также значительно выше.
В детском возрасте кожа выполняет целый ряд функций. Во-первых, она служит защитным барьером от внешних агрессивных факторов. Другая функция - дыхательная, и чем меньше ребенок, тем более значимой она является. Выделительная функция кожных покровов у детей раннего возраста по сравнению с детьми старшего возраста развита хуже. Кожа является сложным органом чувств. В ней находится много рецепторов, воспринимающих раздражения.
Причинами развития ПД является постоянный контакт кожи ребенка с подгузниками или пеленками (трение), длительное воздействие химических факторов (кал, моча), неправильное использование средств ухода (мазей, присыпок, мыла). Кроме того, возникновению ПД способствует повышенная влажность кожных покровов и затрудненный доступ воздуха во влажные пеленки (подгузники). К ПД больше предрасположены дети с отягощенным аллергическим фоном. Младенцы, находящиеся на естественном вскармливании, ПД страдают реже, что объясняется низкой ферментативной активностью кала у этих детей.
Пеленочный дерматит следует рассматривать как циклический процесс [2]. На первом этапе снижается защитная функция рогового слоя эпидермиса здоровой кожи при ее повреждении. Контакт кожи с мочой, калом приводит к повышению количества влаги на ее поверхности и оказывает раздражающее действие. Под действием трения влажная кожа легче повреждается, что, в свою очередь, способствует более глубокому проникновению агрессивных веществ (мочевина, аммиак, ферменты кала). На следующем этапе развивается воспалительный процесс - непосредственно ПД. Он проявляется гиперемией, отеком, появлением сыпи (папулы, везикулы) в области контакта с подгузником (пеленкой), которая захватывает нижнюю часть живота, спины, ягодицы, область промежности и внутреннюю поверхность бедер. Микробные и грибковые агенты, содержащиеся в фекалиях, могут инфицировать ослабленную кожу. О присоединении бактериальной инфекции свидетельствует появление гиперемии с экссудатом, формирование пустул. Наиболее часто развивается стрептококковый, стафилококковый или кандидозный ПД. Это вызывает не только физический дискомфорт, но и отрицательно сказывается на функциональном состоянии нервной системы у детей - они становятся беспокойными, нарушается сон, снижается аппетит.
Различают три степени тяжести ПД. При легкой степени дерматита площадь поражения составляет менее 10% поверхности, отмечается умеренное покраснение, нерезко выраженная папулезная сыпь и шелушение эпидермиса. При среднетяжелом течении на коже возникают папулы, пустулы, эрозии, в кожных складках могут образовываться инфильтраты, высока частота инфицирования. При неустранении раздражающих факторов и продолжительном течении заболевания (тяжелая степень) образуются инфильтраты, папулы, пузырьки, мокнутие, глубокие эрозии, изъязвления, а область поражения значительно увеличивается. Следует отметить, что неосложненный ПД при соответствующем уходе за кожей ребенка ликвидируется через 2-3 дня, тогда как инфицирование приводит к усугублению воспалительного процесса, а также к увеличению длительности заболевания.
Основной целью ухода за кожей ребенка раннего возраста является устранение раздражения и предотвращение повреждения эпидермиса [3]. При использовании одноразовых подгузников важно их регулярно менять (каждые 3-4 ч), даже ночью. Следует подбирать их точно по размеру и с учетом пола малыша. Ребенка не следует одевать в плотно прилегающую одежду, имеющую большое количество оборок, застежек, складок и пр. Не кутать - ребенок раннего возраста очень чувствителен к перегреванию. Использовать натуральные хлопковые или смесовые ткани, мягкие, с хорошей воздухопроницаемостью.
Нежная кожа младенца нуждается в мягком и регулярном очищении, особенно в области промежности. Для этого используют щадящие моющие средства, однако их не следует применять часто и в избыточном количестве. Мыло может раздражать кожу за счет щелочного компонента, пены для ванн и шампуни также дают обезжиривающий эффект. Поэтому купать ребенка с применением моющих средств следует не чаще 2-3 раз в неделю, тогда как подмывать - регулярно, а после дефекации - обязательно. Сушить кожу лучше промокающими движениями с помощью бумажных полотенец или пеленок из мягкой хлопчатобумажной ткани. Кожу малыша можно припудривать, однако важно, чтобы при этом она была тщательно высушена, а также смазывать смягчающими средствами. Косметические средства ухода за кожей надо подбирать индивидуально (косметические линии «Авен», «Мустела», «Атодерм» и пр.).
При ПД для обработки пораженных участков рекомендуется применение кремов и мазей. Используемый препарат следует ежедневно наносить тонким слоем на пораженные участки кожи ребенка во время пеленания до исчезновения симптомов ПД.
Мазь на основе цинка оксида (деситин, дудо-крем, цинковая мазь) оказывает стягивающее действие, в результате чего уменьшается поступление слизи и других секретов на пораженные участки кожи. Создается защитный барьер для действия раздражающих факторов. Оказывает подсушивающее, адсорбирующее, вяжущее и дезинфицирующее действие. Уменьшает экссудацию и мокнутие, что снимает местные явления воспаления и раздражение.
Мази на основе декспантенола (Д-пантенол, Бепантен) нормализуют клеточный метаболизм, увеличивают прочность коллагеновых волокон, оказывают регенерирующее, слабое противовоспалительное действие, питают и смягчают кожу.
Соблюдение гигиены и правил ухода за кожей не только предотвращает развитие ПД и снижает риск вторичных (ассоциированных) инфекций кожных покровов, но также способствует формированию санитарно-гигиенических навыков у ребенка в более старшем возрасте.
Гистиоцитоз из клеток Лангерганса под маской пеленочного дерматита у новорожденного
Пеленочный дерматит и его варианты у новорожденного
Для дерматозов характерны острые (эритема, отек и везикуляция) и/или хронические (шелушение, лихенификация, увеличение или уменьшение пигментации) изменения кожи. При микроскопическом исследовании наблюдаются инфильтрация кожи воспалительными клетками, вариабельное утолщение эпидермиса и десквамация.
Ирритантный контактный пеленочный дерматит
Пеленочный дерматит - одно из самых распространенных кожных заболеваний младенческого возраста. Его самая типичная форма - ирритантный контактный дерматит. Область подгузников - основная мишень ирритантного дерматита, поскольку она контактирует с мочой и фекалиями и плотно закрыта подгузниками.
Хотя вначале ведущая роль в патогенезе пеленочного дерматита отводилась аммиаку мочи, современные данные свидетельствуют о том, что главным виновником заболевания являются фекалии. Когда эпидермальный барьер нарушается, кожа становится чувствительной к другим раздражителям, таким как мыло, тальк и детергенты.
Частый водянистый стул, особенно после приема антибиотиков или вирусных инфекций, нередко вызывает тяжелый дерматит, устойчивый к консервативным терапевтическим мероприятиям.
Краснота, шелушение и иногда эрозивные реакции раздражения обычно ограничены выпуклыми поверхностями промежности, нижней частью живота, ягодицами и проксимальными участками конечностей. Интертригинозные участки, как правило, не поражаются. Мягкая и тщательная очистка этой зоны и применение лубрикантов (например, вазелина) и защитных паст (например, окиси цинка) обычно приводят к разрешению дерматита.
Устранение симптомов при тяжелом дерматите можно ускорить курсом местной терапии КСП в форме крема, содержащего гидрокортизона бутират (Локоид), при постепенном уменьшении количества аппликаций.

а - ирритантный контактный дерматит поражает выпуклые поверхности зоны подгузников, оставляя нетронутыми кожные складки.
б - стафилококковый пеленочный дерматит. Наблюдается множество целостных тонкостенных пустул, окруженных красными ободками,
а также многочисленные участки, на которых пустулы вскрылись,
оставив воротничок шелушения вокруг оголенного красного основания.
Аллергический контактный пеленочный дерматит
Хотя аллергический контактный дерматит встречается реже, чем ирритантный, иногда он также может быть причиной высыпаний в области подгузников. Ароматизаторы, консерванты и эмульгаторы, такие как меркаптобензотиазол, ароматическая смесь, дисперсный краситель, циклогексилтиофталимид, n-трет-бутил-фенолформальдегидная смола и сорбитана сесквиолеат в продуктах для местного применения у детей и в подгузниках могут вызывать аллергические реакции в области подгузников, а также на лице, туловище и конечностях.
Исключение провоцирующего вещества, активное применение эмолентов и разумные аппликации топических КСП (Локоид) способствуют разрешению таких реакций в течение нескольких дней.
Инфицированный контактный пеленочный дерматит
Контактный пеленочный дерматит иногда осложняется вторичной стафилококковой инфекцией, или же пустулы могут появляться как первичные очаги, особенно в первые несколько недель жизни. Наличие тонкостенных пустул на эритематозном основании должно вызвать подозрение на наличие стафилококкового пустулеза. Очаги обычно быстро вскрываются и высыхают, образуя воротничок чешуек вокруг оголенного красного основания.
Окрашивание препарата содержимого пустулы по Граму позволяет визуализировать гроздья грамположительных кокков и нейтрофилов. Анализ на бактериальную культуру подтверждает диагноз.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Пеленочный дерматит. Клинические рекомендации.
Пеленочный дерматит – распространенное заболевание детей в возрасте до 2-х лет, характеризующееся островоспалительными высыпаниями на коже в области ношения подгузника.
1. Краткая информация
1.1 Определение
1.2 Этиология и патогенез
Пеленочный дерматит – мультифакториальное заболевание. Основными этиологическими факторами его развития являются трение подгузника, мацерация (размягчение верхних слоев эпидермиса в результате мокнутия), в следствии воздействие на кожу мочи, ферментов кала, изменение рН кожи в щелочную сторону, контакт кожи с очищающими гигиеническими средствами, присоединение вторичной грибковой инфекции (C. albicans).
Несоблюдение гигиенических процедур приводит к продолжительному контакту кожи ребенка в области подгузника с мочой и калом, что обусловливает повышенную влажность кожи в этой зоне и проникновение щелочных веществ через эпидермальный барьер. При сохранении указанных условий более трех дней отмечается присоединение C. albicans.
1.3 Эпидемиология
Пеленочный дерматит развивается у 20% младенцев и детей в возрасте до 2 лет, чаще всего в возрастной период между 9 и 12 месяцами [1,2]. Заболевание с одинаковой частотой наблюдается у детей женского и мужского пола [3, 4].
1.4 Кодирование по МКБ 10
L22 – Пеленочный дерматит.
1.5. Классификация
Общепринятой классификации не существует.
1.6 Клиническая картина
В зависимости от преобладания тех или иных провоцирующих факторов выделяют три клинических типа пеленочного дерматита: пеленочный дерматит в результате трения, контактный ирритантный пеленочный дерматит и пеленочный дерматит, осложненный кандидозом [5].
Пеленочный дерматит в результате трения является наиболее легкой и часто встречающейся клинической формой пеленочного дерматита у детей в возрасте от 7 до 12 месяцев. Проявления заболевания обусловлены, в первую очередь, контактом кожи с мочой. Высыпания локализуются в местах наибольшего сдавления и трения кожи подгузником: на животе в области талии, внутренних поверхностях бедер, ягодицах. Дерматит характеризуется умеренной эритемой кожи.
Контактный ирритантный пеленочный дерматит чаще всего локализуется в области межъягодичной складки, на лобке, перианально. Могут быть также поражены нижняя часть живота и верхняя часть бедер. Клинические проявления могут варьировать от слабого покраснения и шелушения кожи до выраженных папулезных и пустулезных элементов на фоне яркой эритемы. Тяжелые формы заболевания характеризуются нарушением целостности кожного покрова вплоть до появления эрозий. Основными провоцирующими факторами их развития являются диарея и щелочная рН кала.
Пеленочный дерматит, осложненный кандидозом, характеризуется ярко-красными эрозивными очагами высыпаний с приподнятыми периферическими краями и влажной поверхностью, точечными везикуло-пустулами и единичными сателлитными пустулами. Высыпания локализуются в генитальной области, нижней части живота, на ягодицах, внутренней поверхности бедер и могут выходить за пределы зоны подгузника.
2. Диагностика
2.1 Жалобы и анамнез
Дискомфорт, зуд, жжение в аногенитальной области.
2.2 Физикальное обследование
Объективные клинические проявления пеленочного дерматита, выявляемые при физикальном обследовании, описаны в разделе «Клиническая картина».
2.3 Лабораторная диагностика
- Рекомендуется микроскопическое исследование на Candida.
Уровень убедительности рекомендаций A (уровень достоверности доказательств 1++)
2.4 Инструментальная диагностика
2.5 Иная диагностика
3. Лечение
3.1 Консервативное лечение
- Рекомендуется проведение комплекса мероприятий по уходу за кожей ребенка для предотвращения заболевания. Комплекс мероприятий по уходу является ключевым моментом в терапии больных пеленочным дерматитом. При правильном уходе за кожей ребенка клинические проявления пеленочного дерматита регрессируют в течение 2–3 дней. При отсутствии положительного эффекта от проводимого немедикаментозного лечения проводят медикаментозную терапию. Чаще всего медикаментозное лечение требуется в случае пеленочного дерматита, осложненного вторичной грибковой и/или бактериальной инфекциями.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 4)
- Для лечения пеленочного дерматита, осложненного С. albicans, рекомендуется назначение наружно одного из следующих антимикотических препаратов:
клотримазол 1% крем 2 раза в сутки в течение 14 дней [18].
Уровень убедительности рекомендаций А (уровень достоверности доказательств 1++)
нистатин мазь 2 раза в сутки в течение 14 дней [18].
натамицин 2% крем 2 раза в сутки в течение 14 дней [21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 3)
- Для лечения пеленочного дерматита, осложненного стафилококковой или стрептококковой инфекцией, рекомендуется назначение наружно одного из следующих препаратов:
мупироцин 2% мазь 2-3 раза в сутки в течение 7–10 дней [19].
фузидовая кислота 2% крем 2-3 раза в сутки в течение 7–10 дней [19].
- Для лечения ирритантного пеленочного дерматита на фоне диареи рекомендуется назначение наружно декспантенола 5% крем в сочетании с цинковой мазью в течение 7 дней [20].
Уровень убедительности рекомендаций В (уровень достоверности доказательств 2++)
3.2 Хирургическое лечение
3.3 Иное лечение
4. Реабилитация
5. Профилактика и диспансерное наблюдение
Для профилактики пеленочного дерматита применяется комплекс мероприятий ABCDE (от английских слов air – воздух, barrier – барьер, cleansing – очищение, diapering – смена подгузников, education – обучение) [6].
- Рекомендуются воздушные ванны, позволяющие сократить контакт кожи с любыми раздражителями и уменьшить трение и раздражение кожи подгузником [7,8].
Уровень убедительности рекомендаций D (уровень достоверности доказательств 3)
- Рекомендуются наружные средства в форме крема или пасты, содержащие оксид цинка и/или вазелин, создающие барьер, позволяющий уменьшить контакт кожи с мочой и калом. В то же время они не создают препятствия для восстановления поврежденной поверхности кожи и регресса высыпаний. Барьерные наружные средства должны наноситься толстым слоем после каждой смены подгузника на всю поверхность кожи, имеющую контакт с повреждающими и раздражающими факторами [9].
- Детские присыпки, особенно с содержанием крахмала, не рекомендуются для ухода за кожей в зоне подгузника в связи с риском вдыхания порошкообразных веществ [10].
- Рекомендуется очищение кожи, являющееся неотъемлемой частью профилактики и лечения пеленочного дерматита.
Комментарии: Традиционное очищение водой с использованием хлопковой материи по своему влиянию на увлажненность кожи, рН, эритему, микробную колонизацию при пеленочном дерматите не отличается от очищения при помощи специальных влажных салфеток. В то же время, применение влажных салфеток позволяет быстрее очистить поверхность от остатков кала, тем самым уменьшая дополнительное трение кожи [11, 12].
- При выборе влажных салфеток рекомендуется избегать содержания в них ароматизаторов и спирта, способных вызвать аллергический контактный дерматит [13].
- Рекомендуется своевременная смена подгузника, являющаяся одним из основных и важнейших факторов в лечении пеленочного дерматита. Необходимо менять подгузник через каждые 1–3 часа в течение дня и, как минимум, один раз ночью, а так же в случае его выраженного загрязнения [14]. Доказательными исследованиями роль одноразовых подгузников в предупреждении возникновения пеленочного дерматита не подтверждена, но и не опровергнута [15], при этом ряд научных работ свидетельствует о важном значении этого фактора [16, 17].
- Рекомендуется информирование родителей или ухаживающего персонала об особенностях ухода за кожей в зоне подгузника и обязательном соблюдении правил гигиены, ориентирование на максимально быструю смену загрязненного подгузника и, по возможности, частое пребывание ребенка без подгузника [14].
Критерии оценки качества медицинской помощи
Критерии качества
Уровень достоверности доказательств
Уровень убедительности доказательств
Выполнено микроскопическое исследование соскоба с кожи на C. albicans
Проведена наружная терапия клотримазолом или нистатином или натамицином
Проведена наружная терапия мупироцином или фузидовой кислотой
Достигнута эрадикация C. albicans
Достигнуто исчезновение клинических симптомов заболевания (клиническое выздоровление)
Список литературы
Приложение А1. Состав рабочей группы
- Кубанова Анна Алексеевна – академик РАН, доктор медицинских наук, профессор, Президент Российского общества дерматовенерологов и косметологов.
- Кубанов Алексей Алексеевич – доктор медицинских наук, профессор, член Российского общества дерматовенерологов и косметологов.
- Прошутинская Диана Владиславовна – доктор медицинских наук, доцент, член Российского общества дерматовенерологов и косметологов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория клинических рекомендаций:
- Врачи-специалисты: дерматовенерологи, педиатры;
- Ординаторы и слушатели циклов повышения квалификации по указанным специальностям.
Таблица П1- Уровни достоверности доказательств
Уровни
достоверности доказательств
Описание
Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок
Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок
Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок
Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококачественные обзоры исследований случай-контроль или когортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи
Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи
Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи
Неаналитические исследования (например, описания случаев, серий случаев)
Таблица П2 – Уровни убедительности рекомендаций
Характеристика показателя
По меньшей мере один мета-анализ, систематический обзор или РКИ, оцененные как 1++, напрямую применимые к целевой популяции и демонстрирующие устойчивость результатов
группа доказательств, включающая результаты исследований, оцененные как 1+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов
Группа доказательств, включающая результаты исследований, оцененные как 2++, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов
экстраполированные доказательства из исследований, оцененных как 1++ или 1+
Группа доказательств, включающая результаты исследований, оцененные как 2+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов;
экстраполированные доказательства из исследований, оцененных как 2++
Доказательства уровня 3 или 4;
экстраполированные доказательства из исследований, оцененных как 2+
Порядок обновления клинических рекомендаций
Рекомендации в предварительной версии рецензируются независимыми экспертами. Комментарии, полученные от экспертов, систематизируются и обсуждаются членами рабочей группы. Вносимые в результате этого изменения в рекомендации или причины отказа от внесения изменений регистрируются.
Предварительная версия рекомендаций выставляется для обсуждения на сайте ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России для того, чтобы лица, не участвующие в разработке рекомендаций, имели возможность принять участие в обсуждении и совершенствовании рекомендаций.
Для окончательной редакции и контроля качества рекомендации повторно анализируются членами рабочей группы.
Приложение А3. Связанные документы
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
Клиническое наблюдение гистиоцитоза у ребенка 1 месяца 3 недель, протекавшего под маской наружного диффузного отита
Авторы: Молчанова М.В. 1 , Алексеенко С.И. 2 , Артюшкин С.А. 3
1 ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России, Санкт-Петербург; СПб ГБУЗ «ДГМКЦ ВМТ им. К.А. Раухфуса», Санкт-Петербург
2 ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России, Санкт-Петербург ; СПб ГБУЗ «ДГМКЦ ВМТ им. К.А. Раухфуса», Санкт-Петербург
3 ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» МЗ РФ, Санкт-Петербург
Гистиоцитозы представляют собой группу заболеваний, которые объединяет пролиферативный процесс в моноцитарно-макрофагальной системе с накоплением в очагах поражения патологических гистиоцитов и формированием специфических гранулем.
Возможна иммунопатологическая и опухолевая природа заболевания. В пользу иммунопатологической природы гистиоцитоза свидетельствуют высокая частота спонтанных ремиссий, низкая летальность и отсутствие хромосомных аномалий в клетках из очагов поражения, в пользу опухолевой природы — клональный характер пролиферации клеток Лангерганса в очагах поражения.
Клинические проявления гистиоцитоза весьма разнообразны, что определяет трудность диагностики. В патологический процесс могут вовлекаться различные органы и ткани: кожа, лимфатические узлы, наружное и среднее ухо, плоские кости, костный мозг, печень, селезенка, легкие, эндокринные железы, желудочно-кишечный тракт, головной мозг.
В статье представлен клинический случай гистиоцитоза, диагностированный у ребенка 1 мес. 3 нед., клинические проявления которого маскировались под симптомы наружного диффузного отита.
Описание данного клинического случая преследует цель обратить внимание на особенности течения рецидивирующих наружных и средних отитов у грудных детей, т. к. за маской данных заболеваний может скрываться гистиоцитоз.
Ключевые слова: наружный и средний диффузный отит, дети грудного возраста, гистиоцитоз, компьютерная томография.
Для цитирования: Молчанова М.В., Алексеенко С.И., Артюшкин С.А. Клиническое наблюдение гистиоцитоза у ребенка 1 месяца 3 недель, протекавшего под маской наружного диффузного отита. РМЖ. 2018;10(II):102-104.
Clinical observation of histiocytosis, proceeding under the mask of an acute otitis externa, in a child of 1 month 3 weeks
M.V. Molchanova 1,2 , S.I. Alexeenko 1,2 , S.A. Artyushkin 1
1 Mechnikov Northwestern State Medical University, Saint Petersburg
2 Raukhfus Children City Multi-Profile Clinical Center of High Medical Technologies, Saint Petersburg
A histiocytosis is a group of diseases that combine the proliferative process in the monocyte-macrophage system with the accumulation of pathological histiocytes in the lesions and a formation of specific granulomas.
There is a possibility of an immunopathological and tumor nature of the disease. A high incidence of spontaneous remission, low mortality and an absence of chromosomal abnormalities in cells from lesions are in favor of the immunopathological nature of histiocytosis. In favor of the tumor nature — the clonal nature of the Langerhans cells proliferation in the lesions.
Clinical manifestations of histiocytosis are very diverse, which determines the difficulty of diagnosis. Various organs and tissues can be involved in the pathological process: skin, lymph nodes, external and middle ear, flat bones, bone marrow, liver, spleen, lungs, endocrine glands, gastrointestinal tract, brain.
The article presents a clinical case of histiocytosis diagnosed in a child of 1 month 3 weeks, the clinical manifestations of which were masked under the symptoms of an acute otitis externa.
The description of this clinical case is intended to draw attention to the peculiarities of the course of recurrent otitis externa and otitis media in infants, as the “mask” of these diseases may be histiocytosis.
Key words: acute otitis externa and otitis media, infants, histiocytosis, computerized tomography.
For citation: Molchanova M.V., Alexeenko S.I., Artyushkin S.A. Clinical observation of histiocytosis, proceeding under the mask of an acute otitis externa, in a child of 1 month 3 weeks // RMJ. 2018. № 10(II). P. 102–104.
В статье представлен клинический случай гистиоцитоза, диагностированный у ребенка 1 мес. 3 нед., клинические проявления которого маскировались под симптомы наружного диффузного отита.
Введение
Гистиоцитозы представляют собой группу заболеваний, разнообразных по клиническим проявлениям и прогнозу, которые объединяет пролиферативный процесс в моноцитарно-макрофагальной системе с накоплением в очагах поражения патологических гистиоцитов и формированием специфических гранулем [1–4]. Современная классификация гистиоцитозов включает 3 нозологические формы: гистиоцитоз из клеток Лангерганса, злокачественный гистиоцитоз и вирус-ассоциированный гемофагоцитарный синдром [2, 5].
Гистиоцитоз из клеток Лангерганса — крайне редкое заболевание: в детском возрасте встречаются 3–4 случая на 1 млн населения, у взрослых — 1 случай на 560 000 населения [6–8].
Этиология и патогенез гистиоцитоза до конца не изучены [2, 6, 9]. Возможна иммунопатологическая и опухолевая природа заболевания. В пользу иммунопатологической природы гистиоцитоза свидетельствуют высокая частота спонтанных ремиссий, низкая летальность (у детей — 15%, у взрослых — 3%) и отсутствие хромосомных аномалий в клетках из очагов поражения. В пользу опухолевой природы говорит клональный характер пролиферации клеток Лангерганса в очагах поражения [10].
Клинические проявления гистиоцитоза весьма разнообразны, что определяет трудность диагностики. В патологический процесс могут вовлекаться различные органы и ткани: кожа, лимфатические узлы, наружное и среднее ухо, плоские кости, костный мозг, печень, селезенка, легкие, эндокринные железы, желудочно-кишечный тракт, головной мозг [2, 6, 11].
Среди ЛОР-органов наиболее часто поражаются наружное и среднее ухо с кровянисто-гнойными выделениями из наружного слухового прохода, имитируя таким образом наружный и средний гнойный отит.
Верификация диагноза проводится на основании биопсии пораженных очагов с последующим гистологическим и иммуногистохимическим исследованиями материала [2].
Клинический случай гистиоцитоза
Вашему вниманию предлагается случай своевременно диагностированного гистиоцитоза у ребенка грудного возраста.
Девочка Г., 1 мес. 3 нед., поступила в ЛОР-отделение СПб ГБУЗ «ДГМКЦ ВМТ им. К.А. Раухфуса» в экстренном порядке с жалобами на геморрагические выделения из правого уха.
Из анамнеза заболевания известно, что за 2 нед. до поступления на фоне полного здоровья родители заметили геморрагические выделения из правого уха у девочки в небольшом количестве. Факт травмы родители отрицали. К ЛОР-врачу амбулаторно не обращались. Появившиеся выделения из правого уха повторно побудили родителей обратиться в дежурный ЛОР-стационар.
Из анамнеза жизни известно, что девочка от первой беременности, первых срочных родов. Беременность протекала без особенностей. При рождении: масса тела — 3650 г, рост — 53 см, закричала сразу, оценка по шкале Апгар — 8/8 баллов. Девочка находилась на грудном вскармливании, отмечались достаточные весовые прибавки. Проходила регулярные плановые осмотры в декретированные сроки у педиатра и специалистов в поликлинике по месту жительства. Девочка наблюдается у хирурга, онколога по месту жительства по поводу образования боковой поверхности грудной клетки слева (лимфангиома?).
При поступлении: ребенок в сознании, активен, сон не нарушен, аппетит не снижен. Температура тела 36,5 °С. Общий соматический статус без отклонений от возрастной нормы.
Проведена оценка ЛОР-статуса. Риноскопия: носовое дыхание удовлетворительное. Слизистая носа розовая, носовые раковины обычные, отделяемого нет. Фарингоскопия: слизистая глотки розовая, налетов не обнаружено.

Выполнена отоскопия. AD: заушная область не изменена. Кожа наружного слухового прохода незначительно гиперемирована, инфильтрирована. В наружном слуховом проходе отмечается гнойно-геморрагическое отделяемое. На задневерхней стенке наружного слухового прохода на границе с барабанной перепонкой визуализируется образование розового цвета, однородное, с четкими контурами, размер 7×5,5 мм, при дотрагивании кровоточит. Барабанная перепонка обозрима не полностью, серая. AS: заушная область не изменена. Наружный слуховой проход широкий, свободный. Барабанная перепонка серая, контуры четкие.
Ребенок госпитализирован в ЛОР-отделение, проведено дообследование: клинический анализ крови, общий анализ мочи, копрограмма, бактериологическое исследование патологического отделяемого из правого уха, УЗИ органов брюшной полости, желудка, биохимический анализ крови, ЭКГ, консультация педиатра.
После угасания острого воспалительного процесса наружного слухового прохода справа выполнена компьютерная томография височных костей с внутривенным введением контрастного вещества.
В клиническом анализе крови отмечались признаки анемии легкой степени тяжести (эритроциты 3,09×10 12 , гемоглобин 100 г/л).
В общем анализе мочи, копрограмме, УЗИ органов брюшной полости, желудка патологии не выявлено.
В результате бактериологического исследования отделяемого из наружного слухового прохода справа выделен Staphylococcus aureus, чувствительный к амоксициллину в комбинации с клавулановой кислотой, цефотаксиму, цефтриаксону.
ЭКГ: синусовый ритм с ЧСС 138 уд./мин, нормальное положение электрической оси сердца. Поворот против часовой стрелки (R1, V1–V6); неполная блокада правой ножки пучка Гиса.
Девочка консультирована педиатром. Диагноз: Образование боковой поверхности грудной клетки слева (лимфангиома?). Анемия легкой степени тяжести.
Проведена консервативная терапия: системная антибактериальная терапия (цефтриаксон по 400 мг 1 р./сут в/м 10 дней); антигистаминная терапия (диметинден (капли) по 3 капли 3 р./сут внутрь); интраназально вводился вазоконстриктор (оксиметазолин 0,01% по 1 капле 2 р./сут); местный антибактериальный препарат (в правое ухо: рифамицин по 3 капли 3 р./сут 10 дней).
На фоне проводимой терапии воспалительные явления стихли, однако при отоскопии сохранялось образование на задневерхней стенке наружного слухового прохода справа.
С целью уточнения распространенности процесса назначена компьютерная томография височных костей с внутривенным введением контрастного вещества.
По данным компьютерной томографии височных костей, выполненной по стандартной программе до и после внутривенного введения контрастного вещества, на задней стенке наружного слухового прохода справа определяется мягкотканное образование однородной структуры, овальной формы с четкими контурами, размером 7×5,5 мм. Образование прилежит к барабанной перепонке, несколько смещает ее внутрь, умеренно накапливает контрастный препарат. Просвет наружного слухового прохода в данной области сужен до 1 мм. Костных деструктивных изменений не выявлено. Антрум и барабанные полости с обеих сторон пневматизированы. Слуховые косточки прослеживаются четко. Улитки без особенностей (рис. 1).
В условиях операционной под внутривенным наркозом при отомикроскопическом контроле удалено образование наружного слухового прохода справа. Материал направлен на гистологическое исследование.
По результатам патоморфологического исследования: гистологическая картина лангергансоклеточного гистиоцитоза.
Девочка консультирована детским онкологом. Рекомендован пересмотр блоков и стекол с выполнением иммуногистохимического исследования материала в НМИЦ ДГОИ им. Д. Рогачева.
Катамнез: по результатам гистологического и иммуногистохимического исследования в НМИЦ ДГОИ им. Д. Рогачева диагноз подтвержден. После выписки из ЛОР-отделения ДГМКЦ ВМТ им. К.А. Раухфуса девочка прошла обследование у онколога, другие очаги не выявлены. Системная терапия онкологом не назначалась. В течение года 1 раз в 3 мес. консультируется онкологом, оториноларингологом, ребенку проводится отомикроскопия — отмечается стойкая ремиссия.
Заключение
Описание данного клинического случая преследует цель обратить внимание на особенности течения рецидивирующих наружных и средних отитов у грудных детей, т. к. за маской данных заболеваний может скрываться гистиоцитоз.
Читайте также:
- Влияние аминокислот и гормонов на секрецию инсулина. Инсулин в углеводно-жировом обмене
- Влияние тромболизиса на летальность. Анализ эффективности тромболизиса при инфаркте миокарда
- МРТ лонного сочленения и приводящих мышц во фронтальной проекции в норме
- Причины гипокалиемии. Гиперкалиемия. Признаки гиперкалиемии.
- Побочные реакции лекарственных препаратов
