Лучевая диагностика паразитов панкреатобилиарной системы
Обновлено: 15.05.2024
Методы лучевой диагностики позволяют определить степень местного и отдаленного распространения процесса.
Методы лучевой диагностики нейроэндокринных опухолей:
компьютерная томография (МСКТ),
магнитно-резонансная томография (МРТ, МРХПГ),
позитронно-эмиссионная томография (ПЭТ).
МСКТ и МРТ выполняются с внутривенным введением контрастного препарата. Последние два метода применяются для оценки активности опухоли - оценки ее метаболизма (обмен веществ).
Задачи лучевой диагностики
Выявление патологического образования - нейроэндокринной опухоли.
Дифференциальная диагностика патологических образований.
Оценка распространенности поражения органов и систем.
Стадирование опухолей (TNM).
Оценка эффективности лечения.
Противопоказания к МСКТ
При выборе метода лучевой диагностики учитываются их точность, доступность и наличие противопоказаний.
аллергия на йодсодержащие препараты,
выраженное нарушение функции почек.
Противопоказания к МРТ
МРТ сложно выполнять пациентам в тяжелом общем состоянии, если они не могут задерживать дыхание, в соответствии с требованиями, что препятствует получению качественных диагностических изображения.
первый триместр беременности,
наличие металлических инородных тел,
наличие искусственных водителей ритма,
наличие кохлеарных имплантов,
наличие искусственных клапанов сердца (если нет сертификата, разрешающего проведение МРТ),
наличие эндопротезов крупных суставов и других металлоконструкций (если нет сертификата, разрешающего проведение МРТ).
МСКТ и МРТ имеют разную диагностическую ценность при обследовании того или иного органа. МСКТ - оптимальный метод для обследования легких и органов средостения, мягких тканей шеи, органов брюшной полости и забрюшинного пространства, желудочно-кишечного тракта. МРТ предоставляет исчерпывающую информацию о патологии головного мозга, орбит, органов малого таза (мочевой пузырь, предстательная железа, матка и яичники, прямая кишка), позволяет четко оценить органы брюшной полости и забрюшинного пространства, желчные протоки, специальная методика - МР-энтерография дает представление о патологии тонкого кишечника.

Рисунок 1. Множественные нейроэндокринные опухоли поджелудочной железы. Определяются только на фоне внутривенного введения контрастного препарата.
В 50-90% случаев на поверхности злокачественных клеток нейроэндокринных опухолей (НЭО) наблюдается увеличение количества соматостатиновых трансмембранных рецепторов (somatostatin seven-transmembrane-domain receptor, SSTR). На этом основано применение радионуклидных методов диагностики. При выполнении позитронно-эмиссионной томографии (ПЭТ\КТ) для диагностики НЭО предназначены радиофармпрепараты 68 Ga-DOTA-TATE (DOTA-TATE, меченый галлием-68) и 68 Ga-DOTA-NOC (DOTA-NOC, меченый галлием-68), как обладающие сродством к большинству подтипов SSTR .
Нередко возникают ситуации, когда чувствительность ПЭТ/КТ с 68 Ga-DOTA-TATE и 68 Ga-DOTA-NOC снижена. В таких случаях возникает необходимость выполнения исследования с другим радиофармпрепаратом - 18 F-фтордезоксиглюкозой ( 18 F-ФДГ).
Для установления наиболее эффективного радиофармпрепарата в каждом конкретном клиническом случае необходимо воспользоваться нижеприведённой таблицей. Производится это путём сопоставления двух параметров, полученных из иммуногистохимического: Grade (G) и Ki-67 (параметры агрессивности опухоли).
++: чувствительность метода высокая;
-: чувствительность метода низкая;
+: чувствительность метода одинаковая (ПЭТ/КТ можно выполнить как с 68 Ga-DOTA-TATE и 68 Ga-DOTA-NOC, так и с 18 F-ФДГ).
 |  |
| Рисунок 4. Накопление радиофармпрепарата 68 Ga-DOTA-TATE пораженными лимфатическими узлами у пациента с НЭО прямой кишки. | |
Для проведения и качественной интерпретации данных лучевого исследования (КТ/МРТ/ПЭТ) врачу-рентгенологу необходимо знать цель исследования, результаты лабораторных тестов, данные архива лучевых исследований, важно ознакомиться с выписками и другими медицинскими документами каждого пациента.
Автор статьи: Савельева Татьяна Вячеславовна (врач - рентгенолог)
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Лучевая терапия неоперабельного панкреатобилиарного рака. Непосредственные и отдаленные результаты
Нерешенным и спорным остается и вопрос консервативного лечения ПБР. Исследований в этой области очень мало, со скудным количеством пациентов, а результаты рандомизированих исследований зачастую противоречат друг друга.
Цель исследования. Улучшение результатов лечения неоперабельного ПБР, путем максимальной реализации радикальной программы лучевой терапии (ЛТ).
Материал и методы. Работа основана на анализе результатов лечения 133 больных неоперабельным ПБР, находившихся на лечении в РНЦРР с 1988 по 2012 г. Лучевая терапия при ПБР применялась при противопоказаниях к радикальному хирургическому лечению и\или не возможности его проведения. Абсолютными противопоказаниями для проведения лучевой терапии явились: множественные метастазы, выраженная раковая кахексия, выраженная диарея как симптом ПБР, язвенная болезнь желудка и двенадцатиперстной кишки в фазе обострения, эпизоды кровотечения из опухоли, которая прорастает в просвет двенадцатиперстной кишки и\или желудка, болезнь Крона, язвенный колит, анемия, лейкопения и тромбоцитопения 3-4 степени. Относительными противопоказаниями к лучевой терапии ПБР явились: прорастание опухоли в крупные сосуды, желудок и/или двенадцатиперстную кишку, язвенная болезнь желудка и/или двенадцатиперстной кишки (последнее обострение в течение последнего месяца), длительное (более двух месяцев) время после паллиативных хирургических вмешательств, сопутствующие заболевания, тяжелое общее состояние.
Лучевое лечение проведено 66 (49.6%) больным раком поджелудочной железы, 46 (34.6%) - раком внепеченочных желчных протоков, 21 (15.8%) - раком фатерова соска. Мужчины составили 60,2%, а женщины - 39.8%. При РПЖ преобладание мужчин более весомое, чем при РВЖП. Средний возраст больных составил 64,9 ±11,7. Самый молодой - 35 лет с раком поджелудочной железы, самый старый - 82 года с раком фатерова соска (табл. 1).
Таблица 1. Распределение больных по возрасту
Распределение пациентов с раком поджелудочной железы, внепеченочных желчных протоков и фатерова соска, получивших лучевое лечение, в зависимости от стадии заболевания, представлено в табл. 2.
Таблица 2. Распределение больных в зависимости от стадии заболевания
При раке поджелудочной железы преобладали опухоли со значением Т3 (со стадией T3N0-1M0 - 40 больных), при раке внепеченочных желчных протоков и раке ампулы фатерова соска - T2N1M0, 17 и 8 соответственно.
Общее состояние больных было унифицировано по шкале Карновского. Перед лучевой терапией у 63,4% пациентов с раком поджелудочной железы общее состояние оценивалась 50, 60% активности по шкале Карновского. Общее состояние больных с раком внепеченочных желчных протоков было менее удовлетворительным: у 60,1% больных оно оценивалось 40, 50% активности. Больные с раком ампулы фатерова соска в целом подходили к лечению в более удовлетворительном состоянии: общее состояние 47,6% больных оценивалось как 60-80%, но и у такого же количества пациентов оно оценивалось 40, 50% (табл. 3).
В плане подготовки к проведению лучевой терапии проводились рентгенотопометрические исследования и дозиметрическое планирование лучевой терапии. В поле облучения включались область первичной опухоли и зоны регионарного лимфооттока: перипанкретические узлы (панкреодуоденальные, верхние и нижние панкреатические, панкреатолиенальные), чревные лимфоузлы, лимфоузлы ворот печени и селезенки, ретропанкретические лимфатические узлы: пре- парааортальные лимфоузлы.
Таблица 3. Общее состояние больных перед лучевой терапией
Главной методологической особенностью явилось то, что лучевое лечение проводилось методом последовательно сокращающихся полей. При реализации радикальной программы лучевого лечения СОД составила 50 - 60 Гр на весь объем облучаемых тканей и 66 - 70 Гр - на зону первичной опухоли.
Лучевые реакции стали причиной изменения плана лечения у 18 (13,8%) больных. Им назначались вынужденные перерывы на 5 - 7 дней.
Результаты и обсуждение. Непосредственные результаты лучевой терапии оценивались в зависимости от степени регрессии опухолей, оценка которой проводилась по система RECIST 1.1.
Непосредственные результаты лучевой терапии в зависимости от ответа на лучевую терапию представлены в табл. 4.
Полная и частичная регрессия была достигнута в 28,8% случаях, а при раке фатерова соска - 42,1% случаев. В основном была достигнута стабилизация (62,5%), а прогрессирование наблюдалась только в 8,8% случаях. Самыми худшими были непосредственные результаты лучевой терапии рака внепеченочных желчных протоков: полная регрессия была достигнута лишь в 2,3% случаях, а прогрессирование наблюдалась в 11,4 % случаях.
Таблица 4. Непосредственные результаты лучевой терапии
Непосредственные результаты лучевой терапии оказались лучше при подведении большей СОД. Несмотря на то, что доля больных, у которых наблюдалась стабилизация заболевания, в группах получавших ЛТ в дозах СОД 50-70 Гр и до 50 Гр, практически одинакова, значительно больше прогрессирование заболевания наблюдалось в группе получавших СОД до 50 Гр. Полный ответ был получен только в группе получавших СОД 50-70 Гр (рис. 1).
Рис. 1. Непосредственные результаты лучевой терапии в зависимости от ее дозы
В плане непосредственных результатов лечения также анализировался анальгезирующий эффект лучевой терапии (табл. 5). Анальгезирующий эффект лучевого лечения достигнут у 64 (61,5%) больных.
Таблица 5. Прием анальгетиков до и после лучевой терапии
Количество пациентов, у которых болевой синдром купировался приемом наркотических анальгетических средств (НАС), после лучевой терапии уменьшилось более чем в пять раз (27 больных до и 5 после). Более того, у половины пациентов боли, сохранившиеся после ЛТ, купировались приемом ненаркотических анальгетических средств (ННАС) менее 3 раз в сутки.
При анализе общего состояния пациентов после ЛТ (рис. 2), выяснилось, что пациентов с общим состоянием 70, 80% по шкале Карновского в 2 раза больше, чем до начало лечения. Пациенты с общим состоянием 90% были только после лучевой терапии. Практически одинаковое количество больных с общим состоянием 50, 60% до и после лечения объясняется улучшением и «сдвигом» пациентов с худшим общим состоянием.
Рис. 2. Общее состояние пациентов до и после лучевой терапии
При оценке общей выживаемости рассчитывались медиана выживаемости (МВ) и 3-, 5-летняя выживаемость. Выживаемость больных с раком поджелудочной железы, внепеченочных желчных протоков и фатерова соска после ЛТ в зависимости от стадии заболевания представлены в табл. 6.
Таблица 6. Выживаемость больных после ЛТ в зависимости от стадии заболевания
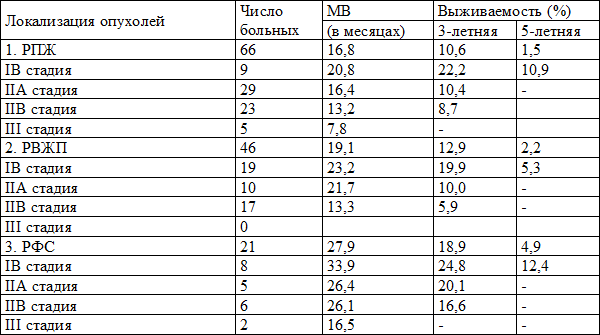
Медиана выживаемости при раке поджелудочной железы составила 16,8 мес., при раке внепеченочных желчных протоков - 19,1 мес., при раке фатерова соска - 27,9 мес. 3- и 5-летняя выживаемость пациентов после лучевой терапии составила: при раке поджелудочной железы - 10,6% и 1,5% соответственно, при раке внепеченочных желчных протоков - 12,9% и 2,2% и при раке фатерова соска - 18,9% и 4,9% соответственно. С нарастанием стадии заболевания отмечалось ухудшение отдаленных результатов. Резкое снижение медианы выживаемости отмечается у пациентов III стадией заболевания (р<0,05). При локализации опухоли в поджелудочной железе она составляет всего 7,8 мес., при раке фатерова соска - 16,5 мес. Никто из больных этой группы не прожил 3 лет.
Отдаленные результаты лучевого лечения больных раком поджелудочной железы, внепеченочных желчных протоков и фатерова соска в зависимости от значений значения Т представлены в табл. 7.
Таблица 7. Выживаемость больных после лучевой терапии в зависимости от значений символа Т

При раке поджелудочной железы, внепеченочных желчных протоков и фатерова соска медиана выживаемости и 3-летняя выживаемость при N0 оказались выше выживаемости при N1 (p<0,05) (табл. 8).
Проведен анализ отдаленных результатов лучевого лечения пациентов раком поджелудочной железы, внепеченочных желчных протоков и фатерова соска в зависимости от непосредственных результатов лечения (табл. 9).
Медиана выживаемости пациентов после лучевой терапии зависит от степени регрессии опухолей. При полной и частичной регрессии медиана выживаемости у пациентов с раком поджелудочной железы составила 23,4 месяца при стабилизации заболевания - 15,1 месяцев, а при прогрессировании - всего 4,4 месяца (p<0,05). Такая же картина наблюдается при раке внепеченочных желчных протоков: медиана выживаемости при полной и частичной регрессии составляет 26,1 месяцев, при стабилизации процесса - 16,2 месяцев и при прогрессировании - 6,1 месяцев (p<0,05).
Таблица 8. Выживаемость больных после лучевой терапии в зависимости от значений символа N

Таблица 9. Медиана выживаемости после лучевой терапии в зависимости от непосредственных результатов
Анализ отдаленных результатов ЛТ пациентов раком поджелудочной железы, внепеченочных желчных протоков и фатерова соска в зависимости от суммарной дозы облучения подтвердил общие закономерности, заключающиеся, в частности, в том, что продолжительность жизни больных после лучевой терапии в прямой зависимости от суммарной очаговой дозы лучевой терапии. Медиана выживаемости и 3-летняя выживаемость в группе получавших СОД 50-70 Гр при РПЖ составили 17,9 месяцев и 12,2% соответственно, при раке внепеченочных желчных протоков - 21,2 месяцев и 14,7% и при РФС - 31,3 месяцев и 24,9% соответственно, что статистически достоверно отличается от тех же показателей в группе получавших лучевой терапии СОД меньше 50 Гр (14,7 месяцев и 7,7% при РПЖ, 16,1 месяцев и 9,9% при РВЖП и 22,1 месяцев и 24,9% при РФС).
Статистически достоверной разницы в медиане выживаемости и 3-х летней выживаемости между мужчинами и женщинами, а так же в отдельных возрастных группах не наблюдалось.
Выводы. Таким образом, применение лучевой терапии при неоперабельном ПБР позволяет достичь регрессии опухолей, а в отдельных случаях их полной резорбции, исчезновения или уменьшения болевых ощущений, улучшения качества жизни. После лучевой терапии лучшая медиана выживаемости и 3- и 5-летняя выживаемость наблюдается при РФС - 27,9 месяцев и 18,9% и 4,9% соответственно. При раке поджелудочной железы эти показатели составили 16,8 месяцев, 10,6% и 1,5% соответственно, при раке внепеченочных желчных протоков - 19,1 месяцев, 12,9% и 2,2%. С нарастанием стадии заболевания, значения символа Т и N отмечалось ухудшение отдаленных результатов. Достоверно лучшие результаты наблюдаются при полной или частичной регрессии опухоли.
Список использованных источников:
1. Беджанян А.Л., Ратникова Н.П., Шатверян Н.П., Скипенко О.Г. Ближайшие отдаленные результаты лечения рака фатерова соска// Анналы хирургической гепатологии. Тез. XII Междунар. конгр. хирургов гепатологов. 2005. Т. 10. №2. С. 141.
2. Борисов А.Е., Березников Е.А., Левин Л.А. Руководство по хирургии печени и желчевыводящих путей. - СПб.: Скифия-принт. 2003. 124 с.
3. Габоян А. С. Хирургическое лечение больных раком органов билиопанкреатодуоденальной области: Автореф. дис. … докт. мед. наук. - М., 2012. - 31 с.
4. Гладина Т.С. Результаты хирургического и комплексного лечения рака поджелудочной железы// Анналы хирургической гепатологии. 1999. Т.4. №1. C. 34-39.
5. Долгушин Б.И., Косырев В.Ю., Синюков Г.Т. Комплексная диагностика опухолей билиопанкреатодуоденальной зоны// Практическая онкология. 2004. Т.5. №2. С. 77-84
6. Касумьян С.А., Алибегов Р.А., Бельков А.В. Хирургическое лечение рака поджелудочной железы и периампулярной зоны// Анналы хирургической гепатологии. 2001. Т. 6. №1. С. 81-87.
7. Кубышкин В.А., Вишневский В.А. Рак поджелудочной железы. - М.: Медпрактика. 2003. 375 с.
8. Лапкин К.В., Пауткин Ю.Ф. Билиопанкреатодуоденальный рак. -М.: Изд-во Университета Дружбы народов. 1991. 110 с.
9. Макаров Е.С., Нечушки М.И. Соверменные возможности лучевого лечения рака органов билиопанкреатобиларной зоны// Практическая онкология. 2004. Т. 5. № 2. С. 135-144.
10. Малярчук В.И., Климов А.Е., Пауткин Ю.Ф. Билиопанкреатодуоденальный рак. - М.: РУДН. 2006. 444 с.
11. Нечипай А.М. Комбинированное лечение местно-распространенного рака внепеченочных желчных протоков. методика, ближайшие и отдаленные результаты// Росс. онкологический журнал. 2002. 1. C. 4-8.
12. Осипенко С.К. Результаты лучевого, комбинированного и комплексного лечения рака поджелудочной железы// Вопросы онкологии. 2001. Т.47. №3. C. 343-347.
13. Патютко Ю.И., Котельников А.Г. Хирургия рака органов билиопанкреатодуоденальной зоны. - М.: Медицина. 2007. 448 с.
14. Bakkevold K., Arnesjo B., Kambestad B. Carcinoma of pancreas and papilla of Vater: symptoms, signs and diagnosis related to stage and tumor site. A prospective multicenter trial in 472 patients// Scand J. Gastroenterology. 1992. V. 27. N. 4. P. 317-325.
15. Chang D.K., Johns A.L., Merrett N.D. et al. Margin clearance and outcome in resected pancreatic cancer// Journal of Clinical Oncology. 2009. V. 27. P. 2855-2862.
16. Conroy T., Desseigne F., Ychou M., et al. FOLFIRINOX versus gemcitabine for metastatic pancreatic cancer// New England Journal Medicine. 2011. V. 12. N. 364(19). P. 1817-1825.
17. Gemmel C., Eickhoff A., Helmstadter L., et al. Pancreatic cancer screening: state of the art. // Gastroenterology. 2009. V. 3. N. 1. P. 89-96.
18. Hazard L. The Role of Radiation Therapy in Pancreas Cancer// Gastrointestinal Cancer Research. 2009. V. 3. P. 20-28.
20. Slavin J., Ghaneh P., Jones L. The future of surgery for pancreatic cancer// Annals of Oncology. 1999. V. 10. N. 4. P. 285-290.
21. Sobrero A., Van Cutsem E. Pancreatic cancer treatment and research: an international expert panel discussion// Annals of Oncology. 2011. V. 22. P. 1500-1506.
Подписано в печать: 04.09.2013
Видно ли паразитов на УЗИ брюшной полости?
Глисты (гельминты) - группа паразитических организмов (червей), которые обитают в человеческом теле и вызывают заболевания и поражение различных органов: печени, желудочно-кишечного тракта и других. Также они могут существовать в частях тел животных, растений.
Заразиться паразитами возможно различными способами:
- При непосредственном контакте с зараженным человеком или животным
- Из-за употребления зараженных продуктов - плохо обработанное мясо, птица, рыба
- Через воду, почву, песок (в том числе во время плавания в открытом водоеме)
- Укусы насекомых (кроме тех, кто таким методом откладывает собственные личинки)
Дети подвержены риску заражения гораздо сильнее, чем взрослые, за счет более слабого иммунитета.
Признаки наличия паразитов в организме
Симптомы заражения гельминтами бывают двух видов: видимые и скрытые.
Первая группа состоит из таких явлений:
- Зуд и жжение в области заднего прохода
- Потеря веса, которая не сопровождается очевидными причинами
- Анемия, слабость
- Постоянная усталость
Вторая же представляет собой обострение ряда иных заболеваний:
- Инфекция - гайморит, стоматит и иные
- Обострение хронических недомоганий
- Признаки аллергии - зуд, высыпания, ринит
- При появлении кишечных паразитов проявляется расстройство желудочно-кишечного тракта - рвота, боли в области живота, понос или запор
- Интоксикация и сопутствующее ей ослабление организма - головокружения, тошнота, мигрень, угнетение нервной системы
Можно ли увидеть гельминтов на УЗИ?
Ультразвуковое исследование - анализ при помощи воздействия звуковых волн высокой частоты, которые испускаются датчиком. Его действие основано на том, что ткани человеческих органов имеют отличную друг от друга структуру и поэтому по-разному отражают такие волны. Результаты отображаются на мониторе врача-диагноста в реальном времени.
Это одно из самых безопасных обследований, которое можно проводить очень часто.
УЗИ брюшной полости позволяет обнаружить паразитов, а также изменения органов, которые эти существа провоцируют. Некоторые виды гельминтов отображаются сами по себе. В иных случаях их можно обнаружить по относительным признакам, которые ультразвук помогает выявить в качестве патологических изменений в органах.
Это могут быть образования или воспаления в печени, поджелудочной железе, желчном пузыре и даже легких и мозге человека.
В отличие от иных способов, данный метод позволяет обнаружить паразитов и в тех случаях, когда они находятся не в желудочно-кишечном тракте. Если ранее наличие глистов уже было установлено, УЗИ можно использовать для нахождения мест их локализации, а также определить обширность поражения.
Какие органы обследуют при подозрении на гельминтов
При обследовании пациента при помощи УЗИ брюшной полости можно обнаружить глистов или результаты их жизнедеятельности. Они располагаются в таких органах, как:
- Печень
- Желчный пузырь и протоки
- Поджелудочная железа
- Желудочно-кишечный тракт
При наличии предпосылок стоит осмотреть при помощи ультразвука и иные органы:
УЗИ помогает определить структуру вышеперечисленных органов, их однородность, наличие или отсутствие в них новообразований, кист и иных нарушений, а также патологическое увеличение или уменьшение их размеров. При появлении симптомов различных заболеваний данный анализ способствует уточнению клинической картины и более точной постановке диагноза и выяснению причин патологического состояния органов.
Признаки паразитов на ультразвуковой сонограмме
При обследовании организма при помощи УЗИ брюшной полости на наличие глистов врач обращает внимание на следующие изменения в строении органов:
- Увеличение печени - оно может стать свидетельством поражения паразитами, которые могут спровоцировать проявление ранее не диагностированного или обострение уже обнаруженного гепатита
- Проблемы в функционировании желчного пузыря и его протоков
- Наличие плотных, воспаленных кист
- Различного рода уплотнения и узлы в поджелудочной железе
Некоторые признаки поражения могут быть найдены и в виде проблем с иными органами:
- Поражение и воспаление легких
- Нарушения в работе мозга
Какие еще методы исследования следует применять?
Часто на УЗИ брюшной полости отображаются не сами паразиты, а признаки их наличия и жизнедеятельности. Поэтому необходимо провести комплекс анализов, не ограничиваясь только ультразвуком.
В группу обследований при подозрении на гельминтов входят:
- Анализ кала на содержание данных организмов и их яиц
- Забор крови на степень содержания эозинофилов - тип лейкоцитов, который убивает чужеродные белки
- Исследование мочи
- Анализ содержимого кишечника
- Исследование желчного пузыря
- Осмотр мышечной ткани
- Состав отделяющейся мокроты из бронхов и легких
- Компьютерная томография - используют и при поиске паразитов в головном мозге, легких, глазах
- Эндоскопия - с ее помощью можно обнаружить паразитов в кишечнике и желудке
- Рентген - чаще всего необходим при диагностике гельминтов в легких, так как в этом органе они наиболее отчетливо видны на результатах лучевой диагностики
Для постановки наиболее точного диагноза врачи рекомендуют использовать не только УЗИ, но и иные методы. Важнее всего, чтобы больной не занимался самолечением, а вовремя обратился к профессионалам, чтобы не навредить самому себе.
Лучевая диагностика паразитов панкреатобилиарной системы
Институт хирургии им. А.В. Вишневского Минздравсоцразвития РФ, Москва
ФГБУ "Институт хирургии им. А.В. Вишневского" Минздрава России, Москва
Чувашский государственный университет им. И.Н. Ульянова, Вторая городская больница, Чебоксары
КТ-диагностика рака поджелудочной железы: современное состояние проблемы
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2011;(8): 98‑102
Захарова О.П., Кармазановский Г.Г., Егоров В.И. КТ-диагностика рака поджелудочной железы: современное состояние проблемы. Хирургия. Журнал им. Н.И. Пирогова. 2011;(8):98‑102.
Zakharova OP, Karmazanovskiĭ GG, Egorov VI. The computed tomography by pancreatic cancer: state of art. Pirogov Russian Journal of Surgery = Khirurgiya. Zurnal im. N.I. Pirogova. 2011;(8):98‑102. (In Russ.).
Проблема диагностики и лечения рака поджелудочной железы (ПЖ) остается актуальной для современной клинической онкологии. Заболеваемость раком ПЖ неуклонно растет как в нашей стране, так и за рубежом. Несмотря на совершенствование методов диагностики, хирургической техники, появление новых противоопухолевых препаратов, разработку комбинированных и комплексных методов лечения больных раком ПЖ, общая 5-летняя выживаемость не превышает 5-20% [3].
Хирургическое удаление опухоли продолжает оставаться единственным методом радикального лечения больных раком ПЖ, которое позволяет получать обнадеживающие результаты. Неудовлетворительные результаты лечения связаны в первую очередь с поздней диагностикой данного заболевания, когда опухолевый процесс принимает распространенную форму и применить радикальное лечение невозможно. В свою очередь полнота хирургической резекции (R0/R1/R2) зависит от точности предоперационного и интраоперационного выявления опухоли. Мультидетекторная КТ (МДКТ) является наиболее информативной предоперационной методикой для установления резектабельности рака ПЖ. Чувствительность и специфичность ее составляет 90 и 99% соответственно [2, 27]. Одно из наиболее ценных преимуществ МДКТ - возможность мультипланарной реконструкции (МПР) изображений и создания трехмерных изображений. МПР позволяет достичь хорошего качества изображения с высоким разрешением, изучить зоны интереса во фронтальной, сагиттальной и других плоскостях на основе заданной кривой, делая изображение более наглядным и привычным для клиницистов. МПР, выполненные в различных плоскостях, помогают детализировать топографоанатомические соотношения. Трехмерное моделирование на основе МДКТ с болюсным контрастным усилением делает возможным создание объемных изображений анатомических зон, в которых показаны соотношения патологического очага, сосудов и окружающих органов [1]. Именно эти реконструкции позволяют хирургам наглядно оценить получаемые при КТ изображения, увидеть нужные объекты в таких ракурсах, которые в реальных условиях, на операционном столе, недостижимы (например, сзади, «изнутри» и т.д.).
Изображения, полученные после обработки данных, значительно расширяют диагностические возможности КТ, улучшают визуализацию панкреатических сосудов и протоков ПЖ. Наиболее часто используемые методы постпроцессорной обработки данных: проекция максимальной интенсивности, объемные построения, проекции минимальной интенсивности и криволинейные плоскости. В литературе встречается множество данных о том, что МПР изображений значительно повысила диагностические способности МДКТ в выявлении опухолей ПЖ, особенно малых размеров [12, 17, 19, 26].
Использование МДКТ-ангиографии с трехмерной реконструкцией изображений дает возможность выявить пути парапанкреатической, периневральной и лимфатической инвазии аденокарциномы ПЖ [6, 21]. При раке панкреатобилиарной области парапанкреатические лимфатические сосуды поражаются довольно часто, что имеет прогностическое значение. Однако в литературе очень мало данных посвящено КТ-визуализации нормальной и патологически измененной парапанкреатической лимфатической системы. При поражении раком головки ПЖ инфильтрация наиболее часто обнаруживается вдоль общей печеночной артерии, а при поражении тела и хвоста ПЖ - вокруг чревного ствола. Знание нормальной КТ-анатомии лимфатической системы области ПЖ позволяет выявлять ее патологические изменения, что существенно для точного стадирования рака.
Проведение МДКТ-ангиографии ПЖ стало неотъемлемой частью подготовки к любой операции на органах панкреатобилиарной области. При предоперационной оценке главными задачами являются: локализация аденокарциномы ПЖ, стадирование и определение локальной резектабельности и анатомических вариантов расположения сосудов в данной зоне.
МДКТ - предпочтительный метод диагностики и определения резектабельности аденокарциномы ПЖ. Единственным ограничением МДКТ в предоперационной оценке рака ПЖ является сравнительно низкая чувствительность в определении метастазов в печень малых размеров, метастазов в лимфатические узлы и диагностике канцероматоза [4]. Точность определения вовлечения лимфатических узлов при КТ, в том числе и при динамическом исследовании, низкая, так как даже лимфатические узлы размером 1-2 мм могут содержать метастатические клетки. G. Zamboni и соавт. [27] определяют лимфатические узлы как пораженные при длине короткой оси ≥1см. Однако в клинической практике низкая точность МДКТ в определении метастатического поражения регионарных лимфоузлов имеет ограниченное значение, поскольку наиболее часто поражаются парапанкреатические лимфоузлы, которые удаляют единым блоком с опухолью [13].
Дооперационное изучение анатомической вариации сосудистой ангиоархитектоники имеет ключевое значение в оценке резектабельности опухоли и в положительном исходе операции. По сравнению с интраоперационными данными МДКТ-ангиография демонстрирует 100% точность в выявлении вариаций ангиоархитектоники целиакомезентериального русла, гемодинамически значимых стенозов, обструкций и аневризм, что существенно влияет на выбор оперативного вмешательства [7]. Особенности анатомии венозного русла, осложняющие венозную реконструкцию или делающие ее вообще невозможной, включают множественные тощекишечные ветви, впадающие в верхнюю брыжеечную вену вблизи конфлюенса воротной вены. Варианты артериальной анатомии, исключающие возможность операции: низкое отхождение общей печеночной артерии от чревного ствола с расположением под воротной веной, а также отхождение общей печеночной артерии от верхней брыжеечной артерии и ее распространение через ретроперитонеальный край резекции мягких тканей. Эти особенности ангиоархитектоники делают опухоли нерезектабельными, несмотря на возможность их удаления при нормальной сосудистой анатомии. Вместе с тем измененная ангиоархитектоника может поспособствовать возможности резекции. Например, при отхождении общей печеночной артерии непосредственно от аорты (чревный ствол снабжает кровью только селезеночную и гастродуоденальную артерии) или при добавочной правой и левой печеночных артериях, отходящих от верхней брыжеечной артерии и левой желудочной артерии соответственно [10].
МДКТ-ангиография позволяет хирургам не только ознакомиться с сосудистой анатомией пациента до планирования оперативного вмешательства, но и с высокой точностью определить поражение сосудов, что может значительно изменить объем операции.
Результаты диагностики помогают хирургам дооперационно оценить хирургические детали и прогноз, однако иногда ошибочные выводы, полученные по результатам исследования, ведут к неуместной терапии [28]. Избежать диагностических ошибок и повысить точность определения резектабельности и нерезектабельности опухоли можно, зная КТ-критерии вовлечения сосудов, метастатического поражения и инвазии смежных органов. Точное определение распространенности опухоли на дооперационном этапе позволяет правильно построить алгоритм лечения и ведения больного, выявлять пациентов, которым поможет радикальный хирургический подход, и тех, кому вначале необходимо проведение неоадъювантной химиотерапии с последующей резекцией опухоли ПЖ. В специализированных центрах подобные данные незаменимы для хирургов, поскольку при погранично-резектабельном раке головки ПЖ имеется высочайшая степень риска получить по результатам гистологического исследования положительный край резекции после операции. Поэтому повсеместное распространение получил мультимодальный подход к диагностике и лечению таких пациентов, включающий предварительную химиотерапию или химиолучевое лечение перед операцией [25].
Раньше определить опухоль как резектабельную, погранично-резектабельную или нерезектабельную можно было лишь интраоперационно. Современные методы визуализации с улучшенным качеством изображения дают возможность предоперационного стадирования. Различные школы расходятся во мнениях относительно предпочтительного метода диагностики и критериев резектабельности опухоли ПЖ.
Авторы из Онкологического центра и исследовательского института Г. Ли Моффита (США) предлагают универсальный алгоритм предоперационной оценки состояния больных, включающих МДКТ-исследование со стандартным для ПЖ двухфазным тонкосрезовым протоколом, эндоскопическое ультразвуковое исследование (высокая точность в определении опухолей

На рис. 1 Рисунок 1. Алгоритм предоперационного обследования. УЗИ - ультразвуковое исследование; эндоУЗИ - эндоскопическое ультразвуковое исследование; ТИБ - тонкоигольная биопсия; РХПГ - ретроградная холангиопанкреатография; МТС - метастазы. представлен алгоритм стратегии предоперационного стадирования аденокарциномы ПЖ, используемый в больнице штата Массачусетс США. Данный алгоритм подчеркивает центральную роль МДКТ как первой ступени в диагностике при подозрении на рак ПЖ [18].

N. Buchs и соавт. [15] предложили алгоритм ведения пациентов с раком ПЖ при подозрении на сосудистую инвазию (рис. 2). Рисунок 2. Алгоритм ведения пациентов с раком ПЖ при подозрении на сосудистую инвазию. ЭндоУЗИ - эндоскопическое ультразвуковое исследование; ЛУЗИ - лапароскопическое ультразвуковое исследование; ВСУЗИ - внутрисосудистое ультразвуковое исследование.
Многие авторы подчеркивают, что при контакте опухоли и сосуда на ≤180° вероятность сосудистой инвазии составляет около 40%. При инфильтрации опухоли >180° окружности сосуда вероятность инвазии сосуда составляет 80%. Когда окружность сосуда инфильтрирована на >270°, со 100% вероятностью можно говорить об инвазии сосуда. Также общепринято, что наличие каплевидной деформации верхней брыжеечной вены (которая в норме округлая или овальная на аксиальных изображениях) является достоверным признаком ее инфильтрации (данный признак описан Hould и соавт. как специфичный при вовлечении верхней брыжеечной вены) [12, 16].
Необходимо помнить, что КТ-признаки перипанкреатической инвазии артерий и вен различаются. Для повышения точности диагностики сосудистой инфильтрации и правильной оценки резектабельности опухоли очень важно обращать внимание на эти различия и уметь правильно интерпретировать данные КТ [11, 14]. По мнению авторов, главная причина различия КТ-признаков сосудистой инвазии артерий и вен заключается в том, что стенки вен тоньше и податливее стенок артериальных сосудов. Когда опухоль окружает вену, ее стенки становятся неровными и калибр вены уменьшается. Скорость тока крови по венам низкая, опухоль зачастую пенетрирует стенку, формируя венозный тромбоз, следствием которого является окклюзия. У артериальных сосудов, наоборот, стенки толще и более упругие, калибр артерий меньше, поэтому даже когда артерии располагаются в структуре опухоли, калибр их зачастую не меняется, а стенки остаются ровными.
H. Li и соавт. [11] к критериям инвазии артерий по данным КТ относят их расположение в структуре опухоли/окружение сосуда опухолью более чем на 50% его диаметра в сочетании с неровностью стенки или уменьшением калибра артерии (чувствительность и специфичность данных критериев равнялись 79 и 99% соответственно). К критериям инвазии вен авторы относят наличие одного (и более) из следующих признаков: венозная облитерация, окружение вены опухолью более чем на 50% ее диаметра, неровность стенки, уменьшение калибра вены и каплевидная деформация верхней брыжеечной вены (чувствительность и специфичность данных критериев равнялись 92 и 100% соответственно).
M. Horton и E. Fishman [8] при диагностике берут за основу не процент инфильтрации опухолью окружности сосуда, а изменение калибра артерий. В то же время C. Valls и соавт. [24] расценивают соприкосновение опухоли и артерии на любом протяжении как признак нерезектабельности.
Несмотря на развивающиеся возможности визуализации панкреатобилиарной области, в некоторых ситуациях довольно сложно достоверно отличить резектабельную (стадия I-II) от местно-распространенной опухоли (стадия III). Для таких случаев введен термин «погранично резектабельный» рак (borderline resectable), критериями которого являются поражение печеночной артерии (на >180° окружности или >50% сечения артерии) на коротком отрезке без инфильтрации чревного ствола (обычно на уровне гастродуоденальной артерии) при возможности резекции с последующей реконструкцией, инфильтрация верхней брыжеечной артерии на ≤180° окружности артерии или окклюзия верхней брыжеечной вены, воротной вены, области конфлюенса на коротком промежутке (при возможности последующей реконструкции сосудов в случае необходимости) [25].
Нет общего мнения о возможной степени вовлечения сосудов венозного русла в опухолевый инфильтрат для определения опухоли как погранично резектабельной (т.е. имеющей высокий риск микроскопически положительного края резекции после операции). Необходимо внедрение обобщающего определения «пограничной резектабельности» как для клинических исследований, для сравнения результатов различных школ, так и для оценки ведения больного [5].
Панкреатодуоденальная резекция - сложная, но потенциально излечивающая операция при аденокарциноме ПЖ. O. Strobel и соавт. [22] рекомендуют динамическое наблюдение за больными после перенесенной операции по поводу опухоли, а также агрессивное оперативное лечение в случае местного рецидива опухоли.
МДКТ является методом выбора при обследовании пациентов, перенесших панкреатодуоденальную резекцию. Как местный, так и отдаленный рецидив опухоли можно визуализировать при МДКТ, а также дать оценку лимфаденопатии, обусловленной метастатическим поражением. Признаком местного рецидива опухоли служит наличие образования с неровными контурами в проекции ложа удаленной головки ПЖ или инфильтрация мягких тканей в зоне операции. Эти изменения могут распространяться вдоль верхних брыжеечных сосудов или воротной вены. Ключевым моментом является дифференциальная диагностика послеоперационных воспалительных изменений и рецидива заболевания. Увеличение размеров выявленного образования при КТ в динамике позволяет дифференцировать местный рецидив заболевания от послеоперационных воспалительных изменений. Отсутствие четкой жировой прослойки между брыжеечными сосудами, периваскулярная муфта и наличие обструкции прилежащей кишки являются в большей степени признаками рецидива опухоли, чем послеоперационными изменениями [9].
Новые возможности и клинические приложения привели к более широкому использованию МДКТ, что в целом увеличило лучевую нагрузку пациента [23], все же суммарно информативность МДКТ в предоперационной оценке рака ПЖ перевешивает потенциальный риск от полученной дозы облучения. Поэтому при подозрении на наличие образования ПЖ рекомендовано выполнение МДКТ, а для снижения лучевой нагрузки многие исследователи пытаются уменьшить количество фаз контрастного усиления (так, рекомендуемый протокол исследования для пациентов с подозрением на рак ПЖ включает две фазы сканирования с контрастным усилением). При послеоперационном мониторинге проводят исследование с меньшей лучевой нагрузкой (одна фаза сканирования с контрастным усилением, толщина среза 5-7 мм) [20].
Таким образом, протоковая аденокарцинома является абсолютно преобладающей опухолью поджелудочной железы с крайне высоким потенциалом злокачественности. При этом результаты лечения в значительной мере зависят от ранней диагностики и правильного стадирования опухоли. КТ - метод выбора при диагностике и оценке резектабельности рака поджелудочной железы, а совместное использование дополнительных методов исследования (МРТ, эндоУЗИ, ПЭТ/КТ) позволит улучшить точность диагностики и избежать ошибок при стадировании и оценке резектабельности опухоли.
Поджелудочная железа — как понять, что не так
Поджелудочная железа - орган пищеварительной системы, вырабатывающий пищеварительные ферменты и гормоны, регулирующие белковый, углеводный и жировой обмен. Она расположена в нижнем отделе брюшной полости, за желудком, возле двенадцатиперстной кишки, на уровне І-ІІ поясничных позвонков. Длина органа до 22 см, вес - 70-80 г. Она покрыта тонкой соединительной капсулой, основное вещество под ней разделено на сегменты, между ними есть соединительные тяжи с выводными протоками, сосудами, нервами. Для вывода произведенных пищеварительных ферментов и других веществ имеет главный и добавочный проток.
Если нормальное функционирование поджелудочной железы нарушается, в ней развивается воспалительный процесс. Группа заболеваний, для которых характерно воспаление в тканях этого органа, нарушение его работы называется панкреатитом. Воспаление поджелудочной железы - опасное заболевание, сопровождающееся сильной болью, нарушением работы пищеварительной и эндокринной системы. Если человек своевременно не получает медицинской помощи, возможно развитие осложнений, вплоть до летального исхода.
Как лечить воспаление поджелудочной железы
Обнаружив у себя симптомы заболевания поджелудочной железы, обращайтесь к врачу. Он выявит причины заболевания и назначит медикаментозное лечение, диету. Если воспалительный процесс вызван закупоркой выводных протоков, для спасения жизни пациента может потребоваться срочное оперативное вмешательство.
Пациентов с острой формой панкреатита госпитализируют в стационар, где врачи постоянно контролируют их состояние, изменение показателей в общем и биохимическом анализах крови, анализах мочи.
Чтобы организм человека победил заболевание, недостаточно медикаментозного лечения. Для успешного выздоровления, или снятия приступов при хроническом течении заболевания нужен холод, голод и покой. Пациенту полезен постельный режим. В первые три дня рекомендуется полный отказ от пищи, питательные вещества вводятся внутривенно. Для снятия болевых симптомов на живот кладется холодный компресс.
Причины заболевания
Воспалительные процессы в поджелудочной железе могут возникать:
- из-за злоупотребления спиртными напитками - наиболее распространенная причина заболевания у мужчин;
- после травм живота, операций, когда были повреждены ткани или протоки этого органа;
- из-за неправильного питания - воспаление может развиваться, если в рационе человека преобладает фаст-фуд, жирные, острые, копченые, жареные блюда;
- при желчнокаменной болезни - у женщин она развивается в 3-5 раз чаще, чем у мужчин, и желчные конкременты могут закупоривать протоки, из-за чего нарушается отток пищеварительных ферментов и они начинают переваривать ткани железы;
- из-за нарушенного обмена веществ при ожирении, сахарной диабете, во время беременности или после родов;
- из-за длительного приема антибиотиков, кортикостероидов, гормональных препаратов;
- из-за генетической предрасположенности - у некоторых мужчин, а чаще у женщин, поджелудочная железа вырабатывает более густой секрет, он медленней выводится по протокам, и даже однократное злоупотребление спиртными напитками, жирной, жареной пищей может спровоцировать приступ панкреатита;
- после отравлений - пищевых, алкогольных, при работе с лаками, красками и вдыхании их паров, другими отравляющими веществами.
Формы панкреатита
При первом приступе врач ставит диагноз острый панкреатит. При соблюдении диеты, других врачебных назначений, приеме медикаментов, воспаление может пройти без последствий. Если человек ответственно относится к своему здоровью, правильно питается, отказывается от алкоголя, курения, следит за весом, приступ может не повторяться.
Но при систематических нарушениях, поджелудочная железа работает с повышенной нагрузкой, ее состояние ухудшается и заболевание переходит в хроническую форму. Если повторный приступ возникает менее чем через 6 месяцев после первого, ставится диагноз острый рецидивирующий панкреатит. Если приступы повторяются больше, чем 6 месяцев, диагноз - хронический панкреатит. Он имеет две фазы: обострение и ремиссия. При соблюдении диеты, применении поддерживающей терапии, ремиссия длится годами, не возникает острых приступов.
Симптомы воспаления поджелудочной железы
При остром и хроническом панкреатите появляются разные симптомы.
Острая форма
При остром приступе пациент ощущает сильную боль в подреберье. В зависимости от расположения и размера очага воспаления она может быть правосторонней, левосторонней или опоясывающей.
Другие признаки, указывающие на воспалительный процесс в поджелудочной железе:
- отрыжка с тухлым запахом, икота;
- непреходящая тошнота, неоднократная рвота;
- жидкий стул несколько раз в сутки или запор;
- повышение температуры;
- ощущение сухости во рту;
- перепады артериального давления;
- усиленное потоотделение;
- нездоровый цвет кожи, возможно появление коричневых пятен, синяков над пупком или на спине в области поясницы.
Большинство из этих признаков, кроме острой боли, наблюдаются и при алкогольной интоксикации. Болезнь у мужчин не всегда своевременно диагностируется - болевые симптомы пациенты некоторое время снимают обезболивающими препаратами и надеются на улучшение самочувствия, когда пройдет похмелье. Это может быть опасно для жизни. Если после употребления больших доз алкоголя возникает боль в пояснице, подреберье, проверьте поджелудочную железу.
Хроническая форма
Зная, как болит поджелудочная железа, можно не пропустить первые признаки развития хронического воспалительного процесса. Своевременное обращение к врачу поможет избежать осложнений, инфицирования, гормональных нарушений в организме.
Признаки боли в поджелудочной железе:
- тупая ноющая;
- ощущается в верхней части живота;
- может отдавать в грудную клетку, поясницу, нижнюю часть живота;
- усиливается после употребления спиртных напитков, жареной, копченой, острой, жирной пищи, маринадов, приступ может спровоцировать чашка кофе, выкуренная натощак сигарета;
- усиливается после стресса.
Сложно поставить диагноз только по характеру болевых симптомов. При панкреатите появляются другие признаки нарушений в работе организма. Обратитесь к врачу, если вы часто ощущаете ноющую боль в области спины или живота, кожа приобретала желтоватый оттенок, пропал аппетит, снижается вес. Аналогичные признаки у женщин могут наблюдаться во время беременности, и ошибочно принимаются за проявления токсикоза. Чтобы не пропустить опасное заболевание, с первых недель беременности женщинам нужно регулярно посещать женскую консультацию, сдавать анализы крови и мочи.
Если не лечить хронический панкреатит, воспаление может распространяться на другие органы пищеварительной системы, нарушается работа эндокринной системы, что увеличивает риск развития сахарного диабета, онкологических заболеваний.
Лечение
Панкреатит - это группа заболеваний, при которых развиваются воспалительные процессы в поджелудочной железе. Чтобы эффективно лечить его, врач должен определить характер и локализацию воспаления, причину, вызвавшую приступ. После оказания первой помощи и снятия острых болевых ощущений проводится обследование.
Диагностика
Чтобы подтвердить диагноз и оценить состояние пациента, гастроэнтеролог использует лабораторные и инструментальные методы диагностики:
- общий и биохимический анализ крови - выявляют признаки и показывает количественные характеристики воспаления, определяют уровень билирубина, ферментов;
- анализ мочи - показывает уровень ферментов;
- анализ кала на паразитов - назначается по при подозрении, что протоки поджелудочной железы закупорены паразитами;
- УЗИ - показывает размер железы, уплотнения, фиброзные участки;
- рентгенография (если есть возможность, назначается более информационное обследование эндоскопическая ретроградная холангиопанкреатография) - назначается для обнаружения камней или других тел, закупоривающих протоки;
- зондирование - характеризует внешнесекреторную функцию железы;
- МРТ или КТ - выявляют некроз тканей, границы пораженных областей.
Особенности терапии
При остром приступе пациента госпитализируют в стационар, где проводят детоксикацию, очистку кишечника, брюшины.
Для снятия острых болей применяют спазмолитические и болеутоляющие препараты, на живот кладется холодный компресс. Ограничивают двигательную активность. Чтобы снизить секрецию гормонов при снижении проходимости протоков или их закупорке, назначают Платифиллин или Атропин. Для предотвращения инфицирования и снятия воспаления применяют антибиотики. В первые дни показан полный отказ от пищи, питательные вещества вводятся внутривенно. Через 3-5 дней в рацион вводят жидкие каши, одновременно с приемом ферментов: Панкреатина, Мезим-Форте. Чтобы избавить пациента от тошноты, назначается Мотилиум или Церукал.
Профилактика новых обострений
Чтобы избежать новых обострений панкреатита, нужно правильно питаться, отказаться от алкоголя, сигарет, избегать стрессов. Есть нужно небольшими порциями 5-6 раз в день. Исключите из рациона жареные, жирные, копченые продукты, пряности, маринады. Отваривайте, запекайте или готовьте блюда на пару. Откажитесь от кофе, сладких газированных напитков. Регулярно принимайте назначенные врачом препараты, поддерживающие работу поджелудочной железы.
Читайте также:
