Доступ и ход операции дренирования абсцесса печени
Обновлено: 18.05.2024
ГБУЗ «ГКБ №1 им Н.И. Пирогова» ДЗ Москвы, Москва, Россия
ФГБОУ ВО «Российский научно-исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, кафедра факультетской хирургии №1, Москва, Россия
Абсцесс печени вследствие пенетрации инородного тела желудка
Журнал: Эндоскопическая хирургия. 2017;23(2): 39‑42
Проглатывание инородного тела и твердых частиц пищи часто встречается в клинической практике (табл. 1). Большинство случаев проглатывания инородных тел наблюдаются в педиатрии и не требуют какого-либо специального лечения. Однако в 10—20% случаев требуется эндоскопическое удаление, а в менее чем 1% — хирургическое вмешательство для извлечения инородного тела или для лечения развившихся осложнений [1, 2]. Застревание твердых частиц пищи в пищеводе встречается с частотой 13 на 100 000 человек [1, 3, 4]. Проглатывание истинных инородных тел как намеренно, так и ненамеренно, встречается гораздо чаще у пожилых людей, у пациентов с психическими расстройствами и умственно отсталых или находящихся в алкогольной интоксикации, у заключенных с целью членовредительства. По обобщенным данным, частота и уровень локализации инородных тел в ЖКТ примерно таковы: пищевод — 68,4%, желудок — 18,9%, тонкая кишка — 7,1%, толстая кишка — 3%, прямая кишка — 2,6%. Задержка госпитализации, длительное наблюдение и запоздалые операции ведут к развитию большого числа осложнений, частота которых колеблется от 17,8 до 64,1% [2, 3].
Таблица 1. Классификация инородных тел
Большинство остроконечных инородных тел желудка не вызывают симптомов и выводятся самостоятельно, однако процент осложнений от остроконечных инородных тел достигает 35% [1, 5].
Большинство истинных инородных тел могут быть обнаружены при помощи обзорной рентгенографии органов брюшной и грудной полости, однако тонкие металлические предметы, дерево, пластик и стекло, рыбные и куриные кости могут остаться незамеченными (табл. 2). Ложноотрицательные результаты рентгеновского исследования инородного тела достигают 87%.
Таблица 2. Классификация инородных тел по радиопоглощению
Наиболее часто проглатываются рыбные кости и кости иного происхождения. Однако рентгенограммы не всегда обнаруживают рентгенопозитивные инородные тела, особенно рыбные кости, так как большие массы мягких тканей и жидкость могут «застелить» содержание кальция в кости, в особенности у тучных пациентов [3]. Проспективное исследование, проведенное у 358 пациентов, проглотивших рыбные кости, показало, что рентгенположительный результат выявлен только у 32%. В этом случае компьютерная томография (КТ) с чувствительностью от 90 до 100% и специфичностью от 93,7 до 100% значительно превосходит рентгенографию. КТ показывает размеры, форму, локализацию, глубину застрявшего инородного тела, состояние окружающей ткани, что важно для назначения лечения и оценки рисков эндоскопического лечения. КТ не только предоставляет лучшую анатомическую информацию, но может обнаружить и такие осложнения, как формирование абсцесса, медиастинит или аорто-трахеальные свищи [6].
Перфорация желудка инородным телом является казуистикой (менее 1% от всех случаев перфорации ЖКТ) и в литературе упоминаются лишь единичные случаи: один из них описан М. Rygl, К. Pycha в 2002 г. — инородное тело желудка (ложка) у 15-летней девочки, страдающей неврогенной анорексией, проявилось перфорацией через 6 мес после проглатывания; 3 случая перфорации антрального отдела желудка рыбной костью описаны в 2005 г. в Сингапуре К. Brian и P. Goh [2, 7].
Мы приводим случай успешного лечения пациента с инородным телом желудка, осложнившимся формированием абсцесса печени.
Пациент П., 46 лет, поступил в клинику в экстренном порядке, с клинической картиной абсцесса 3-го сегмента печени, подтвержденной данными УЗИ органов брюшной полости.
Объективно: температура 37,7 °С, живот умеренно болезненный в эпигастрии, правом подреберье, симптом Ортнера, перитонеальные симптомы отрицательные. По средней линии живота старый послеоперационный рубец вследствие лапаротомии по поводу проникающего ножевого ранения.
Из анамнеза: пациент считает себя больным в течение 3 нед, когда впервые отметил появление болей в эпигастрии, правом подреберье, повышение температуры тела до 39,5 °С; лечился самостоятельно: принимал курс антибиотиков (амоксиклав 7 дней), нестероидные противовоспалительные средства — с незначительным положительным эффектом. В связи с сохраняющимися жалобами и лихорадкой обратился в стационар. При сборе анамнеза данных за выезд за рубеж, контакт с крупным рогатым скотом, перенесенный сепсис, инфекционные заболевания не выявлено.
Результаты лабораторных исследований: лейкоциты (WBC) 11,7·10 9 /л; гемоглобин (HGB) 134 г/л, биохимический анализ крови — без отклонений от нормы. Начато проведение антибактериальной терапии (ципрофлоксацин 400 мг 3 раза в день в/в, метронидазол 500 мг 3 раза в день в/в). Учитывая неясный генез образования абсцесса, с целью дообследования была выполнена КТ органов брюшной полости с в/в болюсным усилением, по результатам которого выявлено инородное тело, располагающееся в передней стенке выходного отдела желудка (рис. 1, 2), размерами 30×2 мм с пенетрацией в паренхиму S3 печени и формированием абсцесса 45×35×30 мм (рис. 3, 4).

Рис. 1.ПациентП. КТоргановбрюшнойполостивнативномрежиме. Визуализируются инородное тело и абсцесс печени.

Рис. 2. Пациент П. КТ органов брюшной полости с 3D-реконструкцией. Визуализируется инородное тело.

Рис. 3. Пациент П. КТ органов брюшной полости в венозную фазу, фронтальный срез. Визуализируются инородное тело и абсцесс печени.

Рис. 4. Пациент П. КТ органов брюшной полости в венозную фазу, аксиальный срез. Визуализируется абсцесс печени.
Первым этапом выполнены пункция и дренирование абсцесса 3-го сегмента печени под УЗ-контролем. На следующие сутки с целью эндоскопического удаления инородного тела выполнена эзофагогастродуоденоскопия: при тщательной ревизии слизистой желудка данных за наличие инородного тела не выявлено. Контрольная мультиспиральная компьютерная томография органов брюшной полости, выполненная на 2-е сутки с контрастированием желудка pe ros показала: полость абсцесса дренирована адекватно, скудное количество газа по ходу дренажа, сохраняется инородное тело в стенке желудка, признаков выхода контраста за пределы желудка не выявлено (рис. 5).

Рис. 5. Пациент П. КТ органов брюшной полости после дренирования абсцесса в нативном режиме. Визуализируются инородное тело в стенке желудка, дренаж в полости абсцесса.
Больному продолжен курс консервативной терапии, включая антибактериальную, с положительным эффектом: гипертермии, болей в животе, признаков системной воспалительной реакции нет. В течение 4 дней отмечалось мутное отделяемое по дренажу с дебитом около 10 мл в сутки, дренаж ежедневно промывался. На 5-е сутки пациент в удовлетворительном состоянии выписан, рекомендована повторная госпитализация для хирургического удаления инородного тела.
Через 14 дней выполнена операция: видеолапароскопия, адгезиолизис, удаление инородного тела из брюшной полости, ушивание стенки желудка. При этом в верхнем этаже брюшной полости отмечен выраженный спаечный процесс с формированием воспалительного инфильтрата, распространяющегося на желудок, левую долю печени и большой сальник (рис. 6).

Рис. 6. Пациент П. Видеолапароскопия. Визуализируется воспалительный инфильтрат, распространяющийся на желудок и левую долю печени.
При разделении инфильтрата выявлено инородное тело (рыбная кость, рис. 7, 8), исходящее из стенки желудка. Выполнено удаление инородного тела с последующим ушиванием дефекта серозно-мышечного слоя желудка отдельными узловыми швами.

Рис. 7. Пациент П. Видеолапароскопия. Инородное тело желудка (кость) .

Рис. 8. Пациент П. Извлеченное инородное тело желудка (кость) .
Течение послеоперационного периода неосложненное. 05.09.16 больной в удовлетворительном состоянии выписан под наблюдение хирурга поликлиники по месту жительства. 08.09.16 при амбулаторном осмотре пациенту удален дренаж из абсцесса печени.
Заключение
Инородное тело желудка (кость) может мигрировать в соседние органы, в данном случае — в печень, с образованием абсцесса, без развития клиники перфорации полого органа и перитонита.
Разрешение этой ситуации возможно с применением пошагового, малоинвазивного подхода. Первый этап — перкутанное дренирование абсцесса печени под контролем УЗИ, второй — лапароскопическое удаление инородного тела из брюшной полости.
Доступ и ход операции дренирования абсцесса печени
Хасанов А.Г. 1 Шайбаков Д.Г. 1 Шамсиев Р.Э. 1 Фаязов Р.Р. 1 Бадретдинов А.Ф. 1 Бакиров С.Х. 1 Махиянова Д.Р. 1 Шайбакова К.Д. 1
Гнойные заболевания печени в хирургии встречаются редко, но протекают тяжело. До широкого внедрения в медицинскую практику ультразвукового исследования (УЗИ) диагностика абсцессов печени была трудной проблемой.Ограниченные гнойники печени среди госпитализируемых больныхвстречаются нечасто (до 0,16%), но, как правило, требуют хирургического лечения, сопровождающегося высоким риском серьезных послеоперационных осложнений.В последние годы в хирургии для диагностики и лечения заболеваний печени, в том числе абсцессов, широко используют УЗИ и компьютерную томографию (КТ). Точность диагностики и снижение летальности при абсцессах печени часто связаны с внедрением в хирургическую практику УЗИ, КТ, а также внедрением малоинвазивных хирургических технологий. В представленной статье проанализирован пятилетний опыт наблюдения, диагностики и лечения 19 больных с абсцессами печени по материалам хирургических отделений ГБУЗ ГКБ №8 г.Уфы.Мы добились выздоровления всех 19 пациентов путем пункционной аспирации (12 человек) и дренирования (7 человек) абсцессов.Для санации внутрипеченочных гнойников 8 пациентам было достаточно однократной пункции, в 3 случаях потребовалась двукратная и в 1- трехкратная пункция. Дренирование абсцессов проводилось катетерами pig tail диаметром 8-12 Fr. При абсцессах менее 10 см в диаметре было достаточно дренирования одним микродренажом (5 больных). При больших размерах абсцесса (более 10 см в диаметре) с выраженной капсулой полость абсцесса дренировали двумя катетерами (2 случая). При пункционном лечении абсцессов печени наблюдалось два осложнения. Было однокровотечение при эвакуации содержимого абсцесса при помощи медицинского электроотсоса, что было ликвидировано при помощи тугого наполнения полости физиологическим раствором на 13-15 мин, в другом случае при пункции краевого абсцесса VI сегмента печени размерами более 12см в диаметре был прорыв гноя в брюшную полость, что удалось ликвидировать лапароскопической санацией.
1. Зубов А.Д., Вилсон Дж.И. Абсцессы печени: этиологические факторы и диагностические ошибки // Вестник клуба панкреатологов. 2015. № 2. С. 37-41.
2. Гаюров У.Х.,Курбонов К.М. Диагностика и тактика лечения холангиогенных абсцессов печени //Актуальные вопросы гепатобилиарной хирургии: материалы XXI Международного конгресса ассоциации гепатобилиарных хирургов стран СНГ. Пермь, 2014. С. 87-88.
3. Нартайлаков М.А. Хирургия печени и желчных путей// Здравоохранение Башкортостана. 2005. № 3. С. 112-114.
5. Овчинников В.А., Малов А.А., Акуленко С.В., Захаров А.Г., Парахонян Н.В., Галанин И.А. Современная тактика в лечении бактериальных абсцессов печени // Медицинский альманах. Хирургия. 2013. Т. 29. № 5.С. 99-103.
6. Romano G., Agrusa A., Frazzetta G., De Vita G., Chianetta D., Di Buono G., Amato G., Gulotta G. Laparoscopic drainage of liver abscess: case report and literature review. G. Chir. 2013. V. 34 (5-6). Р. 180-182.
Ограниченные гнойные заболевания печени встречаются редко, но трудно поддаются диагностике и протекают тяжело. Среди госпитализированных в хирургический стационар больных пациенты с абсцессами печени составляют до 0,16%.
Выделяют следующие группы абсцессов печени: 1) холангиогенные (54,8%); 2) криптогенные (19,1%); 3) травматические (7,1%); 4) пилефлебитические (4%); 5) послеоперационные (4,7%); 6) контактные (4,7%); 7) амебные (4%) [1] (рис. 1).

Рис. 1. Этиология абсцессов печени
Лечение этой патологии чаще хирургическое, и до внедрения пункционных методов лечения больные с абсцессами печени обычно подвергались большим полостным операциям, нередко сопровождающимся послеоперационной летальностью от 16,9% до 55,0% [2, 3]. В современной хирургии с диагностической и лечебной целью широко используют компьютерную томографию (КТ) и ультразвуковое исследование (УЗИ) 4.
До внедрения в клиническую практику КТ и УЗИ лечение ограниченных гнойников печени проводилось в основном на основании клинических данных. Прорывом в лечении и, конечно, «золотым стандартом» в лечебной тактике явилось внедрение в клиническую практику методов КТ и УЗИ. Чрескожная пункция и дренирование гнойников печени свое доминирующее место в хирургии приобрели при ультразвуковой навигации. Метод открыл новые возможности для диагностики и лечения, позволил внедрить малотравматичные методы эвакуации гнойников печени. Ведущее место в лечении больных с абсцессом печени занимают пункционные методы. К их достоинствам относят: отсутствие риска общего обезболивания, сокращение сроков нахождения на стационарном лечении, низкий уровень операционной агрессии, невысокий процент летальных исходов 5.
Цель исследования: анализ результатов лечения абсцессов печени пункционным способом под ультразвуковой навигацией.
Материалы и методы исследования
В отделениях хирургии ГКБ № 8 г. Уфы с 2014 по 2019 гг. с солидными абсцессами печени находились 19 больных. Возраст пациентов варьировал от 31 до 72 лет, средний возраст составил 53,5±0,3 года, соотношение мужчин и женщин было соответственно14 (73,7%) и 5 (26,3%) (рис. 2).
Рис. 2. Гендерный состав анализируемых больных (%)
Следует отметить, что в анализируемой группе преобладали более молодые мужчины (их средний возраст составил 38±0,15 года) и более пожилые женщины (средний возраст 65±0,15 года) (рис. 3).
Рис. 3. Частота встречаемости абсцессов печени
Пик заболеваемости приходился на возраст от 31 до 55 лет (43± 0,3 года) (11 пациентов, 57,9%). Гнойный процесс в правой доле выявлялся в 17 (89,5%) случаях, в левой доле - в 2 (11,5%) случаях (рис. 4).
Рис. 4. Локализация абсцессов печени (%)
УЗИ больным с подозрением на абсцесс печени проводили в течение первых 3 суток от момента госпитализации. Степени тяжести состояния больных определяли при помощи шкалы SAPS II, в анализируемой группе среднее число баллов составило 41±1,18. Средний период диагностики составил 4,1±0,7 сут. (таблица).
Этиология абсцессов печени в клинической группе
Результаты исследования и их обсуждение
При УЗИ обычно выявляли увеличение размеров печени, образование округлой или неправильной формы с анэхогенной структурой содержимого, а по периферии имелась капсула повышенной эхогенности. В диагностике приоритетными являлись результаты УЗИ, по ним фактически определялась тактика лечения. При необходимости дифференциальной диагностики применялась КТ. Исходя из стадии формирования абсцессов бактериальной этиологии выделяют 3 возможные вариации эхоскопической картины.
Первоначально при УЗИ в печени выявляется неоднородный, нечетко обозначенный фрагмент паренхимы повышенной эхогенности, внутри которой выделяется бесструктурный гипоэхогенный участок (стадия инфильтрации). В этой стадии в паренхиматозной ткани печени вероятно выявление участка сниженной яркости, который имеет разнородное строение и неотчетливые контуры, которые переходят в здоровую ткань. В центре этого участка мы наблюдаем анэхогенный бесструктурный участок некроза (рис. 5).
Такая картина может наблюдаться непродолжительный отрезок времени, буквально несколько часов, и уловить во время УЗИ ее удается редко.
Рис. 5. Эхограмма. Стадия некроза печени
Со временем в зоне инфильтрации образуется полость с гноем, без четких границ, ее содержимое гипоэхогенное, чаще неоднородное (стадия абсцедирования). Характер содержимого полости связан с наличием гноя и тканевого детрита. В ткани печени, прилежащей к данному участку, имеется воспаление средней степени выраженности. Клинические проявления, соответственно, становятся более выраженными, что соответствует образованию гетерогенной жидкости (рис. 6).
Помимо свойственных для жидкостной структуры эхографических признаков («усиление» задней стенки, эффект боковых теней, эффект длительного псевдоусиления эхосигнала), обнаруживаются нестандартные показатели: внутреннее содержимое полости абсцесса обособляется, в связи с этим образуется граница «жидкость - жидкость» с горизонтальным уровнем, более плотная часть содержимого при этом находится ниже границы; у верхней стенки полости вероятно присутствие воздушных пузырьков в виде гиперэхогенных структур (они дают реверберирующий эффект - «хвост кометы»).
Рис. 6. 2-й вариант эхографической картины, стадия абсцедирования
Третья стадия (хронизации процесса) характеризуется выявлением плотной, толстой пиогенной капсулы по контуру гнойника. При УЗИ мы наблюдаем хронический абсцесс печени, характеризующийся четкими контурами, центральной частью сниженной яркости, толстая стенка очага эхогенная, с явлениями кровотока. Также вероятно выявление кальцинированных компонентов в капсуле (рис. 7). Следовательно, выявление при УЗИ в печени очага обызвествления является возможным признаком обратного развития абсцесса.
Рис. 7. Стадия хронизации абсцесса печени
При проведении исследования с помощью аппарата УЗИ в абсцессах могут быть выявлены в различной степени акустические эффекты, которые присущи кистам. Также имеются такие особенные признаки абсцессов, как разграничение содержимого на два компонента: жидкость и осадок, в гнойной полости выявляются пузырьки воздуха (гиперэхогенные компоненты с реверберирующим эффектом на стенках полости), сдвиг содержимого гнойной полости, который фиксируется с помощью УЗИ.
Для проведения пункционных, УЗ-ассистированных методов лечения противопоказаниями являлись технические причины (отсутствие безопасной пункционной трассы) и тяжелые нарушения свертывающей системы крови.
Пациентам после постановки диагноза под местной анестезией и под контролем УЗИ производили чрескожно-чреспеченочную пункцию и дренирование места абсцесса. Для наглядного контроля при прицельных чрескожных пункциях и для введения дренажей пользовались ультразвуковыми аппаратами «Aloka 1000» и «Medison SonoAce» с конвексным и линейным датчиком с диапазоном частоты 3,5-10 МГц. Для более точного позиционирования пункционной иглы применялся биопсийный адаптер. Показания для выполнения пункционного лечения выставлялись при помощи ультразвуковой диагностики, пункция осуществлялась только под ультрасонографической навигацией, что позволяло проводить прицельную и безопасную пункцию. Для пункции применяли иглы с внешним диаметром 1,5 мм, длиной 15-20 мм.
Местная анестезия, которую применяли при пункционном лечении, является вполне достаточной. Место пункции зависит от пораженного сегмента печени, но чаще ее проводили по задней подмышечной линии. Нами был использован также добавочный доступ в XI-X межреберье между передней и средней подмышечными линиями справа для проведения пункционной манипуляции для более качественного промывания при полостях большого размера. Во время манипуляции производили максимальное удаление гноя из полости с последующим промыванием полости дезинфицирующим раствором (хлоргексидином, диоксидином). В послеоперационном периоде проводили антибактериальную, дезинтоксикационную и направленную на общее укрепление организма терапию.
Мы добились выздоровления всех 19 пациентов путем пункционной аспирации (12 человек) и катетеризации (в 7 случаях). При этом для санации внутрипеченочного гнойника 8 пациентам была достаточна однократная пункция, в 3 случаях потребовалась двукратная и в 1 - трехкратная.
Катетеризацию мы проводили чаще всего катетерами pig tail диаметром 8-12 Fr. При абсцессах менее 10 см в диаметре было достаточно дренирования одним микродренажом (5 больных). При абсцессах большого размера (диаметром более 10 см) и наличии выраженной капсулы мы выполняли двойное дренирование полости (2 случая, 10,5%).
Среднесуточное стояние дренажа у этих больных составило 8±1,4 сут.
В каждом случае мы проводили микробиологическое исследование извлеченной посредством пункции жидкости. При этом этиологическими факторами содержимого абсцесса выступали разнообразные микроорганизмы: гемолитический стрептококк, золотистый стафилококк, энтеробактерии, кишечная палочка, клебсиелла, анаэробные микроорганизмы. Нередко при посеве гноя выделяется смешанная флора. Во время выполнения процедуры эвакуации содержимого полость сокращалась на 60-75%. В динамике после катетеризации абсцесса печени в различные сроки наблюдали полное сокращение остаточных полостей. В проекции дренированного абсцесса жидкость не определяется, в ткани печени визуализируются два дренажа (рис. 8).
Рис. 8. УЗИ в динамике. В проекции дренированного абсцесса в ткани печени визуализируются два дренажа
Больные после первичной пункции находились под наблюдением хирурга поликлиники, в зависимости от общего состояния им выполнялись контрольное УЗИ и по показаниям повторные пункции. Интервал между пункциями определялся индивидуально в зависимости от ультрасонографической динамики, чаще через 1,5-2 месяца. Дренаж мы убирали, если по нему отсутствовало отделяемое после контрольного исследования с помощью аппарата УЗИ.
При пункции абсцессов наблюдалось 2 осложнения. При эвакуации содержимого абсцесса при помощи медицинского электроотсоса отмечалось необильное наружное кровотечение, остановленное при помощи тугого наполнения полости физиологическим раствором на 13-15 мин. В другом случае при пункции краевого абсцесса VI сегмента печени размерами более 12 см в диаметре был прорыв гноя в брюшную полость, что удалось ликвидировать при помощи лапароскопической санации.
1. Способ санации абсцессов печени с помощью пункции под контролем УЗИ обладает доступностью, эффективностью и низкой травматичностью. Данная методика повышает эффективность комплексного лечения, снижая интоксикацию и вероятность послеоперационных осложнений.
2. При небольших абсцессах печени (до 5 см в диаметре) пункция абсцесса в большинстве случаев оказывается достаточной для его санации, при абсцессах от 5 до 10 см в диаметре лечебный эффект может быть достигнут дренированием одним микродренажом, при диаметре абсцесса более 10 см в диаметре и выраженной капсуле полость предпочтительнее дренировать двумя катетерами.
3. Частота постманипуляционных осложнений при лечении абсцессов печени с помощью диапевтических технологий невысока, эти осложнения могут быть купированы без лапаротомии.
Кафедра госпитальной хирургии ФГБОУ ВО «Южно-Уральский государственный медицинский университет», ГБУЗ «Челябинская областная клиническая больница», Челябинск, Россия
Кафедра госпитальной хирургии Южно-Уральского государственного медицинского университета, Челябинск
Кафедра госпитальной хирургии Челябинской государственной медицинской академии, Челябинская областная клиническая больница
Пункционное дренирование абсцесса печени при транспозиции внутренних органов
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(2): 85‑86
Расположение внутренних органов, зеркально противоположное нормальному, — редкая аномалия развития (синонимы: situs viscerus inversus, situs rarior, situs transversus, полное или неполное обратное расположение органов, извращенное положение, транспозиция органов, декстрокардия).
Впервые такое расположение описано Marko Severino в 1643 г. Оно встречается с частотой 1 на 10 000 населения, различается частичной и полной транспозицией органов.
В большинстве случаев оно не влияет на функцию органов и жизнедеятельность человека и может привести врача к диагностической растерянности и конфузу при упущении из вида возможности подобного состояния и создать проблему лишь в трансплантологической практике. Ранее ведущим методом диагностики этого состояния (до ультрасонографии, КТ и МРТ) был рентгенографический.
Мы располагаем клиническим наблюдением успешного излечения абсцесса печени при транспозиции внутренних органов методом дренирования под ультрасонографическим контролем.
Больной И., 63 лет, в экстренном порядке поступил в I хирургическое отделение ЧОКБ 23.03.16 с диагнозом абсцесса печени и с жалобами на общую слабость, подъем температуры тела, боль в левом подреберье, в состоянии средней степени тяжести. Из анамнеза известно, что заболел месяц назад, причину болезни отметить не может.
Был госпитализирован в ЦРБ по месту жительства с температурой 40 °C с рабочим диагнозом: «острая респираторно-вирусная инфекция». При обследовании подтвержден сахарный диабет 2-го типа, выявлена анемия (гемоглобин 98 г/л). При ЭГДС, ультрасонографии органов брюшной полости и рентгенографии органов грудной клетки обнаружена транспозиция органов.

После проведенного антибактериального лечения (амоксициллин 1,5 г в сутки в течение 10 дней без эффекта и цефтриаксон 1 г в сутки в течение недели) наступило незначительное улучшение. Для уточнения диагноза госпитализирован в университетскую клинику ЮУГМУ 18.03.16, где диагностирована нагноившаяся киста левой доли печени. Пациента перевели в ЧОКБ 23.03 и на следующий день выполнили МСКТ органов брюшной полости с контрастным усилением, при которой обнаружены полости в паренхиме печени с нечеткими контурами сливного характера, расположенные в III, IV, VII, VIII сегментах печени, общим размером 100×85×95 мм» (см. рисунок). Мультиспиральная компьютерная томограмма от 24.03.16.
25.03 выполнено пункционное дренирование абсцесса печени под ультразвуковым контролем двумя дренажами с промывной системой. При этом одномоментно эвакуировано 90 мл густого гноя. Послеоперационное течение без осложнений. При контроле (ультрасонография 28.03 и МСКТ 06.04) отмечено спадение стенок гнойной полости. При микроскопическом исследовании пунктата в препарате найдено большое количество лейкоцитов, внутриклеточных бактерий, цисты лямблий, простейшие не обнаружены. Микробиологическое исследование — роста бактерий нет.
11.04 пациент с одним дренажем выписан в ЦРБ по месту жительства с рекомендациями промывать полость 1 раз в сутки антисептиком и удалить дренаж при чистых промывных водах. Дренаж был удален через полтора месяца после выписки из ЧОКБ.
Пациент для контроля осмотрен в апреле 2017 г., наступило полное выздоровление.
Таким образом, приведенное клиническое наблюдение интересно, на наш взгляд, возможностью диагностировать транспозицию внутренних органов при первичном обращении на уровне центральной районной больницы при ультрасонографии, а также возможностью ликвидировать большой абсцесс печени пункционным дренированием.
ФГБУ "Институт хирургии им. А.В. Вишневского" Минздрава России, Москва
Институт хирургии им. А.В. Вишневского Минздравсоцразвития России, Москва
Абсцесс печени с прорывом в правую плевральную полость как осложнение деструктивного аппендицита
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2010;(2): 66‑68
Икрамов Р.З., Андреенков С.С. Абсцесс печени с прорывом в правую плевральную полость как осложнение деструктивного аппендицита. Хирургия. Журнал им. Н.И. Пирогова. 2010;(2):66‑68.
Ikramov RZ, Andreenkov SS. Liver abscess burst to the right pleural cavity as a complication of destructive appendicitis. Pirogov Russian Journal of Surgery = Khirurgiya. Zurnal im. N.I. Pirogova. 2010;(2):66‑68. (In Russ.).
Абсцессы печени подразделяются на пиогенные, возникающие в результате бактериальной контаминации, например на фоне холангита (холангиогенные абсцессы печени), или других гнойно-септических заболеваний, что более характерно для европейских стран, и паразитарные (дизентерия, глистная инвазия), которые распространены в развивающихся странах. В последние годы наблюдается рост частоты выявления абсцессов печени микотической и туберкулезной этиологии. Данное обстоятельство связано с увеличением числа больных с первичным и вторичным иммунодефицитом [1].
В зависимости от путей распространения инфекции абсцессы печени могут быть подразделены на: билиарные, портальные (аппендицит, дивертикулит, болезнь Крона, неспецифический язвенный колит и др.), артериальные (системный сепсис), контактные (возникающие в результате прямого распространения гнойного процесса из прилегающих органов), травматические (тупая или проникающая рана печени) и криптогенные (источник абсцесса не выявляется). Кроме того, абсцессы могут возникать в результате нагноения кист и остаточных полостей печени после хирургических вмешательств. В группе риска находятся больные, получающие иммуносупрессию, химиотерапию, а также больные опухолями внепеченочных желчных путей и билиарными дренажами [1].
Впервые клиническое наблюдение аппендицита, осложнившегося развитием абсцесса печени, было описано Waller в 1847 г. (приведено по E.A. Babler, 1915 г. [5]). Однако из-за крайне редкой встречаемости к настоящему времени в литературе описаны только единичные наблюдения такого варианта течения пилефлебита [6, 7].
Пилефлебит в системе верхней брыжеечной и воротной вен является одним из самых грозных осложнений острого аппендицита. Он встречается сравнительно редко - у 0,06-0,15% больных этим заболеванием [2].Течение исключительно тяжелое, у большинства больных заканчивается летальным исходом [3, 8]. Летальность при пилефлебите достигает 90% [2]. В 1986 г. В.С. Савельев высказал мнение о том, что достоверных наблюдений пилефлебита не известно [4], залогом успеха в лечении этого заболевания является своевременность диагностики.
Клинических наблюдений деструктивного аппендицита с фрагментацией червеобразного отростка, осложненного пилефлебитом, с развитием абсцесса печени, прорывом последнего в правую плевральную полость и с формированием бронхоплеврального свища в литературе не описано. Приводим собственное наблюдение такого варианта развития и течения заболевания.
Больная К., 44 лет, поступила в Институт хирургии им. А.В. Вишневского в июне 2009 г. с жалобами на выраженную слабость, боли в правом плечевом суставе и правом подреберье, подъемы температуры тела до 40 °С.
Из анамнеза известно, что заболела пациентка остро. 08.05 был отмечен подъем температуры тела до 38 °С, сопровождавшийся отеком слизистых и кожных покровов, затруднением дыхания. В дальнейшем присоединились боли в зоне правого плечевого сустава и правом подреберье. Температура тела нарастала и достигла 40 °С. Появился продуктивный кашель с вязкой мокротой темного цвета до 100 мл в сутки. Больная обратилась в поликлинику по месту жительства, где проводилось лечение по поводу бронхопневмонии без значительного улучшения состояния. Было продолжено амбулаторное обследование, и с учетом перечисленных выше жалоб пациентке в Российском онкологическом научном центре им. Н.Н. Блохина было выполнено компьютерно-томографическое исследование. Обнаружена картина абсцесса печени и правого легкого (больше данных о его паразитарном характере).
При более подробном сборе анамнеза (сделанным после оперативного вмешательства) выяснилось, что в марте 2009 г. больную беспокоили боли в животе, локализовавшиеся преимущественно в правой подвздошной области, сопровождавшиеся частым жидким стулом. Самостоятельно больной ситуация была расценена как пищевая токсикоинфекция. Проводилась антибактериальная терапия в течение 7 дней. На фоне лечения симптомы заболевания исчезли.
При поступлении состояние больной средней степени тяжести. Кожные покровы бледные. Температура тела 38 °С. Дыхание через нос свободное. Грудная клетка симметрична, при пальпации безболезненна. Отмечается отставание правой половины грудной клетки при дыхании. Перкуторно определяется притупление с уровня V ребра справа. При аускультации слева дыхание проводится во все отделы, справа резко ослаблено в нижних отделах, единичные сухие хрипы. Частота дыхательных движений 18 уд/мин. Тоны сердца приглушены, ритм правильный. ЧСС 86 уд/мин, АД 110/70 мм рт.ст. Язык чистый, влажный. Живот при пальпации мягкий, безболезненный во всех отделах. Печень на 2 см выступает из-под края реберной дуги. Перистальтика выслушивается. Перитонеальных симптомов нет.
Внутри- и внепеченочные желчные протоки не расширены. Общий желчный проток визуализируется, диаметром 6,2 мм, просвет его свободный. Желчный пузырь не увеличен, его стенки неравномерно утолщены, содержимое однородное.
Дуплексное сканирование в режимах цветового допплеровского картирования, энергии допплеровского сигнала и импульсной допплерографии: чревный ствол: диаметр = 7,6 мм; линейная скорость кровотока (ЛСК) = 1,78 м/с; общая печеночная артерия: Д=6,3 мм, ЛСК=2,0 м/с; собственная печеночная артерия: Д=4,3 мм, ЛСК=1,7 м/с; правая ветвь собственной печеночной артерии: Д=5,2 мм, ЛСК=1,21 м/с; левая ветвь собственной печеночной артерии: Д=4,7 мм, ЛСК=0,921 м/с; поджелудочная железа в размерах не увеличена, имеет четкие ровные контуры, ее паренхима равномерно уплотнена во всех отделах; селезенка увеличена, S=50 см2, контуры ровные, четкие, структура паренхимы однородна. Увеличенных регионарных лимфатических узлов не выявлено.
Заключение: бессосудистое, очаговое (жидкостное) образование печени. Ультразвуковая картина соответствует самостоятельно дренировавшейся в поддиафрагмальное пространство кисте, вероятно, с прорывом в правую плевральную полость. Правосторонний гидроторакс. Диффузные изменения паренхимы печени и поджелудочной железы. Увеличение селезенки. Повышение скорости кровотока по собственной печеночной артерии и ее ветвям.
Спиральная компьютерная томография грудной клетки и органов брюшной полости (консультация снимков исследования РОНЦ им. Н.Н. Блохина специалистами Института хирургии им. А.В. Вишневского): в области нижней доли (VIII сегмент) правого легкого субплеврально определяется полостное образование округлой формы, размером 24×21 мм, в центре которого имеется воздух и, возможно, незначительное количество жидкости, по периферии образования визуализируется капсула толщиной от 4 до 7 мм (рис. 1, а и далее см. на цв. вклейке), Рисунок 1. Компьютерная томограмма. Абсцесс правого легкого в артериальную фазу исследования. а - очаговое образование. Рисунок 1. Компьютерная томограмма. Абсцесс правого легкого в артериальную фазу исследования. б - воспалительная инфильтрация. вокруг образования определяется воспалительная инфильтрация (рис. 1, б).
Полостное образование плотно прилежит к внутренней поверхности грудной стенки, а также четко не дифференцируется от правого купола диафрагмы. Остальная паренхима правого и левого легких с умеренно выраженными диффузными и очаговыми пневмосклеротическими изменениями, причем наибольший очаг (размером до 6 мм) расположен субплеврально в области язычковых сегментов верхней доли слева. Воздушность легочной паренхимы сохранена во всех отделах. Воздушность трахеи и крупных бронхов как справа, так и слева не изменена. Средостение не смещено, структуры его дифференцированы. Медиастинальные лимфатические узлы в области ретрокавального пространства увеличены до 9 мм. Других патологических образований в средостении не обнаружено. В плевральных полостях выпота нет.
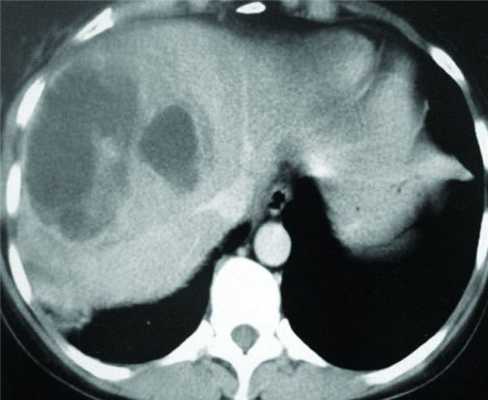
Печень увеличена, негомогенная, в области правой доли (VII-VIII сегменты), возможно, частично в области правого поддиафрагмального пространства определяется скопление сгруппированных полостных образований (не менее 4, возможно, сообщающихся друг с другом) округлой и овальной формы, размером 76×59, 82×54, 39×25 и 53×38 мм. Образования преимущественно гомогенные. В одном из них видны воздушные пузырьки с выраженной воспалительной инфильтрацией окружающей печеночной паренхимы (рис. 2). Рисунок 2. Компьютерная томограмма. Абсцесс VII-VIII сегментов печени в артериальную фазу исследования.
Желчный пузырь спавшийся, кальцинированных конкрементов в просвете не выявлено. Внутрипеченочные желчные протоки не расширены.
Поджелудочная железа и селезенка без патологических изменений.
Заключение: КТ-картина соответствует абсцессам правой доли печени, возможно, с прорывом в поддиафрагмальное пространство справа. Абсцесс нижней доли правого легкого.
С целью исключения бактериальной этиологии заболевания выполнили колоноскопию. Сигмовидная кишка была осмотрена на расстоянии 50 см от ануса. Патологических изменений слизистой осмотренных отделов толстой кишки не выявлено.
При бактериоскопии в мокроте обнаружен Bacteroides fragilis.
Больная была консультирована заведующим отделением торакальной хирургии проф. А.А. Вишневским: имеются абсцессы правой доли печени, вероятно, паразитарного генеза с прорывом в правую плевральную полость. С учетом малого размера абсцесса нижней доли правого легкого больной показана эхинококкэктомия кист VII-VIII сегментов печени, диафрагмотомия, санация и дренирование правой плевральной полости.
Осмотр акад. РАМН В.Д. Федоровым: у больной имеются множественные абсцессы правой доли печени с прорывом в правое поддиафрагмальное пространство и в правую плевральную полость, вероятнее всего, паразитарного генеза. В связи с сохраняющейся высокой температурой тела и выраженной интоксикацией показано оперативное лечение в объеме эхинококкэктомии кист VII-VIII сегментов печени, диафрагмотомии, санации и дренирования правой плевральной полости.
05.06 - операция (д.м.н. Р.З. Икрамов). Ревизия брюшной полости и малого таза: печень увеличена в размерах, тестоватой консистенции, в области VII-VIII сегментов плотно припаяна к диафрагме. Желудок не эктазирован. В матке определяется 3 миоматозных узла размером от 2 до 3 см. В правой подвздошной области инфильтрат с вовлечением купола слепой кишки, матки и правого яичника. Других изменений органов брюшной полости нет.

Произведены мобилизация правой доли печени и разделение сращений печени и диафрагмы тупым и острым путем. На этапе разделения сращений вскрыта гнойная полость между печенью и диафрагмой, эвакуировано около 50 мл сливкообразного гноя. После разделения сращений в VII-VIII сегментах печени определяется образование диаметром около 15 см, мягкой консистенции, состоящее из множества полостей (рис. 3). Рисунок 3. Интраоперационная картина абсцесса VII-VIII сегментов печени, поддиафрагмального пространства с прорывом в плевральную полость. Сделана биопсия, обнаружен некроз ткани. Правая печеночная вена и печеночно-двенадцатиперстная связка взяты на турникет.
Проведена интраоперационная консультация с акад. РАМН В.Д. Федоровым: у больной имеется абсцесс VII-VIII сегментов печени. При гистологическом исследовании данных о паразитарном характере не получено. С учетом наличия инфильтрата в малом тазу рекомендованы его разделение, ревизия малого таза для определения возможной причины абсцесса печени.
Выполнено разделение сращений в области илеоцекального угла. Выделен купол слепой кишки. Червеобразный отросток фрагментирован (рис. 4). Рисунок 4. Интраоперационная картина фрагментированного червеобразного отростка. Рисунок 4. Интраоперационная картина фрагментированного червеобразного отростка. Брыжейка некротизирована. Верхушка спаяна с маткой и правым яичником. Произведена аппендэктомия. Культя отростка погружена в кисетные и Z-образные швы. Верхушка червеобразного отростка выделена из сращений и удалена. Других изменений в малом тазу не выявлено.
После пережатия печеночно-двенадцатиперстной связки, отступя 2-3 см от абсцесса, с помощью биполярной коагуляции выполнена атипичная резекция VII-VIII сегментов печени с перевязкой, клипированием и прошиванием сосудисто-секреторных элементов по срезу печени. Гемостаз с помощью аргонусиленной коагуляции и частичной гепатизации. Срез печени дополнительно укрыт пластинами тахокомба.
При ревизии диафрагмы выявлен свищевой ход диаметром около 0,5 см между правой плевральной и брюшной полостями, по которому поступает сливкообразный гной в количестве около 100 мл. Проведена интраоперационная консультация с проф. А.А. Вишневским: рекомендовано выполнение диафрагмотомии, санации и дренирования плевральной полости с последующей бронхоскопией для санации трахеобронхиального дерева. При невозможности адекватного дренирования полости абсцесса показана торакотомия вторым этапом. На протяжении 5 см выполнена диафрагмотомия справа, произведены санация и дренирование правой плевральной полости. Отверстие в диафрагме ушито отдельными узловыми швами. Контроль на аэростаз дал отрицательный результат. Легкое расправлено, дренаж из плевральной полости перекрыт.

Схема выполненного оперативного вмешательства представлена на рис. 5. Рисунок 5. Схема оперативного вмешательства. Слева - картина после ревизии, справа - результат оперативного вмешательства.
Гистологическое исследование: ткань печени с наличием множественных абсцессов. В сохранной окружающей паренхиме печени умеренно выраженная лимфоцитарная инфильтрация портальных трактов, явления внутриклеточного холестаза. Фрагменты жировой клетчатки с обширным фиброзированием, полнокровием, кровоизлияниями, полиморфноядерной воспалительной инфильтрацией, местами с гигантскими многоядерными клетками. Фрагменты стенки аппендикса с рубцовыми изменениями, полнокровием, кровоизлияниями, обильными грунуляциями.
Послеоперационный период осложнился нагноением послеоперационной раны (рана частично разведена). Проводилось местное лечение послеоперационной раны мазями на водорастворимой основе. По дренажу из плевральной полости длительное время сохранялось гнойное отделяемое (дренаж был на активной аспирации), проводилась санация остаточной полости абсцесса правой плевральной полости растворами антисептиков с учетом бактериальной флоры и чувствительности к ним. После прекращения оттока отделяемого и контрольной рентгенографии легких дренаж был удален.
Таким образом, приведенное клиническое наблюдение демонстрирует пример «эффекта» от самостоятельного приема антибиотиков расширенного спектра действия, вызвавшего стертость клинической картины основного заболевания и приведшего к ограничению воспалительного процесса в малом тазу. Развившийся в дальнейшем пилефлебит с формированием абсцессов печени длительное время протекал бессимптомно. Острое начало заболевания с гектической лихорадкой обусловлено прорывом абсцессов печени в правую плевральную полость с формированием бронхоплеврального свища. На амбулаторном этапе это было расценено как проявление бронхопневмонии. При отсутствии клинически значимого эффекта от проводимой терапии и при более углубленном обследовании были выявлены абсцессы печени с прорывом в правую плевральную полость.
Так как истинный источник заболевания не был выявлен дооперационно, этиология абсцессов с большей вероятностью была расценена как паразитарная. Только во время операции при опровержении паразитарного характера абсцессов по данным срочного гистологического исследования и при ревизии всей брюшной полости удалось установить причину абсцедирования.
Подпеченочный абсцесс
Подпеченочный абсцесс - ограниченное гнойное образование, расположенное между нижней поверхностью печени и петлями кишечника и являющееся осложнением хирургических заболеваний брюшной полости. Клиническими проявлениями подпеченочного абсцесса служат боли в правом подреберье, усиливающиеся при вдохе, лихорадка, интоксикация, диспепсические расстройства. Диагностика основана на детальном изучении анамнеза, результатах лабораторных исследований, рентгенографии, УЗИ и КТ органов брюшной полости. Лечение хирургическое, заключается во вскрытии, дренировании и промывании гнойника, а также системной антибиотикотерапии и дезинтоксикационных мероприятиях.
Общие сведения
Подпеченочный абсцесс в гастроэнтерологии и хирургии является типичным вариантом ограниченного перитонита. Формирование гнойника обусловлено свойствами листков брюшины, образованием сращений между ними, брыжейкой кишечника и другими структурами. Место локализации абсцесса может соответствовать первичному гнойному процессу либо быть результатом осумкования экссудата под диафрагмой. Соответственно этому выделяют две формы подпеченочных абсцессов: первично отграниченные (формирование полости происходит параллельно с основным патологическим процессом в близлежащем органе) и вторично отграниченные (микроорганизмы попадают в подпеченочное пространство как в зону максимальной резорбции из брюшной полости, а затем происходит изоляция гнойника путем формирования воспалительной соединительнотканной капсулы).
Причины подпеченочного абсцесса
Подпеченочный абсцесс является осложнением холецистита, панкреонекроза, гнойного воспаления червеобразного отростка (гнойного аппендицита), перфорации, открытых и закрытых повреждений полых или паренхиматозных органов, нарушений кровообращения в сосудах брыжейки кишечника при ущемленных грыжах и странгуляционной кишечной непроходимости, оперативных вмешательств. Также абсцесс может формироваться при гематогенных и криптогенных разлитых перитонитах. Чаще всего инфекционным агентом выступает ассоциация бактерий кишечной группы (E. coli, клебсиеллы, стафилококки, стрептококки) и анаэробных микроорганизмов.
Формированию отграниченного подпеченочного абсцесса способствуют пластические свойства брюшины: в результате повреждения на ее поверхности накапливается фибринозный клейкий экссудат, который и приводит к склеиванию прилежащих листков серозной оболочки. Далее происходит образование соединительнотканных спаек, и очаг гнойного воспаления изолируется от брюшной полости. В случае вторично отграниченного абсцесса важную роль в патогенезе играет высокая резорбтивная активность брюшины в подпеченочном пространстве, что способствует накоплению экссудата в данной области при распространенном перитоните. Есть и анатомические предпосылки формирования подпеченочного абсцесса - наличие печеночной сумки брюшины.
Симптомы подпеченочного абсцесса
Клиническая картина подпеченочного абсцесса зависит от тяжести процесса и основного заболевания. Наиболее частым признаком является боль в правом подреберье, иррадиирующая в область спины, лопатки или плеча, интенсивность которой увеличивается при глубоком вдохе. Также типична гипертермия (лихорадка имеет интермиттирующий характер), ознобы, тахикардия, возможна артериальная гипотензия. В тяжелых случаях развивается системная реакция на воспаление вплоть до сепсиса и полиорганной недостаточности.
Подпеченочный абсцесс может протекать и без выраженной симптоматики. В таких случаях заподозрить данную патологию позволяет субфебрильная температура тела, лейкоцитоз и увеличение СОЭ в анализах крови, а также болезненность при пальпации в области правого подреберья. К симптомам подпеченочного абсцесса относятся тошнота, метеоризм, запор; при больших размерах гнойника возможны признаки кишечной непроходимости.
Если имеет место вторично отграниченный абсцесс, в клинической картине ему предшествуют признаки разлитого перитонита. При этом на фоне постепенного улучшения состояния пациента формирование гнойника приводит к усилению абдоминальной боли и интоксикации.
Диагностика подпеченочного абсцесса
Консультация гастроэнтеролога и хирурга позволяет выявить характерные анамнестические данные и симптомы подпеченочного абсцесса. При осмотре пациента может определяться бледность кожных покровов. При пальпации в правом подреберье характерна болезненность. Абсцесс определяется как округлое флюктуирующее образование. В области его проекции кожа пастозна. Диагностика данного заболевания иногда весьма затруднительна, поскольку подпеченочный абсцесс может протекать со скудной симптоматикой, а связь с первичным патологическим процессом не всегда удается выявить. Именно поэтому насторожить врача должен недавно перенесенный перитонит, холецистит и другие деструктивные гнойные заболевания брюшной полости.
В лабораторных анализах выявляются характерные признаки воспаления. В общем анализе крови имеет место лейкоцитоз с нейтрофильным сдвигом, ускоренная СОЭ. При проведении рентгенографии органов брюшной полости визуализируется округлое образование с уровнем жидкости, может быть правосторонний плевральный выпот. Более информативные методы исследования при подозрении на подпеченочный абсцесс - УЗИ органов брюшной полости и компьютерная томография (МСКТ ОБП). Данные диагностические методики позволяют выявить наличие гнойника, определить его размеры и анатомическое взаимоотношение с окружающими органами.
Лечение подпеченочного абсцесса
Все пациенты с диагностированным подпеченочным абсцессом подлежат обязательной госпитализации в хирургическое отделение. Основным методом лечения является дренирование полости гнойника. С этой целью в настоящее время чаще применяются малоинвазивные методики. Чрескожная пункция проводится под ультразвуковым контролем; выполняется аспирация содержимого гнойника и дренирование. Через дренаж осуществляется многократное промывание полости абсцесса, введение антибактериальных препаратов. В тяжелых случаях, когда невозможно выполнить малоинвазивное вмешательство, проводится открытая хирургическая операция, предпочтительно из внебрюшинного доступа. Лечение также включает системную антибиотикотерапию, дезинтоксикационные мероприятия.
Прогноз и профилактика подпеченочного абсцесса
При своевременном выявлении и адекватном лечении прогноз благоприятный. Подпеченочный абсцесс может осложниться прорывом в брюшную полость с развитием разлитого перитонита и новых очагов гнойного воспаления, сепсисом и полиорганной недостаточностью. В таких случаях прогноз крайне неблагоприятный. Профилактика данной патологии заключается в своевременном лечении заболеваний, которые могут стать причиной абсцесса, а также тщательном послеоперационном наблюдении пациентов, которые перенесли перитонит и другие гнойные поражения органов брюшной полости.
Читайте также:
- Естественные киллеры ( NK-клетки ). Перфорины. Функция естественных киллеров. Задачи NK-клеток.
- Хлоридные каналы мембраны клетки
- Южно-американские геморрагические лихорадки. Лимфоцитарный хориоменингит. Диагностика аренавирусов. Лечение и профилактика инфекций ареновирусов.
- Травма спинного мозга у детей
- Опухоль толстой кишки: причины, симптомы и лечение
