Изменения кожи при гемохроматозах
Обновлено: 25.04.2024
Клиника гемохроматоза - проявления
В организме железо скопляется рассеянно. Однако в отдельных органах оно откладывается в большем количестве, тем самым создавая преобладающую симптоматологию. Триада: меланодермия, цирроз печени и бронзовый диабет отмечается в большинстве случаев заболевания, либо в совокупности, либо с преобладанием некоторых элементов. К этим признакам присоединяется, с различными частотой и интенсивностью тетрада, состоящая из сердечных, эндокринных, пищеварительных и суставных расстройств.
1. Периоды скрытого течения и проявления гемохроматоза. Поскольку болезнь носит наследственный характер, скопление железа начинается в ранние сроки, видимо вскоре после рождения. Однако первые симптомы проявляются лишь после достижения определенного порога накопления железа в отдельных органах, что способствует началу клеточнометаболического расстройства. Следует отметить, что в практике внутренней медицины, скрытое и нехарактерное течение этого заболевания особо выделяется. В принципе первые проявления болезни наблюдаются после 40 лет, но более часто к 50 годам жизни.
Первая стадия болезни отличается длительным периодом переносимости, при этом ихсодные симптомы столь нехарактерны, что, даже после появления первых субъективных признаков, таких как, утомленность, постепенное ухудшение общего состояния, отсутствие инициативы, понижение мужественности и пр. врач затрудняется найти им какое-либо объяснение на протяжении нескольких лет.
Окраска кожи, относящаяся к объективным признакам, также весьма лукавая и лишь с опозданием привлекает внимание окружающих. Гипотрофию яичек трудно определить на этой стадии. Первыми признаками внутренних органов являются, наиболее часто, проявления печени. В единичных случаях клиническая картина во всей совокупности складывается в течение нескольких месяцев при развитии сопутствующих заболеваний.
2. Период разгара гемохроматоза. В симптоматологии отражается выраженный клинический полиморфизм в связи с чрезмерной нагрузкой железом нескольких органов. До образования полной клинической картины наблюдаются неполные переходные формы, при которых хронологическая последовательность синдромов не подчиняется каким-либо постоянным правилам. Вопреки рассеянности скопления железа, этот процесс одинаково поражает все органы.
Наибольшее скопление наблюдается в печени и поджелудочной железе, на втором месте находятся сердечная мыщца и железы внутренней секреции (в частности яички) и лишь в малом количестве выявляется в селезенке, лимфатических узлах, хрящах, скелете, синовиальных оболочках, пищеварительном тракте, дыхательном и выделительном аппаратах. В отличие от сердечной мышцы в скелетной мускулатуре скопляется небольшое количество железа, а в нервной системе наименьше всего, иногда даже она остается незатронутой. Клинические признаки соответствуют распределению железа в тканях и органах больного.
а) Пигментация покровов и слизистых оболочек при гемохроматозе. Окраска кожи одно из ранних проявлений, составляющих клиническую «триаду» болезни более чем в 90% случаев. Ее обусловливает накопление двух пигментов — меланина, негеминного пигмента (лишенного железа), окрашивающего кожу в напоминающий сланец синевато-серый оттенок, и гемосидерина железистого негеминного пигмента, придающего коже грязно-коричневый цвет.
Окраска общая, однако преимущественно наблюдается на непокрытых участках кожи (лицо, затылок, ладонь), также на слизистой оболочке половых органов, вокруг промежности и подкрыльцовой зоны. Покровы блестящие, сухие, шелушатся, причем последнее явление делает окраску более выраженной, поскольку в глубоких слоях отложение пигментов интенсивнее. В сочетании с алкоголизмом окраска усиливается; отдельные больные предъявляют жалобы на острый зуд кожи.

б) Поражения печени при гемохроматозе. К 25—30 годам развивается прогрессирующая гепатомегалия, которая, в отдельных случаях, достигает пупочной линии. Прощупывание выявляет твердую, равномерную и неболезненную печень с заостренным нижним краем. Долгое время гепатомегалия переносится хорошо, без таких осложнений, как желтуха, увеличение размеров селезенки, побочное кровообращение и синдром водяночного скопления. В дальнейшем сидероз печени превращается в истинный цирроз, не отличаясь от тяжелых форм атрофического цирроза. После такого длительно скрытого периода происходит крутой поворот в направлении быстрой декомпенсации.
Лапароскопия и макроскопическое исследование при вскрытии выявляют крупную печень цвета ржавчины с оттенком охры («старой меди»), слегка уплотненную, на вид гладкую или зернистую (как это бывает при устарелых узелковых формах). На очень далеко зашедших стадиях болезни печень оттягивается за реберный край и атрофируется. В отдельных случаях массивная пигментация железом резко противоположна слабой окраски кожи и даже нормальной сидеремии (Piguet).
в) Поражения поджелудочной железы при гемохроматозе. По значению накопляемого количества железа поджелудочная железа занимает третье место. Сахарная болезнь представляет собой позднее осложнение гемохраматоза поджелудочной железы. Начало вкрадчивое но заболевание можно определить с помощью реакции на сахар крови с нагрузкой. Со временем сахарная болезнь усугубляется, приобретая «слабый», кетозо-килсый вид, при этом для восстановления равновесия в организме, в некоторых случаях требуется назначение крупных доз инсулина, в других — диабет оказывается устойчивым к этому препарату.
Описаны случаи тяжелой формы диабета, изменившего сидеремию и насыщаемость сидерофилина, которые парадоксально, вопреки массивной окраске тканей на повторных контрольных исследованиях, отражали нормальное состояние. С восстановлением нарушенного диабетом равновесия и уменьшением гемохроматоза показатели сидеремии и насыщаемости сидерофилина увеличивались, несмотря на наблюдаемое клиническое улучшение (Симон и сотр.).
г) Сердечные проявления гемохроматоза. Железо довольно часто проникает в сердечную мышцу, которая, с этой точки зрения, составляет единичное явление для мускулатуры. До сорокалетнего возраста миокардоз переносится легко, но затем появляются признаки венечного склероза (околосердечные боли) и склероза сердечной мышцы. Со временем это переходит в обшую сердечную недостаточность, исцеление которой сложное дело.
На поражение сердца указывают определенные ЭКГ изменения, причем наиболее ранними признаками являются низкий вольтаж, удлинение интервала Р—Q, нарушение реполяризации, инверсия волны Т; в иных случаях отмечается расстройство ритма (экстрасистолы, мерцание предсердий) и даже блок ножки пучка Гисса (Choussat, Marty и сотр.).
д) Поражения органов внутренней секреции при гемохроматозе. Нарушения отмечаются в ряде эндокринных органов, однако, при гемохроматозе скопление этого металла в поражаемых железах неодинаково (Velcke).
— Поражение гонад. Среди альтерационных изменений эндокринного характера наиболее частым и явным представляется поражение яичек. Отдельными авторами установлен разный коэффициент частоты этих расстройств. Так, по Finch они составляют 10—20% случаев, по Justin и Besancon 34,5%, по Girard 55%, по Albeaux и Fernet 84%, а по Marble и Baily 100%.
У молодых наблюдается несоразмерный возрасту инфантилизм и «феминизирующий» аспект (гинекомастия, сокращение оволосения и пр.). Даже после наступления половой зрелости наблюдаются выпадение волос в лобковой и подмышечной зонах, скудная борода и аспект первородного пушка на голове (тонкие и мягкие волосы). У взрослых сокращается либидо и рано наступает полное половое бессилие. Морфологически яички атрофируются (обратное развитие до размеров зерна фасоли). Поражение яичников менее известно, видимо по причине редкости заболевания женщин гемохроматозом.
Поражение иных желез. Mac Donald и Mallory отметили наличие отложений железа в передней доле гипофиза в пропорции 86%, однако клинические проявления (гипофизарной недостаточности) значительно реже. Что касается поражения других желез видимо это объясняется их зависимостью от передней доли гипофиза. Поражение коры надпочечников способствует усугублению астении и понижению артериального давления, но степень ее поражения нелегко определить по причине симптоматического взаимодействия с другими органами (недостаточность печени, сахарный диабет, недостаточность яичек и пр.).
Что касается щитовидной железы, несмотря на частую перенагрузку железом, клинические проявления наблюдаются редко; наиболее часто выявляются признаки гипотиреоза.
е) Костносуставные проявления гемохроматоза. К суставным проявлениям относятся дегенеративная артропатия, воспалительный моно- или олигоартрит, хронический эволютивный полиартрит. По наблюдениям Дорфмана и сотр. клинические суставные проявления составляют примерно 44% и выражаются ложноподагрическими или простыми ревматическими приступами, в то время как рентгенологические — 38%. Среди рентгенологических аспектов преобладают следующие два — хондро-кальциноз суставов (особенно колена) и субхондральные изменения, при этом нередко наблюдается их сочетание.
ж) Проявления гемохроматоза пищеварительного характера. Боли в животе редкое явление. Они ощучщаются в надчревной области, правом или левом подреберьи, вокруг пупочной зоне и пр., причем иногда весьма резкие и сопровождаются тошнотой и рвотой.
з) Поздний период гемохроматоза. Прогрессивно или внезапно генуинный гемохроматоз усугубляется, преимущественно на определенных органах. Сопутствующая инфекция также составляет частую причину смерти таких больных.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Изменения кожи при гемохроматозах
Синонимы: бронзовый диабет, цирроз печени пигментный, синдром Труазье—Ано—Шоффара, синдром Реклингхаузена—Аппельбаума.
Определение. Заболевание, вызванное наследственным дефектом обмена железа и сопровождающееся развитием пигментного цирроза печени, пигментации кожи, сахарного диабета и сердечной недостаточности.
Этиология и патогенез. Гемохроматоз относится к группе болезней «накопления», заключается в генетически обусловленном нарушении метаболизма железа и начинается задолго до проявления симптомов. Избыточное накопление железа в виде ферритина и гемосидерина происходит в паренхиматозных органах (чаще в печени, поджелудочной железе, реже в селезенке, сердце и других органах) с последующим их фиброзом и функциональной недостаточностью. Молекулярный механизм, лежащий в основе токсического действия железа,— это генерация свободных радикалов и перекисное окисление липидов. В коже и мышцах откладывается также железосодержащий пигмент — липофусцин.
Итог этого явления — вторичная воспалительно-склеротическая реакция тканей. Под влиянием избыточного содержания железа в коже, по-видимому, за счет усиления тирозин-тирозиназной активности, происходит усиление меланогенеза. На основании генетических и биохимических различий выделяют четыре типа гемохроматоза. Типы 1, 2 и 3 наследуются аутосомно-рецессивно, а тип 4 — аутосомно-доминантно.
Тип 1 является классическим и сопровождается перенасыщением трансферрина, повышением концентрации ферритина и содержания железа в ткани печени; генные локусы — 6р21.3, 1q21.
Тип 2 считается ювенильным и характеризуется значительным отложением железа во внутренних органах, ранним началом и быстрым прогрессирующим течением; генные локусы — 19р13, 1q21.
Тип 3 характеризуется высоким содержанием железа во внутренних органах, нормальными насыщением трансферрина и концентрацией ферритина в крови; локус гена — 7р22. Тип 4 сопровождается значительными изменениями биохимических показателей при минимальных отложениях гемосидерина во внутренних органах; локус гена — 2р32.
Также выделяют приобретенную (вторичную) форму гемохроматоза, которая развивается в результате избыточного поступления в организм железа. Среди вторичных гемохроматозов выделяют четыре вида. Первый (посттрансфузионный) развивается в результате частых повторных гемотрансфузий при лечении хронических анемий. Второй (алиментарный) регистрируется в африканском племени банту, а также у лиц, употребляющих в больших количествах железосодержащие тонизирующие напитки и алкоголь.
Третий (метаболический) возникает при нарушениях метаболизма железа при промежуточной талассемии, циррозе печени (после операции портокавального анастомоза), гепатитах В и С, неалкогольном стеатогепатозе, кожной порфирии, раковых заболеваниях, при закупорке протока поджелудочной железы. Четвертый (смешанный) отмечается при большой талассемии и некоторых видах дизэритропоэтической анемии.

Кисть при гемохроматозе
Частота. Наследственный гемохроматоз является одним из самых распространенных аутосомно-рецессивных заболеваний в Европе, Америке, Австралии с частотой гетерозигот 10—16%, развивающихся в среднем в 3—7 случаях на 1000 носителей гена наследственного гемохроматоза.
Возраст и пол. Эта болезнь в 95% случаев поражает мужчин, обычно в возрасте 40—60 лет, клинические проявления у них наиболее тяжелые и начинаются раньше, чем у женщин.
Общая характеристика. Характерна триада: поражение печени (цирроз у 92%), поджелудочной железы (сахарный диабет у 25—70%) и кожи (меланоз у 84%), однако полный симптомокомплекс наблюдается только в терминальной стадии. Примерно у 50% больных отмечают спленомегалию, артралгии, иногда нейропатии.
Поражение печени. Самый постоянный признак гемохроматоза. При пункционной биопсии обнаруживаются микронодулярный цирроз, большое количество зерен железа в печеночных и купферовских клетках, явления фиброза. Позднее присоединяется асцит, появляются «голова медузы», кровотечения из расширенных вен пищевода.
Поражения кожи. Меланоз кожи возникает на открытых участках, половых органах, в области крупных складок и старых рубцов. На пике заболевания пигментируется весь кожный покров. Пигментация варьирует от грязно-бурой до бронзовой, аспидной, иногда она может предшествовать развитию других симптомов за несколько лет. Кожа сухая, истонченная, с небольшим шелушением. В отличие от болезни Аддисона, слизистые оболочки в процесс вовлекаются редко, обнаруживается пигментация слизистых глаз, полости рта и гениталий.
По другим данным, слизистые поражаются в пятой части случаев. Также могут наблюдаться кожный зуд, атрофия кожи, ихтиозиформные изменения, алопеция, койлонихия, эритема ладоней, паукообразные гемангиомы.

Желтуха при гемохроматозе
Кардиальные проявления. Несмотря на то что отложения железа в сердце при наследственном гемохроматозе имеются в 90—100% случаев, клиническая симптоматика выявляется у трети больных. Поражение сердца может быть бессимптомным, однако выявляется, как правило, при углубленных исследованиях или провокационных пробах. Дисфункция миокарда обычно проявляется хронической застойной недостаточностью.
Эндокринные нарушения. Сахарный диабет может быть латентным, обычно он развивается на поздних стадиях болезни. Отмечается резистентность диабета к терапии. В результате гиперэстрогенемии у мужчин может развиться оволосение лобка по женскому типу, гипогонадизм, гинекомастия, снижение либидо.
Гистология кожи. Обнаруживают повышенное содержание меланина в базальном слое эпидермиса, отложение гемосидерина преимущественно вокруг сосудов, потовых желез.
Диагноз ставят на основании характерных клинических признаков, повышенной концентрации железа в сыворотке крови и определения процента насыщения трансферрина, концентрации ферритина. В классическом варианте и развернутой форме заболевание встречается не часто, но даже при наличии типичной клинической картины не редко диагностируется только на аутопсии или в случаях внезапной смерти при судебно-медицинских вскрытиях.
Течение и прогноз. Заболевание длительно протекает скрытно. Клинические признаки возникают обычно после 40 лет. Частая причина смерти — печеночная недостаточность вследствие цирроза печени, кровотечения из расширенных вен пищевода.
Лечение у терапевтов.
Гемохроматоз ( Бронзовый диабет , Пигментный цирроз )
Гемохроматоз – наследственное полисистемное заболевание, сопровождающееся активным всасыванием железа в ЖКТ и его последующей аккумуляцией во внутренних органах (сердце, поджелудочной железе, печени, суставах, гипофизе). Клиника гемохроматоза характеризуется бронзовой пигментацией кожи и слизистых оболочек, развитием цирроза печени, сахарного диабета, кардиомиопатии, артралгий, нарушения половой функции и т. д. Диагноз гемохроматоза подтверждается при определении повышенной экскреции железа с мочой, высокого содержания железа в сыворотке крови и биоптатах печени, а также с помощью рентгенографии, УЗИ, МРТ внутренних органов. Лечение пациентов с гемохроматозом основано на соблюдении диеты, введении дефероксамина, проведении кровопусканий, плазмафереза, гемосорбции, симптоматической терапии. При необходимости решается вопрос о трансплантации печени и артропластике.
Общие сведения
Гемохроматоз (бронзовый диабет, пигментный цирроз) – генетически обусловленное нарушение метаболизма железа, приводящее к отложению железосодержащих пигментов в тканях и органах и развитию полиорганной недостаточности. Заболевание, сопровождающееся характерным симптомокомплексом (пигментация кожи, цирроз печени и сахарный диабет) было описано в 1871 г., а в 1889 г. получило название гемохроматоза за характерную окраску кожи и внутренних органов. Частота наследственного гемохроматоза в популяции составляет 1,5-3 случая на 1000 населения. Мужчины болеют гемохроматозом в 2-3 раза чаще, чем женщины. Средний возраст развития патологии - 40-60 лет. Ввиду полисистемности поражения, изучением гемохроматоза занимаются различные клинические дисциплины: гастроэнтерология, кардиология, эндокринология, ревматология и др.
В этиологическом аспекте выделяют первичный (наследственный) и вторичный гемохроматоз. Первичный гемохроматоз связан с дефектом ферментных систем, приводящим к отложению железа во внутренних органах. В зависимости от генного дефекта и клинической картины выделяют 4 формы наследственного гемохроматоза:
- I - классический аутосомно-рецессивный, HFE-ассоциированный тип (более 95% случаев)
- II – ювенильный тип
- III - наследственный HFE-неассоциированный тип (мутации в трансферриновом рецепторе 2-го типа)
- IV– аутосомно-доминантный тип.
Вторичный гемохроматоз (генерализованный гемосидероз) развивается в результате приобретенной недостаточности ферментных систем, участвующих в обмене железа, и часто ассоциирован с другими заболеваниями, в связи с чем выделяют следующие его варианты: посттрансфузионный, алиментарный, метаболический, смешанный и неонатальный.
В клиническом течении гемохроматоз проходит 3 стадии: I - без перегрузки железом; II – с перегрузкой железом, но без клинических симптомов; III – с развитием клинических проявлений.
Причины гемохроматоза
Первичный наследственный гемохроматоз является заболеванием с аутосомно-рецессивным типом передачи. В его основе лежат мутации гена HFE, расположенного на коротком плече 6-ой хромосомы. Дефект HFE-гена приводит к нарушению трансферрин-опосредованного захвата железа клетками 12-перстной кишки, следствием чего является формирование ложного сигнала о дефиците железа в организме. В свою очередь, это способствует повышенному синтезу железосвязывающего белка DCT-1 энтероцитами и усиленной абсорбции железа в кишечнике (при нормальном поступлении микроэлемента с пищей). В дальнейшем происходит чрезмерное отложение железосодержащего пигмента гемосидерина во многих внутренних органах, гибель их функционально активных элементов с развитием склеротических процессов. При гемохроматозе ежегодно в организме человека накапливается 0,5-1,0 г железа, а проявления заболевания манифестируют при достижении общего уровня железа 20 г (иногда 40-50 г и больше).
Вторичный гемохроматоз развивается в результате избыточного экзогенного поступления железа в организм. Такое состояние может возникать при частых повторных гемотрансфузиях, неконтролируемом приеме препаратов железа, талассемии, некоторых видах анемии, кожной порфирии, алкогольном циррозе печени, хронических вирусных гепатитах В и С, злокачественных новообразованиях, следовании низкобелковой диете.
Симптомы гемохроматоза
Клиническая манифестация наследственного гемохроматоза приходится на зрелый возраст, когда содержание общего железа в организме достигает критических значений (20-40 г). В зависимости от преобладающих синдромов различают гепатопатическую (гемохроматоз печени), кардиопатическую (гемохроматоз сердца), эндокринологическую формы заболевания.
Заболевание развивается постепенно; в начальной стадии преобладают неспецифичные жалобы на повышенную утомляемость, слабость, похудание, снижение либидо. В этой стадии больных могут беспокоить боли в правом подреберье, сухость кожи, артралгии, обусловленные хондрокальцинозом крупных суставов. В развернутой стадии гемохроматоза формируется классический симптомокомплекс, представленный пигментацией кожи (бронзовая кожа), циррозом печени, сахарным диабетом, кардиомиопатией, гипогонадизмом.
Обычно наиболее ранним признаком гемохроматоза выступает появление специфической окраски кожи и слизистых оболочек, выраженной, главным образом, на лице, шее, верхних конечностях, в области подмышек и наружных гениталий, рубцов кожи. Интенсивность пигментации зависит от давности течения заболевания и варьирует от бледно-серого (дымчатого) до бронзово-коричневого цвета. Характерно выпадение волос на голове и туловище, вогнутая (ложкообразная) деформация ногтей. Отмечаются артропатии пястно-фаланговых, иногда коленных, тазобедренных и локтевых суставов с последующим развитием их тугоподвижности.
Практически у всех больных выявляется увеличение печени, спленомегалия, цирроз печени. Нарушение функции поджелудочной железы выражается в развитии инсулинзависимого сахарного диабета. В результате поражения гипофиза при гемохроматозе страдает половая функция: у мужчин развивается атрофия яичек, импотенция, гинекомастия; у женщин – аменорея и бесплодие. Гемохроматоз сердца характеризуется кардиомиопатией и ее осложнениями – аритмией, хронической сердечной недостаточностью, инфарктом миокарда.
В терминальной стадии гемохроматоза развивается портальная гипертензия, асцит, кахексия. Гибель пациентов, как правило, наступает вследствие кровотечения из варикозно расширенных вен пищевода, печеночной недостаточности, острой сердечной недостаточности, диабетической комы, асептического перитонита, сепсиса. Гемохроматоз значительно увеличивает риск развития рака печени (гепатоцеллюлярной карциномы).
Диагностика гемохроматоза
В зависимости от преобладающих симптомов пациенты с гемохроматозом могут обращаться за помощью к различным специалистам: гастроэнтерологу, кардиологу, эндокринологу, гинекологу, урологу, ревматологу, дерматологу. Между тем, диагностика заболевания едина при различных клинических вариантах гемохроматоза. После оценки клинических признаков больным назначается комплекс лабораторно-инструментальных исследований, позволяющих убедиться в правомерности диагноза.
Лабораторными критериями гемохроматоза служат значительное повышение уровня железа, ферритина и трансферрина в сыворотке крови, увеличение выведения железа с мочой, снижение общей железосвязывающей способности сыворотки крови. Диагноз подтверждается с помощью пункционной биопсии печени или кожи, в образцах которых обнаруживается отложение гемосидерина. Наследственная природа гемохроматоза устанавливается в результате проведения молекулярно-генетической диагностики.
С целью оценки тяжести поражения внутренних органов и прогноза заболевания исследуются печеночные пробы, уровень глюкозы крови и мочи, гликозилированный гемоглобин и др. Лабораторная диагностика гемохроматоза дополняется инструментальными исследованиями: рентгенографией суставов, ЭКГ, ЭхоКГ, УЗИ органов брюшной полости, МРТ печени и др.
Лечение гемохроматоза
Основной целью проводимой терапии служит удаление избытка железа из организма и недопущение развития осложнений. Больным с гемохроматозом назначается диета, предусматривающая ограничение пищевых продуктов с высоким содержанием железа (яблок, мяса, печени, гречневой крупы, шпината и пр.), легкоусвояемых углеводов. Запрещается прием мультивитаминов, аскорбиновой кислоты, БАДов, содержащих железо, алкоголя. Для выведения избытков железа из организма прибегают к кровопусканиям под контролем показателей гемоглобина, гематокрита крови, ферритина. С этой же целью могут использоваться экстракорпоральные методы гемокоррекции – плазмаферез, гемосорбция, цитаферез.
Патогенетическая медикаментозная терапия гемохроматоза основана на внутримышечном или внутривенном введении пациенту дефероксамина, связывающего ионы Fe3+. Одновременно проводится симптоматическое лечение цирроза печени, сердечной недостаточности, сахарного диабета, гипогонадизма. При выраженной артропатии определяются показания к проведению артропластики (эндопротезирования пораженных суставов). У пациентов с циррозом решается вопрос о проведении трансплантации печени.
Прогноз и профилактика
Несмотря на прогрессирующее течение заболевания, своевременная терапия позволяет продлить жизнь пациентов с гемохроматозом на несколько десятилетий. При отсутствии лечения средняя продолжительность жизни больных после диагностики патологии не превышает 4-5 лет. Наличие осложнений гемохроматоза (главным образом, цирроза печени и застойной сердечной недостаточности) является прогностически неблагоприятным признаком.
При наследственном гемохроматозе профилактика сводится к проведению семейного скрининга, раннему выявлению и началу лечения заболевания. Избежать развития вторичного гемохроматоза позволяет рациональное питание, контроль за назначением и приемом препаратов железа, проведением переливаний крови, отказ от приема алкоголя, наблюдение за больными с заболеваниями печени и системы крови.
Гемохромaтоз печени
Гемохроматоз печени – это генетическое аутосомно-рецессивное заболевание, характеризующееся повышенным всасыванием и отложением железа в печени и других паренхиматозных органах. В клинике превалирует триада признаков: цирроз, гиперпигментация кожных покровов, эндокринные нарушения. Диагностика основана на изучении семейного анамнеза, выявлении нарушений обмена железа, МРТ печени с последующей биопсией, выявлении гомозиготного носительства гена гемохроматоза. Специфическое лечение включает назначение препаратов, выводящих излишки железа из организма, эфферентные методики – кровопускание, цитаферез. Заболевание неизлечимо.

Гемохроматоз печени – наследственное заболевание, при котором происходит нарушение метаболизма железа в организме, его избыточное отложение в органах и тканях. Несмотря на системный характер нарушений, наиболее тяжело при гемохроматозе поражается печень – в ней развиваются цирротические изменения. Отложение железа в коже проявляется гиперпигментацией, в железах внутренней секреции – эндокринными нарушениями, сахарным диабетом.
Впервые патология была описана в 1871 г., с тех пор исследования в этой области не прекращаются. На сегодняшний день выявлен ген, отвечающий за развитие гемохроматоза, связанный с HLA-комплексом гистосовместимости. Ген этот рецессивный, поэтому для появления клиники гемохроматоза необходимо наличие данной мутации у обоих родителей пациента. Гемохроматоз печени – заболевание редкое, гетерозиготное носительство встречается у 10% населения, а гомозиготность – лишь в 0,3%. Мужчины страдают в десять раз чаще женщин.
Причины
Генетическая природа гемохроматоза печени и его тесная связь с HLA-комплексом гистосовместимости была доказана в 1976 году. В настоящее время ученым практически удалось выделить ген, отвечающий за развитие данного заболевания. Носительство гена может быть гомозиготным, при котором отмечается развернутая клиническая картина, и гетерозиготным. У носителей гетерозиготных генов обычно выявляется небольшое повышение уровня железа в крови, однако излишнего отложения в тканях, а значит и клинических проявлений, не возникает.
Патогенез
В норме утилизация железа организмом регулируется потребностями тканей в этом микроэлементе. Железо всасывается в начальных отделах тонкой кишки и связывается в крови с транспортным белком трансферрином. По мере необходимости железо поступает в ткани и там используется либо откладывается в связанной форме, в виде ферритина. Самые емкие депо железа – эритроциты, печень и мышцы. С течением времени ферритин в тканях начинает разрушаться с образованием пигмента гемосидерина. Не менее трети всех запасов железа хранится в виде гемосидерина, его количество повышается при нарушениях обмена железа.
В организме здорового человека в среднем содержится примерно 4 г железа. С пищей ежедневно поступает около 10-20 г железа, но потребляется из них не более десятой части, причем при необходимости перенос железа внутрь клеток может производиться даже против градиента концентрации. При полном заполнении депо железа данный элемент практически прекращает всасываться в кишечнике, а при его недостатке скорость всасывания возрастает в десятки раз.
При мутации гена гемохроматоза печени поломка в ферментной системе приводит к формированию ложного сигнала о низком уровне железа в организме. Ионы этого металла начинают всасываться в повышенном количестве, что в результате приводит к накоплению не менее чем 1 г излишков железа в год. После того, как весь пул железосвязывающих белков будет связан с металлом, железо, как сильный элемент, активирует окислительные процессы в клетке. Это приводит к образованию большого количества свободных радикалов, а те, в свою очередь, вызывают некроз клеток, повышенный синтез коллагена, раковое перерождение тканей.
Симптомы гемохроматоза печени
Для появления первых симптомов обычно требуется не менее 20 лет, пока общее содержание железа в организме не превысит 20-40 г. На начальном этапе заболевания, даже при наличии генетической предрасположенности, перегрузки организма железом не наблюдается. Следующим этапом является перегрузка тканей ионами железа без клинических проявлений. И только на поздней стадии появляются типичные клинические признаки.
Первыми проявлениями гемохроматоза печени на протяжении долгих лет могут служить лишь слабость, повышенная утомляемость, снижение половой функции у мужчин (снижение либидо и т. п.) и аменорея у женщин. Нарушение обмена железа приводит к кальцинозу суставов, трофическим изменениям в коже и хрящах, половых органах. На более поздних стадиях заболевания клиническая картина становится развернутой: отложение гемосидерина в коже сопровождается гиперпигментацией открытых мест, подмышечных впадин и промежности.
Из внутренних органов первой поражается печень: происходит некроз гепатоцитов, избыточное образование коллагена, что в будущем приводит к циррозу. Изначально печень увеличивается в размерах, становится плотной, болезненной при пальпации. Затем орган уменьшается, развивается симптоматика печеночно-клеточной недостаточности и портальной гипертензии. Более чем у 80% пациентов отмечаются эндокринопатии: поражаются гипофиз и эпифиз, щитовидная, поджелудочная и половые железы. Практически у всех больных с эндокринопатиями развивается сахарный диабет, зачастую инсулинозависимый.
Очень часто в процесс вовлекаются суставы, центральная нервная система. Отложение гемосидерина в сердце отмечается у 90-100% пациентов, но клиническая симптоматика возникает не более чем у трети больных. Гемохроматоз сердца проявляется кардиомиопатией, гипертрофией миокарда, тяжелой сердечной недостаточностью.
Диагностика
Консультация гепатолога необходима не только для оценки клинических данных, но также для подробного разбора семейного анамнеза, выявления наследственного характера заболевания. Если в ходе осмотра и беседы с пациентом возникает подозрение на гемохроматоз печени, назначается ряд дополнительных анализов и консультация генетика. УЗИ гепатобилиарной системы при гемохроматозе печени позволяет выявить значительное повышение эхогенности печеночной ткани за счет отложений гемосидерина.
Аналогичные изменения можно обнаружить и в других органах при проведении ультрасонографии поджелудочной железы, УЗИ щитовидной железы, ЭхоКГ. Если предварительный диагноз подтверждается с помощью МРТ печени, то пациент направляется на пункционную биопсию печени с последующим морфологическим исследованием биоптатов. Абсолютным доказательством правомочности диагноза является обнаружение дефектного гена гемохроматоза печени при кариотипировании.

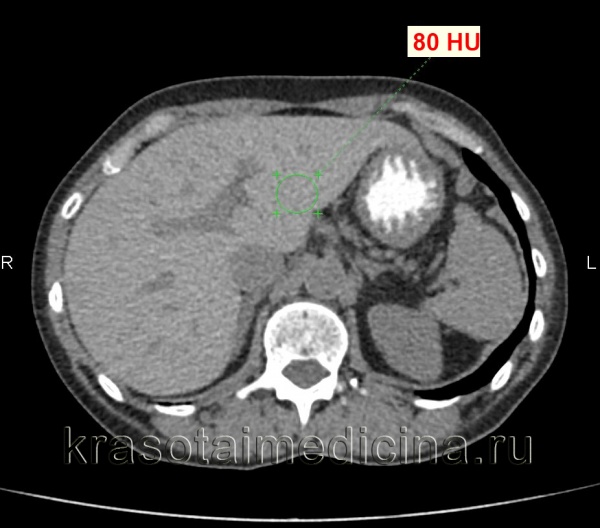
КТ органов брюшной полости. Диффузное повышение плотности печени до 80 ед. Хаунсфилда (преконтрастное изображение) за счет диффузного отложения железа.
Лечение гемохроматоза печени
Методов полного излечения патологии в современной гастроэнтерологии не существует, поэтому терапия направлена на купирование симптомов заболевания. Для начала назначается диета с пониженным содержанием железа и повышенным уровнем белка. В последующем используются методики, позволяющие усилить выведение железа из организма. Наиболее доступный способ уменьшить пул железа – кровопускание. Для правильного расчета объема кровопускания учитываются уровни гемоглобина, гематокрита, трансферрина. При заборе 500 мл крови теряется 200-250 мг железа. В среднем производится эксфузия 300 мл крови дважды в неделю.
Более сложным методом, требующим специального оборудования, является цитаферез – при этом осуществляется удаление клеточных элементов, а плазма возвращается в кровяное русло. Сеансы кровопусканий или цитафереза проводятся до развития умеренной анемии. Так как на фоне исходной анемии использование эфферентных методик ограничено, то в качестве подготовки и сопровождения цитафереза назначается рекомбинантный эритропоэтин. Данный препарат усиливает утилизацию железа, благодаря чему снижается его концентрация в тканях, повышается гемоглобин. Курс введения эритропоэтина – 10-15 недель.
Другим методом лечения гемохроматоза печени является использование дефероксамина – 500 мг этого препарата выводит из организма почти 45 мг железа. Курс лечения дефероксамином составляет не менее 30-40 дней. Одновременно проводят симптоматическую терапию цирроза печени, сердечной и печеночной недостаточности, сахарного диабета.
Течение заболевания длительное, а прогноз благоприятный лишь при своевременном начале лечения. Если патогенетическая терапия была инициирована до значительной перегрузки организма железом, развития цирроза, диабета и полиорганной недостаточности - выживаемость увеличивается на несколько десятилетий. В случае развития цирроза риск гепатоцеллюлярной карциномы возрастает в 200 раз. Смерть обычно наступает от печеночной недостаточности и ее осложнений. Профилактика не разработана.
Гемохроматоз сердца ( Пигментный миокардит , Сидерокардиоз )
Гемохроматоз сердца (сидерокардиоз, пигментный миокардит) – поражение сердца, обусловленное врожденным нарушением метаболизма железа, его неконтролируемой абсорбцией в кишечнике, избыточным содержанием в сыворотке крови и отложением в миокарде. Гемохроматоз сердца проявляется нарушениями сердечного ритма, недостаточностью кровообращения, артериальной гипотонией; сопровождается пигментацией кожи, циррозом печени, сахарным диабетом. Диагноз гемохроматоза сердца подтверждают данные лабораторного исследования метаболизма железа, ЭКГ, МРТ и КТ. При гемохроматозе сердца показаны диета, кровопускания, плазмаферез и гемосорбция, сердечные и гормональные препараты; при осложнениях - трансплантация печени, эндопротезирование суставов.
Гемохроматоз – полисистемное заболевание, обусловленное наследственным нарушением метаболизма железа, его избыточным накоплением в организме и токсическим повреждением тканей и органов. Основные клинические формы гемохроматоза включают поражение сердца, печени, эндокринных желез и суставов.
Поражение миокарда наблюдается в 80-90% случаев заболевания гемохроматозом; в кардиологии этот процесс обозначают как «дегенеративное ржавение» сердца. Из-за отложения чрезмерного количества пигмента гемосидерина, сердце и другие органы приобретают ржаво-бурую окраску, резко уплотняются и увеличиваются в размерах. При гемохроматозе сердца отмечаются дистрофические и атрофические изменения мышечных волокон с разрастанием фиброзной ткани (кардиосклероз), приводящие к снижению сократительной функции миокарда и развитию недостаточности кровообращения.
Гемохроматоз сердца наблюдается преимущественно у лиц мужского пола в возрасте 40-60 лет, т. к. у женщин имеется регулярная физиологическая потеря железа при менструациях.
Причины гемохроматоза сердца
Около 2/3 от общего количества железа в организме входит в состав гемоглобина эритроцитов, миоглобина, других белков и ферментов; 1/3 - депонирована в виде ферритина и гемосидерина в паренхиматозных клетках печени, почек, селезенки, мышцах, костном и головном мозге. Уровень железа регулируется динамикой его всасывания в ЖКТ, преимущественно в верхних отделах тонкой кишки. В норме из 10-20 мг железа, поступающего с пищей, энтероцитами абсорбируется 1-2 мг.
При гемохроматозе сердца отмечается интенсивное всасывание железа в кишечнике и резкое увеличение его запасов: в миокарде - в 5-25 раз, в печени и поджелудочной железе - в 50-100 раз. Свободное железо, обладая сильным редокс-потенциалом, способно запускать цепные свободнорадикальные реакции и вызывать токсическое повреждение макромолекул белков, липидов и нуклеиновых кислот.
Гемохроматоз сердца может быть первичным и вторичным. Первичный гемохроматоз сердца – наследственное заболевание, проявляющееся в четырех формах: аутосомно-рецессивной; ювенильной; связанной с мутацией в трансферриновом рецепторе 2-го типа и аутосомно-доминантной.
Вторичный гемохроматоз сердца развивается при избыточном поступлении железа в организм в случае длительного неконтролируемого приема железосодержащих препаратов, при повторных частых гемотрансфузиях.
Симптомы гемохроматоза сердца
Многообразие симптоматики гемохроматоза определяется поражением различных органов: сердца, кожных покровов, печени, поджелудочной железы, гипофиза, суставов и др. Течение заболевания обычно медленное, с постепенным развитием и преобладанием отдельных проявлений. Классическая триада, наиболее характерная для терминальной стадии гемохроматоза, включает цирроз печени, пигментацию кожи, сахарный диабет.
Имеются случаи заболевания с первичным поражением сердца без развития сахарного диабета и пигментации кожи. При гемохроматозе отмечаются выраженный фиброз сердечной мышцы с преимущественным нарушением проводящей системы сердца. Гемохроматоз проявляется увеличением размеров сердца и расширением его полостей, сбоем сердечного ритма (пароксизмальной тахикардией, мерцательной аритмией), право- или левожелудочковой сердечной недостаточностью, артериальной гипотонией, периферическими отеками.
При гемохроматозе сердца кожа приобретает бронзовый оттенок, особенно на открытых участках (лице, шее, конечностях, области половых органов). Цирроз печени характерен для 90-95% случаев гемохроматоза и сопровождается болями в животе, диспепсией, гепатомегалией, исхуданием, иногда не резко выраженной желтухой. Сахарный диабет, наблюдающийся на поздних стадиях у 70 – 80 % больных гемохроматозом сердца, проявляется жаждой, полиурией.
При гемохроматозе может отмечаться недоразвитие половых органов, снижение либидо, бесплодие, атрофия яичек и феминизация - у мужчин, нарушение менструального цикла - у женщин. Возможно развитие артропатий, периферических невритов, надпочечниковой недостаточности, редко - портальной гипертонии с расширением вен пищевода.
Прогрессирование гемохроматоза может осложняться нарушениями ритма сердца, сердечной недостаточностью, инфарктом миокарда, острой печеночной недостаточностью, асцитом, внутренним кровотечением из вен пищевода, тромбозом сосудов печени и селезенки, иногда - печеночной и диабетической комой, раком печени.
Диагностика гемохроматоза сердца
Диагноз гемохроматоза сердца устанавливается по наличию характерной клинической картины, результатам лабораторных и инструментальных исследований (ЭКГ, ЭхоКГ, МРТ и МСКТ органов брюшной полости, рентгенографии суставов, биопсии печени).
Признаки кардиомиопатии при гемохроматозе сердца обычно сочетаются с пигментацией кожи, циррозом печени, патологией эндокринной системы, сахарным диабетом, поражением суставов.
В диагностике ранних стадий гемохроматоза сердца большое значение имеет определение уровня железа, ферритина и трансферрина в сыворотке крови, общей железосвязывающей способности сыворотки (ОЖСС) и процента насыщения трансферрина железом (НТЖ), десфераловый тест. Для гемохроматоза сердца характерно значительное увеличение количества сывороточного железа (до 54-72 мкмоль/л) и ферритина; снижение показателей ОЖСС и трансферрина, диспротеинемия, гипергликемия. Важные признаки перегрузки железом при гемохроматозе сердца – это повышение коэффициента НТЖ до 60-90%, резкое увеличение выделения железа с мочой при нагрузке десфералом (> 2 мг в течение 6 ч).
С целью оценки степени тяжести гемохроматоза сердца, признаков поражения других органов проводятся общий и биохимический анализ крови, определение глюкозы и гликозилированного гемоглобина крови, общий анализ мочи. Для электрокардиограммы типичны признаки гипертрофии левого желудочка и внутрижелудочковой блокады, говорящие о длительной перегрузке левого желудочка и нарушении сердечного ритма.
Рентгенография суставов при гемохроматозе сердца позволяет выявить признаки гипертрофического остеоартрита, хондрокальциноза суставных хрящей и менисков. Молекулярно-генетическое исследование используется для определения наследственной природы избытка железа в организме. МРТ и КТ обнаруживают повышенную плотность печени.
Для подтверждения диагноза гемохроматоза выполняют биопсию печени с количественным определением концентрации железа в печеночной ткани, цитологическим исследованием биоптатов на наличие отложений избытка гемосидерина в гепатоцитах и портального цирроза. Дифференциальную диагностику гемохроматоза сердца проводят с приобретенным гемосидерозом, миокардитом, ишемической болезнью сердца, ревматизмом, сахарным диабетом.
Лечение гемохроматоза сердца
Лечение гемохроматоза сердца направлено на снижение количества железа в организме, предупреждение развития серьезных осложнений и проводится с использованием немедикаментозных, медикаментозных и хирургических методов. Пациентам с гемохроматозом сердца показана диета с ограничением продуктов и препаратов с высоким содержанием железа, алкоголя, легкоусвояемых углеводов.
Систематические кровопускания (1-2 раза в неделю по 500 мл крови), гирудотерапия, плазмаферез и гемосорбция помогают снизить уровень запасов железа в организме, улучшают самочувствие больных с гемохроматозом сердца. Кровопускания можно выполнять амбулаторно до снижения показателей метаболизма железа (Fe, Hb, ферритина) до нижней границы нормы. После кровопусканий проводится введение плазмы или альбумина, рекомендуется прием пищи, богатой белком.
Патогенетическое лечение гемохроматоза включает внутримышечное или внутривенное введение дефероксамина, способствующего усиленному выведению железа с мочой и предупреждающего развитие цирроза в печени. В комплексной терапии нарушений функции печени, сердечно-сосудистой и эндокринной системы при гемохроматозе сердца используют инсулин, гормональные, сердечные препараты. Хирургическое лечение показано больным с гемохроматозом сердца при развитии цирроза печени (трансплантации печени) и выраженной артропатии (эндопротезирование суставов).
Прогноз гемохроматоза сердца
Прогноз гемохроматоза сердца неблагоприятный при поздней диагностике заболевания, наличии тяжелого поражения миокарда, печени, поджелудочной железы. В отсутствии лечения больные живут не более 4-5 лет. Причинами смерти при гемохроматозе сердца могут быть сердечная недостаточность (около 33%), цирроз печени (32%), рак печени (23%), интеркуррентная патология. При своевременном лечении гемохроматоза сердца продолжительность жизни существенно возрастает.
Пациентам с гемохроматозом сердца ежеквартально показан контрольный осмотр с участием кардиолога, гастроэнтеролога, эндокринолога и гематолога.
Читайте также:
